
Cytosinstruktur, funksjoner, egenskaper, syntese
De cytosin Det er en nitrogenholdig base av pyrimidintypen, som brukes til biosyntese av cytidin-5'-monofosfat og deoksycytidin-5'-monofosfat. Disse forbindelsene tjener for henholdsvis biosyntese av deoksyribonukleinsyre (DNA) og ribonukleinsyre (RNA). DNA lagrer genetisk informasjon og RNA har forskjellige funksjoner.
I levende ting finnes ikke cytosin i fri form, men danner ofte ribonukleotider eller deoksyribonukleotider. Begge typer forbindelser har en fosfatgruppe, en ribose og en nitrogenbase..
2-karbonet av ribose har en hydroksylgruppe (-OH) på ribonukleotider, og et hydrogenatom (-H) på deoksyribonukleotider. Avhengig av antall tilstedeværende fosfatgrupper er det cytidin-5'-monofosfat (CMP), cytidin-5'-difosfat (CDP) og cytidin-5'-trifosfat (CTP).
Deoksygenererte ekvivalenter kalles deoksycytidin-5'-monofosfat (dCMP), deoksycytidin-5'-difosfat (dCDP) og deoksycytidin-5'-trifosfat (dCTP)..
Cytosin, i sine forskjellige former, deltar i forskjellige funksjoner, for eksempel DNA- og RNA-biosyntese, glykoproteinbiosyntese og regulering av genuttrykk..
Artikkelindeks
- 1 Struktur og egenskaper
- 2 Biosyntese
- 2.1 Regulering av biosyntese
- 2.2 Pyrimidiner, som cytosin, resirkuleres
- 3 Roll i DNA-biosyntese
- 4 Roll i å stabilisere strukturen til DNA
- 5 Rollen til cytosinrike regioner i DNA
- 6 Roll i RNA-biosyntese
- 7 Roll i glykoproteinbiosyntese
- 8 Cytosine og kreft kjemoterapeutiske behandlinger
- 9 Referanser
Struktur og egenskaper
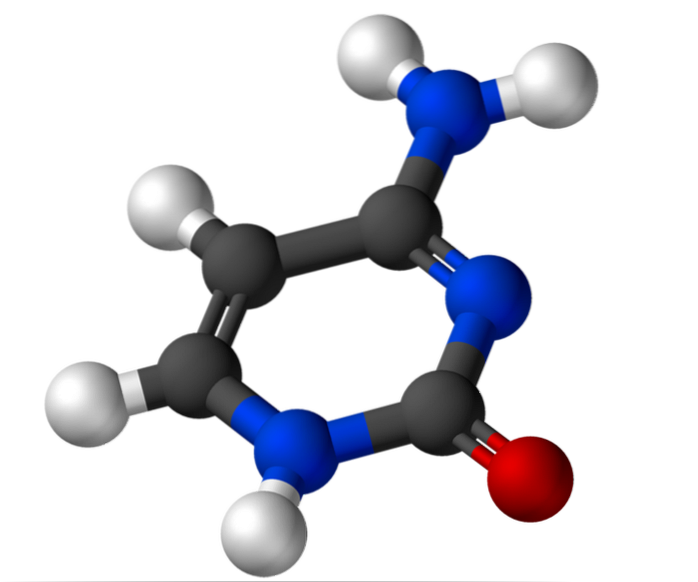
Cytosin, 4-amino-2-hydroksypyrimidin, har den empiriske formelen C4H5N3O, hvis molekylvekt er 111,10 g / mol, og renses som et hvitt pulver.
Strukturen til cytosin er en plan, aromatisk heterosyklisk ring. Bølgelengden med maksimal absorbans (ʎmaks) er ved 260 nm. Smeltetemperaturen til cytosin overstiger 300 ° C.
For å danne et nukleotid er cytosin bundet kovalent, gjennom nitrogen 1, via en N-beta-glykosidbinding til 1'-karbonet i ribose. 5'-karbonet er forestret med en fosfatgruppe.
Biosyntese
Pyrimidinnukleotidbiosyntese har en felles vei, bestående av seks enzymkatalyserte trinn. Banen begynner med karbamoylfosfatbiosyntese. I prokaryoter er det bare ett enzym: karbamoylfosfatsyntase. Dette er ansvarlig for syntesen av pyrimidiner og glutamin. I eukaryoter er det karbamoylfosfatsyntase I og II, som er ansvarlige for henholdsvis biosyntese av glutamin og pyrimidiner.
Det andre trinnet består av dannelsen av N-karbamoylaspartat, fra karboylfosfat og aspartat, en reaksjon katalysert av aspartattranscabamoylase (ATCase).
Det tredje trinnet er syntesen av L-dihydrorotat, som forårsaker lukking av pyrimidinringen. Dette trinnet katalyseres av dihydrootase..
Det fjerde trinnet er dannelsen av orotat, som er en redoksreaksjon katalysert av dihydroorotatdehydrogenase..
Det femte trinnet består av dannelsen av orotidylat (OMP) ved bruk av fosforibosylpyrofosfat (PRPP) som substrat, og orotatfosforibosyltransferase som en katalysator..
Det sjette trinnet er dannelsen av uridylat (uridin-5'-monofosfat, UMP), en reaksjon katalysert av en OMP-dekarboksylase..
De neste trinnene består av fosforylering av UMP, katalysert av kinaser, for å danne UTP, og overføring av en aminogruppe fra glutamin til UTP for å danne CTP, en reaksjon katalysert av CTP-syntetase..
Regulering av biosyntese
Hos pattedyr forekommer regulering på nivået av karbamoylfosfat syntase II, et enzym som finnes i cytosolen, mens karbamoylfosfat syntase I er mitokondrie.
Karbamoylfosfatsyntase II reguleres av negativ tilbakemelding. Dens regulatorer, UTP og PRPP, er henholdsvis hemmer og aktivator av dette enzymet.
I ikke-levervev er karbamoylfosfatsyntase II den eneste kilden til karbamoylfosfat. Mens i leveren, under betingelser med overskudd av ammoniakk, produserer karbamoylfosfatsyntase I, i mitokondriene, karbamoylfosfat, som transporteres til cytosolen, hvorfra den går inn i pyrimidinbiosynteseveien..
Et annet reguleringspunkt er OMP-dekarboksylase, som er regulert av konkurransehemming. Dets reaksjonsprodukt, UMP, konkurrerer med OMP om bindingsstedet på OMP-dekarboksylase..
Pyrimidiner, som cytosin, resirkuleres
Resirkulering av pyrimidiner har den funksjonen å gjenbruke pyrimidiner uten behov for de novo biosyntese og unngå nedbrytningsveien. Resirkuleringsreaksjonen katalyseres av pyrimimidinfosforibosyltransferase. Den generelle reaksjonen er som følger:
Pyrimidin + PRPP -> pyrimidinnukleosid 5'-monofosfat + PPi
Hos virveldyr finnes pyrimimidinfosforibosyltransferase i erytrocytter. Substratpyrimidinene for dette enzymet er uracil, tymin og orotat. Cytosin resirkuleres indirekte fra uridin-5'-monofosfat.
Roll i DNA-biosyntese
Under DNA-replikering kopieres informasjonen i DNA-en til DNA-en av en DNA-polymerase..
RNA-biosyntese krever deoksynukleotidtrifosfat (dNTP), nemlig: deoksytymidintrifosfat (dTTP), deoksycytidintrifosfat (dCTP), deoksyadenintrifosfat (dATP) og deoksyguanintrifosfat (dGTP). Reaksjonen er:
(DNA)n rester + dNTP -> (DNA)n + 1 rest + PPi
Hydrolyse av uorganisk pyrofosfat (PPi) gir energi til RNA-biosyntese.
Rollen i å stabilisere strukturen til DNA
I DNA-dobbeltspiralen er en enstrenget purin knyttet til den motstrengte pyrimidinet ved hydrogenbindinger. Dermed er cytosin alltid knyttet til guanin av tre hydrogenbindinger: adenin er knyttet til tymin av to hydrogenbindinger..
Hydrogenbindinger brytes når en løsning av renset nativt DNA, ved pH 7, utsettes for temperaturer over 80 ºC. Dette fører til at DNA-dobbeltspiralen danner to separate tråder. Denne prosessen er kjent som denaturering..
Temperaturen der 50% av DNA blir denaturert er kjent som smeltetemperaturen (Tm). DNA-molekyler hvis forhold mellom guanin og cytosin er høyere enn thymin og adenin, har høyere Tm-verdier enn de hvis forholdet mellom baser er invers.
Ovenstående beskrevet utgjør det eksperimentelle beviset for at et større antall hydrogenbindinger bedre stabiliserer de innfødte DNA-molekylene..
Rollen til cytosinrike regioner i DNA
Nylig ble det funnet at DNA fra kjernen til menneskelige celler kan adoptere strukturer med interspersed motiv (iM). Disse strukturene forekommer i regioner som er rike på cytosin.
IM-strukturen består av fire DNA-tråder, i motsetning til klassisk dobbeltstrenget DNA som har to tråder. Mer spesifikt er to parallelle duplekskjeder iscenesatt i en antiparallell orientering, og holdes sammen av et par hemiprotonerte cytosiner (C: C+).
I det menneskelige genomet finnes iM-strukturer i regioner som promotorer og telomerer. Antall iM-strukturer er høyere under G1 / S-fasen av cellesyklusen, der transkripsjonen er høy. Disse regionene er proteigenkjenningssteder involvert i aktivering av transkripsjonsmaskineriet..
På den annen side, i regionene som er rike på påfølgende guaninbasepar (C), har DNA en tendens til å vedta A-helix-formen under dehydratiserende forhold. Denne formen er typisk for RNA og blandede DNA-RNA dobbeltbånd under transkripsjon og replikasjon, og på bestemte tidspunkter når DNA er bundet til proteiner..
Det har vist seg at sammenhengende baseregioner av cytosin danner et elektropositivt plaster i den største spalten av DNA. Derfor antas disse regionene å binde seg til proteiner, og disponere visse genomiske regioner til genetisk skjørhet..
Roll i RNA-biosyntese
Under transkripsjon blir informasjonen i DNA kopiert til RNA av en RNA-polymerase. RNA-biosyntese krever nukleosidtrifosfat (NTP), nemlig: cytidintrifosfat (CTP), uridintrifosfat (UTP), adenintrifosfat (ATP) og guanintrifosfat (GTP). Reaksjonen er:
(RNA)n rester + NTP -> (RNA)n + 1 rest + PPi
Hydrolyse av uorganisk pyrofosfat (PPi) gir energi til RNA-biosyntese.
Roll i glykoproteinbiosyntese
Den sekvensielle overføringen av heksoser for å danne oligosakkarider, O-koblet til proteiner, skjer fra nukleotidforløpere.
Hos virveldyr består det siste trinnet i O-bundet oligosakkaridbiosyntese av tilsetningen av to sialinsyrerester (N-acetylneuramin) fra en forløper av cytidin-5'-monofosfat (CMP). Denne reaksjonen forekommer i transgolgisekken.
Cytosine og kreft kjemoterapeutiske behandlinger
Tetrahydrofolatsyre (FH4) er en kilde til -CH grupper3, og er nødvendig for biosyntese av dTMP fra dUMP. I tillegg dannes FH2. Reduksjonen av FH2 til FH4 krever en reduktase av folat og NADPH. Noen folatreduktasehemmere, som aminopterin og metotreksat, brukes i kreftbehandlinger.
Metotreksan er en konkurransedyktig hemmer. Folatreduktase binder 100 ganger mer affinitet til denne hemmeren enn til substratet. Aminopterin fungerer på en lignende måte.
Inhiberingen av folatreduktase hindrer indirekte biosyntese av dTMP, og derfor den av dCTP. Direkte inhibering skjer av hemmere av tymidylatsyntetaseenzymet, som katalyserer dTMP fra dUMP. Disse inhibitorene er 5-fluorouracil og 5-fluoro-2-deoksyuridin..
For eksempel er 5-fluoroacyl ikke i seg selv en hemmer, men blir først omdannet i resirkuleringsveien til deoksyuridinmfosfat d (FdUMP), som binder og hemmer tymidylatsyntetase..
Stoffer som er analoge med glutamin, azaserin og acivicin, hemmer glutaminamidotransferase. Azarin var et av de første stoffene som ble oppdaget som fungerer som en selvmordsinaktivator.
Referanser
- Assi, H.A., Garavís, M., González, C., og Damha, M.J. 2018. i-Motif DNA: strukturelle trekk og betydning for cellebiologi. Nuclei Acids Research, 46: 8038-8056.
- Bohinski, R. 1991. Biokjemi. Addison-Wesley Iberoamericana, Wilmington, Delaware.
- Devlin, T.M. 2000. Biokjemi. Redaksjonell Reverté, Barcelona.
- Lodish, H., Berk, A., Zipurski, S.L., Matsudaria, P., Baltimore, D., Darnell, J. 2003. Cellular and molecular biology. Redaksjonell Medica Panamericana, Buenos Aires, Bogotá, Caracas, Madrid, Mexico, São Paulo.
- Nelson, D. L., Cox, M. M. 2008. Lehninger-Principles of biochemistry. W.H. Freeman, New York.
- Voet, D. og Voet, J. 2004. Biokjemi. John Wiley and Sons, USA.



Ingen har kommentert denne artikkelen ennå.