
Epimers egenskaper, formasjon og eksempler
De epimerer de er diastereoisomerer der bare ett av deres achiralsentre er forskjellige i romlig konfigurasjon; i motsetning til enantiomerer, der alle achiralsentrene har forskjellige konfigurasjoner, og representerer et par speilbilder som ikke kan legges på hverandre.
Resten av diastereoisomerer (for eksempel geometriske isomerer) kan ha mer enn to sentre med forskjellige konfigurasjoner. Derfor er en stor andel stereoisomerer diastereoisomerer; mens epimerer er mye mindre, men ikke av den grunn, mindre viktige.
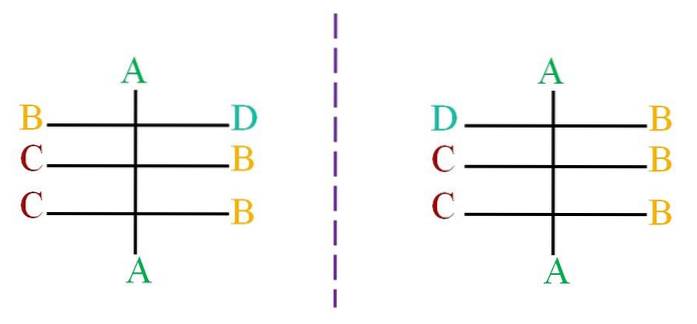
Anta en struktur med et skjelett av svarte atomer knyttet til bokstavene A, B, C og D (øvre bilde). Den stiplede linjen representerer speilet og viser at molekylparet ovenfor ikke er enantiomerer, siden alle deres chirale sentre har samme konfigurasjon; bortsett fra det første senteret, knyttet til bokstavene B og D..
Molekylet til venstre har bokstaven D vendt mot høyre side, mens molekylbrevet D til høyre vender mot venstre side. For å vite hva konfigurasjonen til hver vil være, bruk Cahn-Ingold-Prelog-systemet (R-S).
Artikkelindeks
- 1 Egenskaper for epimerer
- 2 Trening
- 2.1 Tautomerisering
- 3 eksempler
- 3.1 Glukose anomerer
- 3.2 Isomerer av mentol
- 4 Referanser
Kjennetegn ved epimerer
Hovedkarakteristikken til epimerer ligger utelukkende i et achiralt (eller stereogent) senter. Endring av romlig orientering av D og B kan føre til mer stabile eller ustabile konformatorer; det vil si at rotasjonene av enkeltbindingene får to atomer eller grupper av klumpete atomer til å møtes eller bevege seg bort.
Fra dette perspektivet kan den ene epimeren være mye mer stabil enn den andre. Den som, ved å rotere bindingene, genererer mer stabile strukturer, vil være epimeren med den største tendensen til å danne seg i likevekt..
Å gå tilbake til bokstavene, D og B kan være veldig store, mens C er et lite atom. Således er epimeren til høyre mer stabil, siden D og C funnet til venstre for de to første sentrene lider av mindre sterisk hindring..
Mikroskopisk blir dette en karakteristikk for paret epimerer som blir vurdert; men makroskopisk blir forskjellene forsterket, og ender for eksempel opp med forskjellige smeltepunkter, brytningsindekser, NMR-spektre (i tillegg til mange andre egenskaper).
Men innen biologi og enzymkatalyserte reaksjoner, er det her epimerer skiller seg enda mer ut; den ene kan metaboliseres av kroppen, mens den andre ikke er det.
Opplæring
Hvordan dannes epimerer? Gjennom en kjemisk reaksjon som kalles epimerisering. Hvis begge epimerer ikke er veldig forskjellige i stabilitet, etableres en epimeriseringsvekt, som ikke er noe annet enn en interkonvertering:
EpA <=> EpB
Der EpA er epimer A, og EpB er epimer B. Hvis en av dem er mye mer stabil enn den andre, vil den ha en høyere konsentrasjon og vil forårsake det som kalles mutarotasjon; det vil si at den vil kunne endre retningen til en polarisert lysstråle.
Epimerisering er kanskje ikke likevekt, og derfor irreversibel. I disse tilfellene oppnås en racemisk blanding av EpA / EpB-diastereoisomerer..
Den syntetiske veien til epimerer varierer avhengig av reagensene som er involvert, reaksjonsmediet og prosessvariablene (bruk av katalysatorer, trykk, temperatur osv.).
Av denne grunn må dannelsen av hvert par av epimerer studeres individuelt fra de andre; hver med sine egne kjemiske mekanismer og systemer.
Tautomerisering
Ut av alle epimerdannelsesprosesser kan tautomerisering av to diastereoisomerer betraktes som et generelt eksempel..
Dette består av en likevekt der molekylet adopterer en keton (C = O) eller enol (C-OH) form. Når ketonformen er omgjort, endres konfigurasjonen av karbon ved siden av karbonylgruppen (hvis den er chiral), og genererer et par epimerer.
Et eksempel på det ovennevnte er paret cis-decalone og trans-decalone.
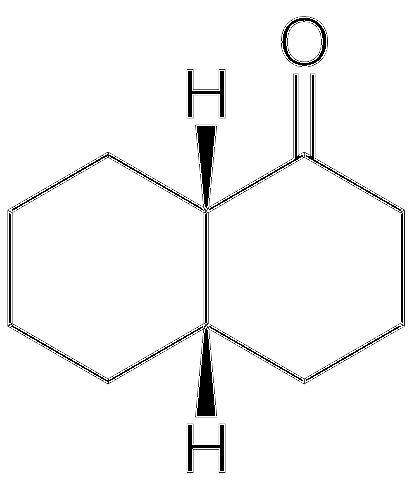
Strukturen til cis-decalone er vist ovenfor. H-atomene er på toppen av de to ringene; mens i trans-decalone, er den ene over ringene, og den andre er under. Karbonet til venstre for C = O-gruppen er det chirale sentrum, og derfor det som skiller epimerer.
Eksempler
Glukose anomerer
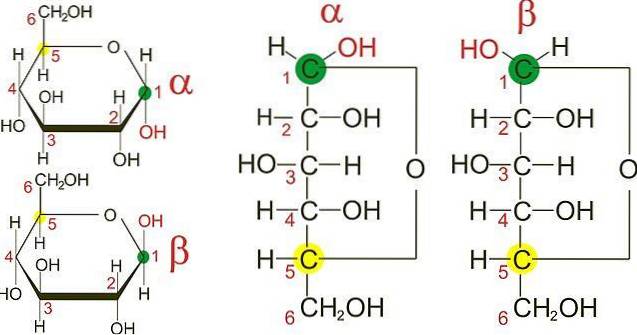
Det øvre bildet viser furanringene til de to anomerer av D-glukose: α og β. Fra ringene kan man se at OH-gruppene på karbon 1 er funnet enten i samme retning som den tilstøtende OH, i α-anomeren, eller i motsatte retninger, som i β-anomeren..
Fisher-projeksjonene til begge anomerer (til høyre for bildet) gjør forskjellen mellom de to epimerer, som selv er anomerer, enda tydeligere. Imidlertid kan to α-anomerer ha forskjellige romlige konfigurasjoner på et av de andre karbonene, og derfor være epimerer..
I C-1 i Fisher-projeksjonen for α-anomeren "ser" OH-gruppen til høyre, mens den i β-anomeren "ser" til venstre..
Isomerer av mentol

På bildet har du alle stereoisomerer av mentolmolekylet. Hver kolonne representerer et par enantiomerer (observer nøye), mens radene tilsvarer diastereoisomerer.
Så hva er epimerer? De må være de som nesten ikke skiller seg ut i den romlige posisjonen til et enkelt karbon..
(+) - mentol og (-) - neoisomenthol er epimerer, og dessuten diastereoisomerer (de er ikke i samme kolonne). Hvis observert i detalj, i både -OH- og -CH-gruppene3 komme ut av planet (over ringen), men i (-) - neoisomenthol peker isopropylgruppen også ut av planet.
Ikke bare (+) - mentol er epimer av (-) - neoisomenthol, men også (+) - neomenthol. Sistnevnte skiller seg bare ved at gruppen -CH3 peker nedover flyet. Andre epimerer er:
-(-) - isomentol og (-) - neomentol
-(+) - isomentol og (+) - neomentol
-(+) - neoisomenthol og (-) - neomenthol
-(+) - neomenthol og (-) - neoisomenthol
Disse stereoisomerer representerer et praktisk eksempel for å klargjøre begrepet epimerer, og du kan se at fra flere diastereoisomerer kan mange bare skille seg inn i et enkelt asymmetrisk eller chiralt karbon..
Referanser
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. (10th utgave.). Wiley pluss.
- Carey F. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Uruguay Educa klasserom. (s.f.). Epimere. Gjenopprettet fra: aulas.uruguayeduca.edu.uy
- Wikipedia. (2018). Epimer. Gjenopprettet fra: en.wikipedia.org/wiki/Epimer
- Fray J. M. (2014). Undersøkelse av epimerdannelse i amidkoblingsreaksjoner: Et eksperiment for avanserte studenter. School of Chemistry, University of Nottingham, University Park, Nottingham NG7 2RD, Storbritannia. J. Chem. Utdanning. 2014, 91, 1, 136-140
- Reist & kol. (nitten nitti fem). Racemisering, enantiomerisering, diastereomerisering og epimerisering: deres betydning og farmakologiske betydning. Chirality 7: 396-400.


Ingen har kommentert denne artikkelen ennå.