
Glutation-egenskaper, struktur, funksjoner, biosyntese
De glutation (GSH) er et lite tripeptidmolekyl (med bare tre aminosyrerester) ikke-protein som deltar i mange biologiske fenomener som enzymatisk mekanikk, makromolekylers biosyntese, mellommetabolisme, oksygentoksisitet, intracellulær transport, etc..
Dette lille peptidet, som finnes i dyr, planter og noen bakterier, regnes som en "buffer" oksido-reduserende, siden det er en av de viktigste forbindelsene med lav molekylvekt som inneholder svovel og mangler toksisitet forbundet med cysteinrester.
Noen sykdommer hos mennesker har vært assosiert med mangelen på spesifikke enzymer av glutationmetabolisme, og dette er på grunn av dens mange funksjoner for å opprettholde kroppshomeostase.
Underernæring, oksidativt stress og andre patologier som mennesker lider, kan påvises som en drastisk reduksjon i glutation, og det er derfor det noen ganger er en god indikator på helsetilstanden til kroppssystemene.
For planter er glutation på samme måte en viktig faktor for deres vekst og utvikling, siden den også utfører funksjoner i flere biosyntetiske veier og er viktig for cellulær avgiftning og intern homeostase, der den fungerer som en kraftig antioksidant..
Artikkelindeks
- 1 Funksjoner
- 2 Struktur
- 3 funksjoner
- 3.1 Koenzym
- 3.2 Oppbevaring av cystein
- 3.3 Proteinfolding
- 3.4 Funksjon i erytrocytter
- 3.5 Fremmedstoffskifte
- 3.6 Oksidativ tilstand av celler
- 4 Biosyntese
- 4.1 Redusert glutation (GSH)
- 4.2 Oksidert glutation (GSSG)
- 5 Fordeler med inntaket
- 5.1 Kreft
- 5.2 HIV
- 5.3 Muskelaktivitet
- 5.4 Leverpatologier
- 5.5 Antioksidant
- 5.6 "Absorpsjon"
- 6 Bivirkninger
- 7 Referanser
Kjennetegn
De første studiene utført i forhold til den subcellulære plasseringen av glutation viste at den er tilstede i mitokondriene. Senere ble det også observert i regionen som tilsvarer kjernefysisk matrise og i peroksisomer.
For tiden er det kjent at rommet der konsentrasjonen er mest rikelig er i cytosolen, siden det er aktivt produsert der og transporteres til andre cellulære rom som mitokondriene..
I pattedyrceller ligger glutationkonsentrasjonen i millimolområdet, mens i redusert form (GSH) i blodplasma finnes i mikromolare konsentrasjoner..
Denne intracellulære konsentrasjonen ligner konsentrasjonen av glukose, kalium og kolesterol, viktige elementer for mobil struktur, funksjon og metabolisme..
Noen organismer har analoge eller varierende glutationmolekyler. Protozoiske parasitter som påvirker pattedyr har en form som kalles "trypanothion", og i noen bakterier er denne forbindelsen erstattet av andre svovelmolekyler som tiosulfat og glutamylcystein..
Enkelte plantearter har, i tillegg til glutation, homologe molekyler som har andre rester enn glycin i den C-terminale enden (homoglutation), og som er preget av å ha funksjoner som ligner på det aktuelle tripeptidet..
Til tross for at det finnes andre forbindelser som ligner på glutation i forskjellige organismer, er dette en av "tiolene" som finnes i den høyeste konsentrasjonen intracellulært..
Det høye forholdet som normalt eksisterer mellom den reduserte formen (GSH) og den oksyderte formen (GSSG) av glutation er et annet kjennetegn ved dette molekylet..
Struktur
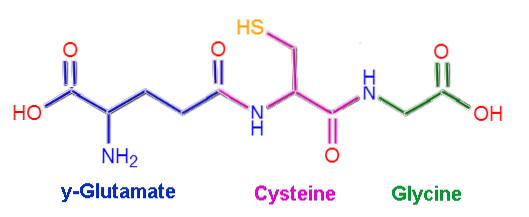
Glutation eller L-γ-glutamyl-L-cysteinyl-glysin, som navnet antyder, består av tre aminosyrerester: L-glutamat, L-cystein og glysin. Cystein- og glysinrester er koblet sammen gjennom vanlige peptidbindinger, det vil si mellom a-karboksylgruppen i en aminosyre og a-aminogruppen i den andre..
Imidlertid er bindingen som oppstår mellom glutamat og cystein ikke typisk for proteiner, siden den forekommer mellom γ-karboksyldelen av R-gruppen av glutamat og α-aminogruppen i cystein. Kalles γ-binding.
Dette lille molekylet har en molær masse på litt over 300 g / mol, og tilstedeværelsen av γ-bindingen ser ut til å være avgjørende for immuniteten til dette peptidet mot virkningen av mange aminopeptidasenzymer..
Funksjoner
Som nevnt er glutation et protein som deltar i mange cellulære prosesser i dyr, planter og visse prokaryoter. I denne forstand er dens generelle deltakelse i:
-Prosessene med proteinsyntese og nedbrytning
-Dannelsen av DNA-ribonukleotidforløpere
-Regulering av aktiviteten til noen enzymer
-Beskyttelse av celler i nærvær av reaktive oksygenarter (ROS) og andre frie radikaler
-Signaltransduksjon
-Genetisk uttrykk og i
-Apoptose eller programmert celledød
Koenzym
Glutation har også blitt bestemt for å fungere som et koenzym i mange enzymatiske reaksjoner, og den delen av dens betydning er relatert til dens evne til å transportere aminosyrer i form av γ-glutamylaminosyrer intracellulært..
Glutation som kan forlate cellen (som den gjør i redusert form) er i stand til å delta i oksidasjonsreduksjonsreaksjoner i nærheten av plasmamembranen og det omkringliggende celle miljøet, som beskytter celler mot skade mot forskjellige klasser av oksidasjonsmidler.
Lagring av cystein
Dette tripeptidet fungerer også som en kilde for cysteinlagring og bidrar til å opprettholde den reduserte tilstanden til sulfhydrylgruppene i proteinene inne i cellen og jernholdig tilstand i hemgruppen til proteinene som inneholder nevnte medfaktor..
Proteinfolding
Når den deltar i proteinfolding, ser det ut til å ha en viktig funksjon som et reduksjonsmiddel for disulfidbroer som har blitt dannet uhensiktsmessig i proteinstrukturer, noe som vanligvis skyldes eksponering for oksidasjonsmidler som oksygen, hydrogenperoksid, peroksynitrit og noen superoksider.
Erytrocytfunksjon
I erytrocytter, redusert glutation (GSH) produsert av enzymet glutation reduktase, som bruker NADPH produsert av pentosefosfatveien, bidrar til fjerning av hydrogenperoksid gjennom reaksjonen katalysert av et annet enzym: glutationperoksidas, som produserer vann og oksidert glutation (GSSG).
Nedbrytningen av hydrogenperoksid og dermed forebygging av akkumulering i erytrocyttene forlenger levetiden til disse cellene, siden det unngår oksidativ skade som kan oppstå i cellemembranen og som kan ende i hemolyse..
Xenobiotisk metabolisme
Glutation er også en viktig aktør i metabolismen av xenobiotika, takket være virkningen av glutation S-transferase-enzymer som genererer glutationkonjugater som deretter kan metaboliseres intracellularly..
Det er klokt å huske at begrepet "fremmedfrykt" brukes om medisiner, miljøforurensende stoffer og kjemiske kreftfremkallende stoffer som en organisme utsettes for..
Oksidativ tilstand av celler
Siden glutation finnes i to former, en redusert og en oksidert, bestemmer forholdet mellom de to molekylene redoksstilstanden til celler. Hvis GSH / GSSG-forholdet er større enn 100, betraktes cellene som sunne, men hvis det er nær 1 eller 10, kan det være en indikator på at cellene er i en tilstand av oksidativt stress.
Biosyntese
Glutation-tripeptidet syntetiseres i celler, både i planter og dyr, ved virkningen av to enzymer: (1) γ-glutamylcysteinsyntetase og (2) glutation-syntetase (GSH-syntetase), mens nedbrytning eller "nedbrytning" avhenger av virkningen av enzymet γ-glutamyl-transpeptidase.
I planteorganismer blir hvert av enzymene kodet av et enkelt gen, og defekter i noen av proteinene eller deres kodende gener kan forårsake dødelighet i embryoer.
Hos mennesker, som hos andre pattedyr, er det viktigste stedet for glutation-syntese og eksport leveren, spesielt i leverceller (hepatocytter) som omgir venekanalene som transporterer blod og andre stoffer til og fra det aktuelle organet.
Syntese de novo glutation, dets regenerering eller gjenvinning, krever energi fra ATP for å oppstå.
Redusert glutation (GSH)
Redusert glutation er avledet fra aminosyrene glycin, glutamat og cystein, som allerede nevnt, og syntesen av den begynner med aktivering (ved bruk av ATP) av γ-karboksylgruppen av glutamat (fra R-gruppen) for å danne et mellomliggende acylfosfat, som blir angrepet av α-aminogruppen av cystein.
Denne første to aminosyrekondensasjonsreaksjonen katalyseres av y-glutamylcysteinsyntetase og påvirkes vanligvis av den intracellulære tilgjengeligheten av aminosyrene glutamat og cystein..
Det således dannede dipeptidet kondenseres deretter med et glycinmolekyl takket være virkningen av GSH-syntetase. Under denne reaksjonen skjer en aktivering med ATP av a-karboksylgruppen av cystein også for å danne et acylfosfat og således favorisere reaksjonen med glycinresten..
Oksidert glutation (GSSG)
Når redusert glutation deltar i oksidasjonsreduksjonsreaksjoner, består den oksyderte formen faktisk av to glutationmolekyler bundet sammen gjennom disulfidbroer; det er av denne grunn at den oksyderte formen forkortes med initialene "GSSG".
Dannelsen av den oksyderte arten av glutation avhenger av et enzym kjent som glutationperoksidase eller GSH peroksidase, som er en peroksidase som inneholder et selenocystein (en cysteinrest som i stedet for å ha et svovelatom har et selenatom) på plass aktiv.
Interkonversjonen mellom oksidert og redusert form skjer takket være deltakelse av en GSSG-reduktase eller glutationreduktase, som bruker NAPDH for å katalysere reduksjonen av GSSG i nærvær av oksygen, med samtidig dannelse av hydrogenperoksid.
Fordeler med inntaket
Glutation kan administreres oralt, topisk, intravenøst, intranasalt eller forstøvet for å øke den systemiske konsentrasjonen hos pasienter som lider av oksidativt stress, for eksempel.
Kreft
Forskning på oral administrering av glutation antyder at inntaket kan redusere risikoen for oral kreft, og at når den administreres i forbindelse med oksidativ kjemoterapi, reduserer den de negative effektene av behandlingen hos kreftpasienter..
HIV
Vanligvis har pasienter smittet med det ervervede immunsviktvirus (HIV) intracellulær glutationmangel i både røde blodlegemer og T-celler og monocytter, som bestemmer deres korrekte funksjon.
I en studie av Morris et al., Ble det vist at tilførsel av glutation til makrofager fra HIV-positive pasienter betydelig forbedret funksjonen til disse cellene, spesielt mot infeksjoner med opportunistiske patogener som f.eks. M. tuberculosis.
Muskelaktivitet
Andre studier har å gjøre med forbedring av kontraktil aktivitet i muskler, antioksidativt forsvar og oksidativ skade forårsaket som respons på iskemi / reperfusjonsskader etter oral administrering av GSH under fysisk motstandstrening..
Leverpatologier
Det har i sin tur blitt ansett at dets inntak eller intravenøs administrering har funksjoner i forebygging av fremdriften av noen typer kreft og i reduksjon av celleskader som oppstår som et resultat av visse leverpatologier..
Antioksidant
Selv om ikke alle rapporterte studier er utført på humane pasienter, men vanligvis er tester i dyremodeller (vanligvis murine), bekrefter resultatene oppnådd i noen kliniske studier effektiviteten av eksogent glutation som en antioksidant..
Av denne grunn brukes den til behandling av grå stær og glaukom, som et "anti-aldringsprodukt", for behandling av hepatitt, mange hjertesykdommer, hukommelsestap og for å styrke immunforsvaret, og for klarering etter tungmetall og narkotikaforgiftning.
"Absorpsjon"
Eksogent administrert glutation kan ikke komme inn i celler med mindre det hydrolyseres til dets bestanddeler aminosyrer. Derfor er den direkte effekten av administrasjonen (oral eller intravenøs) av denne forbindelsen økningen av den intracellulære konsentrasjonen av GSH takket være bidraget til aminosyrene som er nødvendige for dens syntese, som effektivt kan transporteres til cytosolen..
Bivirkninger
Selv om inntak av glutation anses å være "trygt" eller ufarlig, er det ikke gjort nok studier på bivirkningene..
Fra de få rapporterte studiene er det imidlertid kjent at det kan ha negative effekter som skyldes interaksjonen med andre legemidler, og som kan være helseskadelig i ulike fysiologiske sammenhenger..
Hvis det tas på lang sikt, ser det ut til at de virker for å redusere sinknivået for mye, og hvis det i tillegg inhaleres, kan det gi alvorlige astmaanfall hos astmatiske pasienter.
Referanser
- Allen, J., og Bradley, R. (2011). Effekter av oral glutationtilskudd på systemiske oksidative stress-biomarkører hos frivillige mennesker. Tidsskriftet for alternativ og komplementær medisin, 17(9), 827-833.
- Conklin, K. A. (2009). Antioksidanter i kosten under kreftkjemoterapi: Innvirkning på kjemoterapeutisk effektivitet og utvikling av bivirkninger. Ernæring og kreft, 37(1), 1-18.
- Meister, A. (1988). Glutation Metabolism and Its Selective Modification. Journal of Biological Chemistry, 263(33), 17205-17208.
- Meister, A., & Anderson, M. E. (1983). Glutation. Ann. Rev Biochem., 52, 711-760.
- Morris, D., Guerra, C., Khurasany, M., Guilford, F., & Saviola, B. (2013). Glutation Tilskudd forbedrer makrofag funksjoner i HIV. Journal of Interferon & Cytokine Research, elleve.
- Murray, R., Bender, D., Botham, K., Kennelly, P., Rodwell, V., & Weil, P. (2009). Harper's Illustrated Biochemistry (28. utg.). McGraw-Hill Medical.
- Nelson, D. L., og Cox, M. M. (2009). Lehninger prinsipper for biokjemi. Omega-utgaver (5. utg.). https://doi.org/10.1007/s13398-014-0173-7.2
- Noctor, G., Mhamdi, A., Chaouch, S., Han, Y. I., Neukermans, J., Marquez-garcia, B.,… Foyer, C. H. (2012). Glutation i planter: en integrert oversikt. Plante, celle og miljø, 35, 454-484.
- Pizzorno, J. (2014). Glutation! Undersøkende medisin, 1. 3(1), 8-12.
- Qanungo, S., Starke, D. W., Pai, H. V, Mieyal, J. J., & Nieminen, A. (2007). Glutathion Supplementation Potentiates Hypoxic Apoptosis by S-Glutathionylation of p65-NFkB. Journal of Biological Chemistry, 282(25), 18427-18436.
- Ramires, P. R., og Ji, L. L. (2001). Glutationstilskudd og trening øker hjerteinfarktresistens mot iskemi-reperfusjon in vivo. Ann. J. Physiol. Heart Circ. Physiol., 281, 679-688.
- Sies, H. (2000). Glutation og dens rolle i mobilfunksjoner. Gratis radikal biologi og medisin R, 27(99), 916-921.
- Wu, G., Fang, Y., Yang, S., Lupton, J. R., og Turner, N. D. (2004). Glutation metabolisme og dens implikasjoner for helsen. American Society for Nutritional Sciences, 489-492.



Ingen har kommentert denne artikkelen ennå.