
Guaninegenskaper, struktur, formasjon og funksjoner
De guanin Det er en nitrogenholdig base som tjener til biosyntese av guanylat 5'-monofosfat og deoksyguanylat 5'-monofosfat. Begge stoffene er henholdsvis en del av RNA og DNA, som lagrer den genetiske informasjonen til celler.
Ribonukleinsyre (RNA) og deoksyribonukleinsyre (DNA) består av nukleotider, som består av en nitrogenholdig base festet til et sukker og en fosfatgruppe.
Guanin, i tillegg til å være en del av nukleinsyrer, deltar i sine former av nukleosider monofosfat, difosfat og trifosfater (GMP, BNP og GTP) i prosesser som energimetabolisme, oversettelse av det intracellulære signalet, fotoreseptorers fysiologi og vesikelfusjon.
Artikkelindeks
- 1 Kjemisk struktur
- 2 funksjoner
- 3 Biosyntese
- 4 Funksjon
- 5 Relaterte sykdommer
- 5.1 Lesch-Nyhan syndrom
- 5.2 Økt PRPP-syntaseaktivitet
- 5.3 von Gierke syndrom
- 6 Referanser
Kjemisk struktur
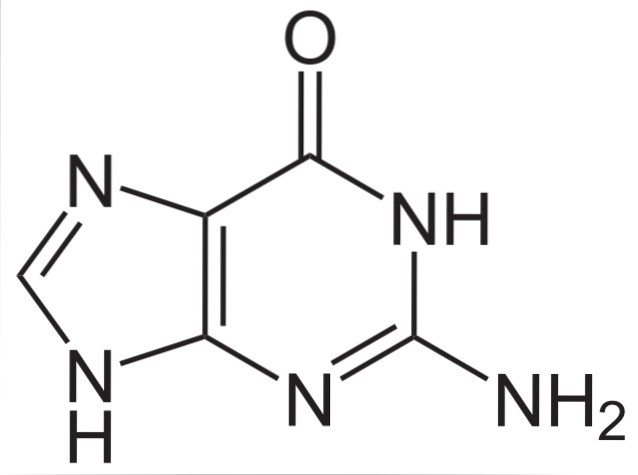
Den kjemiske strukturen til guanin (2-amino-6-hydroksypurin) er en heterosyklisk purinring, som består av et system med to koblede ringer: den ene ringen er pyrimidin og den andre ringen er imidazol..
Den heterosykliske ringen av guanin er flat og med noen konjugerte dobbeltbindinger. I tillegg har den to tautomere former, keto- og enolformene, mellom C-1 og N-6-gruppene..
Kjennetegn
Karakteristikken til guanin er som følger:
- Guanin er et apolært stoff. Det er uoppløselig i vann, men det er løselig i konsentrerte oppløsninger av sterke syrer eller baser.
- Det kan isoleres som et hvitt fast stoff, med empirisk formel C5H5N5O og molekylvekt 151,3 g / mol.
- DNA-egenskapen til å absorbere lys ved 260 nm skyldes delvis den kjemiske strukturen til guanin.
- I DNA danner guanin tre hydrogenbindinger. C-6 karbonylgruppen er en hydrogenbindingsakseptor, N-1-gruppen og C-2-aminogruppen er hydrogenbindingsdonorer.
Av denne grunn tar det mer energi å bryte en binding mellom en guanin og et cytosin, enn det til et adenin med et tymin, siden sistnevnte par er koblet av bare to hydrogenbindinger..
- I cellen finnes den alltid som en del av nukleinsyrer eller som GMP, BNP og GTP, aldri i sin frie form.
Biosyntese
Guaninmolekylet, som andre puriner, syntetiseres de novo fra 5-fosforibosyl-1-pyrofosfat (PRPP), gjennom reaksjoner katalysert av enzymer.
Det første trinnet består av tilsetning av en aminogruppe, fra glutamin, til PRPP og 5-fosforibosylamin (PRA) dannes.
Deretter, i en ordnet sekvens, tilsettes glysin, aspartat, glutamin, formiat og karbondioksid til PRA. På denne måten dannes en mellommetabolitt kalt inosin 5'-monofosfat (IMP)..
I løpet av denne prosessen brukes fri energi fra hydrolyse av ATP (adenosin 5'-trifosfat), som produserer ADP (adenosin 5'-difosfat) og Pi (uorganisk fosfat)..
En oksidasjon av IMP er avhengig av NAD+ (nikotinamidadenindinukleotid), produserer xantin 5'-monofosfat (XMP). Etterfølgende tilsetning av en aminogruppe til XMP produserer guanylatmolekylet.
Reguleringen av guanylatbiosyntese finner sted i begynnelsen, når PRA dannes, og til slutt når IMP-oksidasjon oppstår. Regulering skjer ved negativ tilbakemelding: et GMP-nukleotid hemmer enzymer i begge trinn.
Under metabolsk nedbrytning av nukleotider resirkuleres nitrogenholdige baser. GMP dannes av enzymet hypoksantin-guanin fosforibosyltransferase, og overfører en fosribosylgruppe fra PRPP til guanin.
Funksjon
Siden guanin ikke finnes i sin frie form, er dens funksjoner assosiert med GMP, BNP og GTP. Noen av dem er nevnt nedenfor:
- Guanosin 5'-trifosfat (GTP) fungerer som et reservoar med fri energi. Gamma-fosfatgruppen i GTP kan overføres til adenosin-5'-trifosfat (ADP) for å danne ATP. Denne reaksjonen er reversibel, og katalyseres av nukleosiddifosfatkinase..
- GMP er den mest stabile formen av nukleotidet som inneholder guanin. Gjennom hydrolyse danner GMP syklisk GMP (cGMP), som er en andre messenger under intracellulær signalering, i oversettelsesveiene. For eksempel i fotoreseptor og kjemoreseptorceller av lukt.
- CGMP deltar i avslapning av blodkar i glatt muskulatur under nitrogenoksidbiosyntese i endotelceller.
- GTP gammafosfathydrolyse fungerer som en gratis energikilde for proteinbiosyntese i ribosomer.
- Hellicase-enzymer krever fri energi fra GTP-hydrolyse for å skille DNA-dobbeltspiralen under DNA-replikering og transkripsjon.
- I hippocampusneuroner reguleres virkningen av spenningsstyrte natriumkanaler av hydrolyse av GTP til BNP..
Beslektede sykdommer
Høye nivåer av urinsyre i blod og urin har vært assosiert med tre forskjellige metabolske feil, som vi vil se nedenfor..
Lesch-Nyhan syndrom
Det er preget av en mangel på HPRT (hypoxanthine-guanine phosphoribosyl transferase), et enzym som er viktig for resirkulering av hypoxanthine og guanine. I dette tilfellet øker PRPP-nivået, og IMP og GMP, to viktige regulatorer i det innledende stadiet av purinsyntese, blir ikke dannet. Alt dette favoriserer biosyntese de novo av puriner.
Økt PRPP-syntaseaktivitet
Dette gir en økning i PRPP-nivåene. Denne metabolitten fungerer som en aktivator av glutamin PRPP-amidotransferase, som er ansvarlig for syntesen av 5-fosforibosylamin, og øker biosyntese. de novo puriner.
Von Gierke syndrom
Det er en sykdom relatert til lagring av glykogen type I. Pasienter med dette syndromet har en defekt glukose 6-fosfatase. Dette gir en økning i glukose 6-fosfatnivåer, som tjener til syntese av ribose 5-fosfat, via pentosefosfat..
Ribose 5-fosfat er startmetabolitten for PRPP biosyntese. I likhet med de to tidligere tilfellene fører dette til en økning i biosyntese de novo av puriner.
Økt urinsyre i blod og urin forårsaker symptomer som er kjent som urinsyregikt. I tilfelle av Lesch Nyhan syndrom mangler pasienter fullstendig aktiviteten til HPRP-enzymet, noe som fører til manifestasjon av andre symptomer, inkludert lammelse og mental retardasjon..
HPRP-genet er lokalisert på X-kromosomet, og mutasjoner i dette genet påvirker hannene. Det er ingen behandling for å behandle nevrologiske problemer. Symptomer forbundet med økt urinsyre behandles med allopurinol.
Referanser
- Dawson, R. et al. 1986. Data for biokjemisk forskning. Clarendon Press, Oxford.
- Horton, R; Moran, L; Scrimgeour, G; Perry, M. And Rawn, D. 2008. Prinsipper for biokjemi. 4. utgave. Pearson Education.
- Mathews, Van Holde, Ahern. 2001. Biokjemi. 3. utgave.
- Murray, R; Granner, D; Mayes, P. And Rodwell, V. 2003. Harpers illustrerte biokjemi. 26. utgave. McGraw-Hill selskaper.
- Nelson, DL og Cox, M. 1994. Lehninger. Prinsipper for biokjemi. 4. utgave. Ed omega.
- Sigma-Aldrich. 2019. Kjemisk ark for guanin. Wide Web-adresse: sigmaaldrich.com.



Ingen har kommentert denne artikkelen ennå.