
Jernmetallstruktur, typer, egenskaper

De jernholdig metall De er de som inneholder jern (Fe), så vel som små mengder andre metaller som tilsettes for å gi visse gunstige egenskaper til legeringene. Selv om jern kan eksistere i forskjellige oksidasjonstilstander, er +2 (jernholdig) og +3 (jern) den vanligste.
Imidlertid refererer begrepet "jern" tilstedeværelsen av jern uavhengig av dets oksidasjonstilstand i materialet. Jern er det fjerde mest utbredte elementet i jordskorpen, men globalt er det det viktigste jordelementet. Derfor har jernholdige metaller historisk og industrielt hatt en rolle i utviklingen av mennesket..

Dette har vært tilfelle på grunn av sin store overflod og modifiserbare egenskaper. Disse jernholdige metaller starter fra utvinning av jern fra mineralogiske kilder, slik som: hematitt (FetoELLER3), magnetitt (Fe3ELLER4) og sideritt (FeCO3). På grunn av ytelse er disse oksyder mest ønsket i jernbearbeiding.
Det øverste bildet viser et glødende støpejern "ildens tunge". Av alle jernholdige metaller består det viktigste av en jernlegering med små mengder karbon tilsatt: stål..
Artikkelindeks
- 1 Struktur
- 2 Egenskaper og egenskaper
- 3 eksempler
- 3.1 Smed eller jern
- 3.2 Råjern eller råjern
- 3.3 Rent jern
- 3.4 Støpejern (støperi)
- 3,5 Grått jern
- 3.6 Duktilt jern
- 3.7 Stål
- 4 Stål og dets applikasjoner
- 4.1 Karbon eller konstruksjonsstål
- 4.2 Silisiumstål
- 4.3 Galvanisert stål
- 4.4 Rustfritt stål
- 4.5 Manganstål
- 4.6 Invar stål
- 5 Referanser
Struktur
Fordi jern er hovedkomponenten i jernholdige metaller, består strukturene av krystallinske deformasjoner av deres rene faste stoff.
Derfor er jernholdige legeringer som stål ikke noe annet enn interstitiell inkludering av andre atomer i krystallarrangementet av jern..
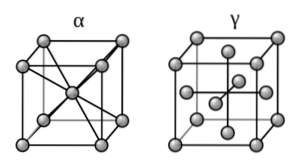
Hva er denne ordningen? Jern danner allotroper (forskjellige faste strukturer) avhengig av temperaturen det utsettes for, og endrer magnetiske egenskaper. Dermed presenterer den ved romtemperatur et bcc-arrangement, også kjent som alfa-jern (kuben til venstre, øvre bilde).
På den annen side, i en rekke høye temperaturer (912-1394 (ºC)), manifesterer den arrangementet ccp eller fcc: jern-gamma (kuben til høyre). Når denne temperaturen er overskredet, går jernet tilbake til bcc-formen for til slutt å smelte.
Denne endringen i alfa-gammastruktur er kjent som fasetransformasjon. Gamma-fasen er i stand til å "fange" karbonatomer, mens alfafasen ikke er det.
Således, når det gjelder stål, kan strukturen visualiseres som sett med jernatomer som omgir et karbonatom..
På denne måten avhenger strukturen til jernholdige metaller av fordelingen av fasene til jern og atomene til andre arter i det faste stoffet..
Kjennetegn og egenskaper
Rent jern er et mykt og veldig duktilt metall, veldig følsomt for korrosjon og oksidasjon fra eksterne faktorer. Men når det inkluderer forskjellige proporsjoner av et annet metall eller karbon, får det nye egenskaper og egenskaper..
Faktisk er det disse endringene som gjør jernholdige metaller nyttige for utallige bruksområder..
Jernlegeringer er generelt sterke, holdbare og tøffe, med lyse grålige farger og magnetiske egenskaper..
Eksempler
Smijern eller søtt
Den har et karboninnhold på mindre enn 0,03%. Den er sølvfarget, ruster lett og sprekker internt. I tillegg er det duktilt og støpbart, en god elektrisitetsleder og vanskelig å sveise..
Det er typen jernholdig metall som mennesket først brukte til fremstilling av våpen, redskaper og bygninger. Den brukes for tiden i tallerkener, nagler, trelliser, etc. Siden det er en god elektrisk leder, brukes den i kjernen av elektromagneter.
Råjern eller støpejern
I det første masovnsproduktet inneholder den 3-4% karbon og spor av andre elementer som silisium, magnesium og fosfor. Hovedbruken er å gripe inn i produksjonen av andre jernholdige metaller.
Rent jern
Det er et gråhvitt metall med magnetiske egenskaper. Til tross for hardheten er den sprø og sprø. Smeltepunktet er høyt (1500 ºC.) Og det oksiderer raskt.
Det er en god elektrisk leder, og det er derfor den brukes i elektriske og elektroniske komponenter. Ellers nytter det lite.
Støpejern (støperi)
De har et høyt karboninnhold (mellom 1,76% og 6,67%). De er hardere enn stål, men sprøere. De smelter ved en lavere temperatur enn rent jern, rundt 1100 ºC.
Fordi den er støpbar, er det mulig å produsere stykker av forskjellige størrelser og kompleksitet med den. I denne jerntypen brukes gråstøpejern, som gir stabilitet og formbarhet..
De har en høyere motstand mot korrosjon enn stål. Dessuten er de billige og tette. De har flyt ved relativt lave temperaturer og er i stand til å fylle formene.
De har også gode kompresjonsegenskaper, men er sprø og går i stykker før de bøyes, så de er ikke egnet for veldig forseggjorte stykker..
Grått jern
Det er det vanligste støpejernet, og den grå fargetone skyldes tilstedeværelsen av grafitt. Den har en karbonkonsentrasjon mellom 2,5% og 4%; i tillegg inneholder den 1-3% silikon for å stabilisere grafitten.
Den har mange av egenskapene til grunnleggende støpejern, som er veldig flytende. Den er ufleksibel og bøyer seg kort før den brytes.
Ductil jern
Karbon tilsettes, i form av sfærisk granitt, i en konsentrasjon mellom 3,2% og 3,6%. Den sfæriske formen av grafitt gir større slagfasthet og smidbarhet enn grå jern, slik at den kan brukes i detaljerte og kantede design.
Stål
Karboninnhold mellom 0,03% og 1,76%. Blant egenskapene er hardhet, utholdenhet og motstand mot fysisk innsats. Generelt ruster de lett. De er sveisbare og kan bearbeides i smiingen eller mekanisk.
De har også større hardhet og mindre flyt enn støpejern. Av denne grunn trenger de høye temperaturer for å strømme i formene..
Stål og dets applikasjoner

Det finnes flere typer stål, hver med forskjellige bruksområder:
Karbon eller konstruksjonsstål
Karbonkonsentrasjonen kan variere og etablere fire former: mildt stål (0,25% karbon), semi-søtt stål (0,35% karbon), semi-hardt stål (0,45% karbon) og hardt (0,5%).
Den brukes til fremstilling av verktøy, stålplater, jernbanevogner, spiker, skruer, biler og båter.
Silisiumstål
Også kalt elektrisk stål eller magnetisk stål. Silisiumkonsentrasjonen varierer mellom 1% og 5%, Fe varierer mellom 95% og 99%, og karbon har 0,5%.
I tillegg tilsettes mindre mengder mangan og aluminium. Den har stor hardhet og høy elektrisk motstand. Den brukes til fremstilling av magneter og elektriske transformatorer.
Galvanisert stål
Den er belagt med sinkbelegg som beskytter den mot rust og korrosjon. Derfor er det nyttig for å lage rørdeler og verktøy..
Rustfritt stål
Den har en sammensetning av Cr (14-18%), Ni (7-9%), Fe (73-79%) og C (0,2%). Det er motstandsdyktig mot oksidasjon og korrosjon. Det brukes i produksjon av bestikk så vel som skjæremateriale.
Manganstål
Sammensetningen er Mn (10-18%), Fe (82-90%) og C (1,12%). Den er hard og slitesterk. Brukes på togskinner, safer og rustning.
Invar stål
Den har 36% Ni, 64% Fe og 0,5% karbon. Den har en lav utvidelseskoeffisient. Den brukes i konstruksjonen av indikatorvekter; for eksempel: målebånd.
Referanser
- Whitten, Davis, Peck & Stanley. (2008). Kjemi. 8. utg., CENGAGE Learning.
- Administrator. (19. september 2017). Hva er jern, hvor kommer det fra og hvor mange typer jern det er. Hentet 22. april 2018 fra: termiser.com
- Wikipedia. (2018). Jern. Hentet 22. april 2018 fra: en.wikipedia.org
- Metaller. Generelle egenskaper. Ekstraksjon og klassifisering av metaller. Hentet 22. april 2018 fra: edu.xunta.gal
- Jose Ferrer. (Januar 2018). Metallurgisk karakterisering av jernholdige og ikke-ferreal materialer. Hentet 22. april 2018 fra: steemit.com
- Essays, Storbritannia. (November 2013). Grunnleggende strukturer av jernholdige metaller. Hentet 22. april 2018 fra: ukessays.com
- Cdang. (7. juli 2011). Iron Alpha & Iron Gamma. [Figur]. Hentet 22. april 2018 fra: commons.wikimedia.org
- Włodi. (15. juni 2008). Fletter i rustfritt stål. [Figur]. Hentet 22. april 2018 fra: commons.wikimedia.org



Ingen har kommentert denne artikkelen ennå.