
Aldehyder struktur, egenskaper, bruksområder og eksempler

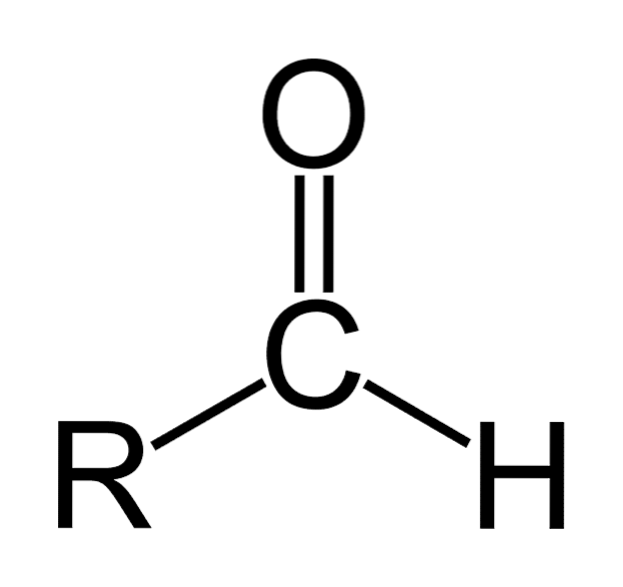
De aldehyder de er organiske forbindelser som har den generelle formelen RCHO. R representerer en alifatisk eller aromatisk kjede; C til karbon; O til oksygen og H til hydrogen. De er preget av å ha en karbonylgruppe som ketoner og karboksylsyrer, og derfor kalles aldehyder også karbonylforbindelser.
Karbonylgruppen gir aldehydet mange av dets egenskaper. De er forbindelser som lett oksideres og er veldig reaktive mot nukleofile tilsetninger. Dobbeltbindingen til karbonylgruppen (C = O) har to atomer som har forskjeller i deres grådighet for elektroner (elektronegativitet).
Oksygen tiltrekker seg elektroner med større kraft enn karbon, slik at elektronskyen beveger seg mot den, noe som gjør dobbeltbindingen mellom karbon og oksygen polær i naturen, med et betydelig dipolmoment. Dette gjør aldehyder til polare forbindelser..
Aldehydenes polaritet vil påvirke deres fysiske egenskaper. Kokepunktet og løseligheten til aldehyder i vann er høyere enn ikke-polare kjemiske forbindelser med lignende molekylvekter, slik det er tilfellet med hydrokarboner..
Aldehyder med mindre enn fem karbonatomer er oppløselige i vann, siden hydrogenbindinger dannes mellom oksygenet i karbonylgruppen og vannmolekylet. Å øke antall karbon i hydrokarbonkjeden gir imidlertid en økning i den ikke-polare delen av aldehydet, noe som gjør det mindre løselig i vann..
Men hvordan er de og hvor kommer de fra? Selv om dens natur i hovedsak avhenger av karbonylgruppen, bidrar resten av molekylstrukturen også mye til helheten. Dermed kan de være av hvilken som helst størrelse, liten eller stor, eller til og med et makromolekyl kan ha regioner der karakteren av aldehyder dominerer..
Således, som med alle kjemiske forbindelser, er det "hyggelige" aldehyder og andre bitre. De kan finnes i naturlige kilder eller syntetiseres i stor skala. Eksempler på aldehyder er vanillin, veldig til stede i iskrem (toppbilde) og acetaldehyd, som tilfører alkohol til alkoholholdige drikker..
Artikkelindeks
- 1 Kjemisk struktur
- 2 Fysiske og kjemiske egenskaper
- 2.1 Smeltepunkter
- 2.2 Kokepunkter
- 2.3 Løselighet i vann uttrykt i g / 100 g H2O
- 3 Reaktivitet
- 3.1 Oksidasjonsreaksjon
- 3.2 Reduksjon til alkohol
- 3.3 Reduksjon til hydrokarboner
- 3.4 Nukleofil tilsetning
- 4 Nomenklatur
- 5 bruksområder
- 5.1 Formaldehyd
- 5.2 Bakelitt
- 5.3 Kryssfiner
- 5.4 Polyuretan
- 5.5 Butyraldehyd
- 5.6 Acetaldehyd
- 5.7 Syntese
- 6 Eksempler på aldehyder
- 6.1 Glutaraldehyd
- 6.2 Benzaldehyd
- 6.3 Glyseraldehyd
- 6.4 Glyseraldehyd-3-fosfat
- 6.5 11-cis-Retinal
- 6.6 Pyridoxal fosfat (vitamin B6)
- 6.7 Salicylaldehyd
- 7 Referanser
Kjemisk struktur

Aldehyder består av karbonyl (C = O) som et hydrogenatom er direkte knyttet til. Dette skiller den fra andre organiske forbindelser som ketoner (RtoC = O) og karboksylsyrer (RCOOH).
Det øvre bildet viser molekylstrukturen rundt -CHO, en formylgruppe. Formylgruppen er flat fordi karbon og oksygen har SP-hybridiseringto. Denne planariteten gjør den utsatt for angrep av nukleofile arter, og derfor oksideres den lett..
Hva refererer denne oksidasjonen til? Til dannelsen av en binding med et hvilket som helst annet atom som er mer elektronegativt enn karbon; og når det gjelder aldehyder er det et oksygen. Dermed oksyderes aldehydet til en karboksylsyre, -COOH. Hva om aldehydet ble redusert? En primær alkohol ville bli dannet i stedet for, ROH.
Aldehyder produseres bare av primære alkoholer: de der OH-gruppen er i enden av en kjede. Tilsvarende formylgruppen for evig er på slutten av en kjede eller stikker ut fra den eller ringen som en substituent (hvis det er andre viktigere grupper, for eksempel -COOH).
Fysiske og kjemiske egenskaper
Siden de er polare forbindelser, er deres smeltepunkter høyere enn for ikke-polære forbindelser. Aldehydmolekyler er ikke i stand til intermolekylær binding gjennom hydrogenbindinger, da de bare har karbonatomer festet til hydrogenatomer..
På grunn av det ovennevnte har aldehyder lavere kokepunkter enn alkoholer og karboksylsyrer.
Smeltepunkter
Formaldehyd -92; Acetaldehyd -121; Propionaldehyd -81; n-butyraldehyd -99; n-Valeraldehyd -91; Kaproaldehyd -; Heptaldehyd - 42; Fenylacetaldehyd -; Benzaldehyd -26.
Kokepunkter
Formaldehyd -21; Acetaldehyd 20; Propionaldehyd 49; n-butyraldehyd 76; n-Valeraldehyd 103; Kaproaldehyd 131; Heptaldehyd 155; Fenylacetaldehyd 194; Benzaldehyd 178.
Løselighet i vann uttrykt i g / 100 g HtoELLER
Formaldehyd, veldig løselig; Uendelig acetaldehyd; Propionaldehyd, 16; n-butyraldehyd, 7; n-Valeraldehyd, lett løselig; kaproaldehyd, lett løselig; Svakt løselig fenylacetaldehyd; Benzaldehyd, 0,3.
Kokepunktene til aldehyder har en tendens til å øke direkte med molekylvekten. Tvert imot er det en tendens til å redusere løseligheten av aldehyder i vann når molekylvekten øker. Dette gjenspeiles i de fysiske konstantene til nettopp nevnte aldehyder..
Reaktivitet
Oksidasjonsreaksjon
Aldehyder kan oksyderes til den tilsvarende karboksylsyren i nærvær av noen av disse forbindelsene: Ag (NH3)to, KMnO4 greittoCrtoELLER7.
Reduksjon til alkohol
De kan hydrogeneres ved hjelp av nikkel-, platina- eller palladiumkatalysatorer. Dermed blir C = O C-OH.
Reduksjon til hydrokarboner
I nærvær av Zn (Hg), konsentrert HC1 eller i NHtoNHto aldehyder mister karbonylgruppen og blir hydrokarboner.
Nukleofil tilsetning
Det er flere forbindelser som tilsettes karbonylgruppen, blant dem er: Grignard-reagenser, cyanid, derivater av ammoniakk og alkoholer.
Nomenklatur
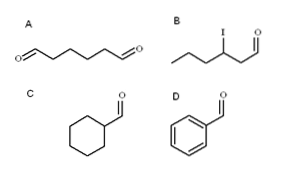
Fire aldehyder er illustrert i bildet ovenfor. Hvordan blir de navngitt?
Siden de er oksyderte primære alkoholer, endres navnet på alkoholen fra -ol til -al. Dermed ble metanol (CH3OH) hvis oksidert til CH3CHO kalles metanal (formaldehyd); CH3CHtoCHO etanol (acetaldehyd); CH3CHtoCHtoCHO propanal og CH3CHtoCHtoCHtoCHO butanal.
Alle de nylig navngitte aldehyder har -CHO-gruppen på slutten av kjeden. Når den er funnet i begge ender, som i A, blir slutt -al prepended med prefikset di-. Ettersom A har seks karbonatomer (teller de fra begge formylgrupper), stammer det fra 1-heksanol, og navnet er derfor: heksanslå.
Når det er en substituent, slik som en alkylgruppe, en dobbelt- eller trippelbinding, eller et halogen, er karbonene i hovedkjeden oppført og gir -CHO tallet 1. Dermed kalles aldehyd B: 3-jodheksanal.
Imidlertid har gruppen -CHO i aldehyder C og D ingen prioritet å identifisere slike forbindelser fra andre. C er en cykloalkan, mens D er en benzen, begge med en av deres Hs substituert med en formylgruppe.
I dem, da hovedstrukturen er syklisk, heter formylgruppen karbaldehyd. Dermed er C cykloheksankarbaldehyd, og D er benzenkarbaldehyd (bedre kjent som benzaldehyd).
applikasjoner
Aldehyder finnes i naturen som er i stand til å gi behagelige smaker, slik er det med kanelaldehyd, som er ansvarlig for den karakteristiske smaken av kanel. Det er derfor de ofte brukes som kunstige smaker i mange produkter som søtsaker eller mat..
Formaldehyd
Formaldehyd er det mest industrielt produserte aldehydet. Formaldehydet oppnådd ved oksidasjon av metanol brukes i en 37% løsning av gassen i vann, under navnet formalin. Dette brukes til garvning av huder og til bevaring og balsamering av lik..
På samme måte brukes formaldehyd som et bakteriedrepende middel, soppdrepende middel og insektmiddel for planter og grønnsaker. Imidlertid er dens største nytte bidrag til produksjonen av polymert materiale. Plasten kalt bakelitt syntetiseres ved reaksjonen mellom formaldehyd og fenol.
Bakelitt
Bakelitt er en svært hard polymer med en tredimensjonal struktur som brukes i mange husholdningsredskaper som håndtak for gryter, panner, kaffetraktere, kniver osv..
Bakelittlignende polymerer er laget av formaldehyd i kombinasjon med forbindelsene urea og melamin. Disse polymerene brukes ikke bare som plast, men også som lim og belegg..
Kryssfiner
Kryssfiner er det kommersielle navnet på et materiale dannet av tynne treplater, sammen med polymerer produsert av formaldehyd. Merkene Formica og Melmac er produsert med sistnevnte deltakelse. Formica er et plastmateriale som brukes i møbelbelegg.
Melmac plast brukes til å lage tallerkener, glass, kopper, etc. Formaldehyd er råmaterialet for syntesen av forbindelsen metylen-difenyl-diisocyanat (MDI), en forløper for polyuretan.
Polyuretan
Polyuretan brukes som isolator i kjøleskap og fryser, polstring av møbler, madrasser, belegg, lim, såler osv..
Butyraldehyd
Butyraldehyd er den viktigste forløperen for syntesen av 2-etylheksanol, som brukes som myknningsmiddel. Den har en behagelig eplearoma som tillater bruk i mat som smakstilsetning.
Den brukes også til produksjon av gummiakseleratorer. Går inn som et mellomreagens ved fremstilling av løsemidler.
Acetaldehyd
Acetaldehyd ble brukt i produksjonen av eddiksyre. Men denne rollen til acetaldehyd har avtatt i betydning, siden den har blitt fortrengt av karbonyleringsprosessen av metanol..
Syntese
Andre aldehyder er forløpere for oksoalkoholer, som brukes i produksjonen av vaskemidler. Såkalte oksoalkoholer fremstilles ved å tilsette karbonmonoksid og hydrogen til et olefin for å oppnå et aldehyd. Og til slutt hydreres aldehydet for å oppnå alkoholen.
Noen aldehyder brukes til fremstilling av parfymer, slik tilfellet er med Chanel nr. 5. Mange aldehyder av naturlig opprinnelse har behagelig lukt, for eksempel: heptanal har en grønn gresslukt; oktanalen en oransje lukt; nonanal en lukt av roser og citral en lukt av kalk.
Eksempler på aldehyder
Glutaraldehyd
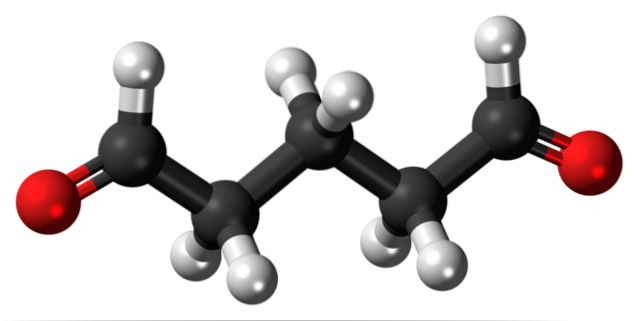
Glutaraldehyd har to formylgrupper i strukturen i begge ender.
Markedsført under navnet Cidex eller Glutaral, og brukes som et desinfeksjonsmiddel for å sterilisere kirurgiske instrumenter. Den brukes til å behandle vorter på føttene og bruke den som en væske. Det brukes også som et vevsfikserende middel i histologi- og patologilaboratorier..
Benzaldehyd
Det er det enkleste aromatiske aldehydet som dannes av en benzenring der en formylgruppe er bundet.
Den finnes i mandelolje, derav den karakteristiske lukten som gjør at den kan brukes som mataroma. I tillegg brukes den til syntesen av organiske forbindelser relatert til fremstilling av medisiner og til fremstilling av plast..
Glyseraldehyd
Det er en aldotriose, et sukker som består av tre karbonatomer. Den har to isomerer kalt D- og L-enantiomerer. Glyseraldehyd er det første monosakkaridet som oppnås i fotosyntese i den mørke fasen (Calvin-syklus)..
Glyseraldehyd-3-fosfat
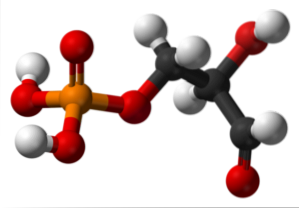
Det øvre bildet illustrerer strukturen til glyseraldehyd-3-fosfat. De røde kulene ved siden av den gule tilsvarer fosfatgruppen, mens de svarte karbonskjelettet. Den røde sfæren knyttet til den hvite er OH-gruppen, men når den er knyttet til den sorte sfæren og den sistnevnte til den hvite, er det CHO-gruppen.
Glyseraldehyd-3-fosfat er involvert i glykolyse, en metabolsk prosess der glukose nedbrytes til pyruvinsyre ved produksjon av ATP, et energireservoar av levende vesener. I tillegg til produksjonen av NADH, et biologisk reduksjonsmiddel.
I glykolyse stammer glyseraldehyd-3-fosfat og dihydroacetonfosfat fra spaltingen av D-fruktose-1-6-bisfosfat
Glyseraldehyd-3-fosfat er involvert i den metabolske prosessen kjent som pentosesyklusen. I den genereres NADPH, en viktig biologisk reduksjonsmiddel..
11-cis-Retinal
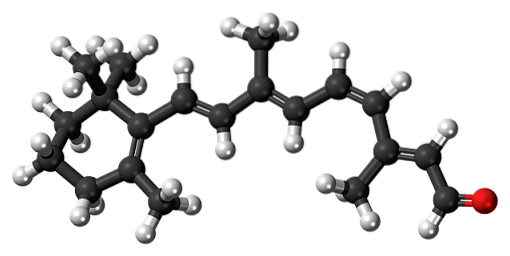
Β-karoten er et naturlig pigment som finnes i forskjellige grønnsaker, spesielt gulrøtter. Den gjennomgår en oksidativ nedbrytning i leveren, og omdannes dermed til retinolalkohol eller vitamin A. Oksidasjonen av vitamin A og den påfølgende isomeriseringen av en av dens dobbeltbindinger, danner 11-cis-retinal aldehyd.
Pyridoksalfosfat (vitamin B6)
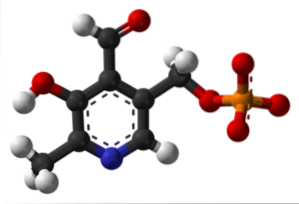
Det er en protesegruppe knyttet til flere enzymer, som er den aktive formen av vitamin B6 og deltar i synteseprosessen til den hemmende nevrotransmitteren GABA..
Hvor er formylgruppen i strukturen din? Merk at dette skiller seg fra resten av gruppene knyttet til den aromatiske ringen.
Salicylaldehyd
Det er et råmateriale for syntese av acetylsalisylsyre, et smertestillende og febernedsettende middel kjent som Aspirin..
Referanser
- Robert C. Neuman, Jr. kapittel 13, karbonylforbindelser: ketoner, aldehyder, karboksylsyrer. [PDF]. Hentet fra: chem.ucr.edu
- Germán Fernández. (14. september 2009). Nomenklatur for aldehyder. Hentet fra: quimicaorganica.net
- T.W. Graham Solomons, Craigh B. Fryhle. Organisk kjemi. (Tiende utgave, s 729-731) Wiley Plus.
- Jerry March og William H. Brown. (31. desember 2015). Aldehyde. Hentet fra: britannica.com
- Wikipedia. (2018). Aldehyder. Hentet fra: https://en.wikipedia.org/wiki/Aldehyde
- Morrison, R. T. og Boyd, R. N. (1990). Organic Chemistry Fifth Edition. Redaksjonell Addison-Wesley Iberoamericana.
- Carey, F. A. (2006). Organic Chemistry Sixth Edition. Mc Graw Hill Publishing House.
- Mathews, Ch. K., Van Holde, K. E. og Athern, K. G. (2002). Biokjemi. Tredje utgave. Utgiver Pearson Adisson Wesley.



Ingen har kommentert denne artikkelen ennå.