
Benzylbenzylhydrogener, karbokasjoner, benzylradikaler
De benzyl eller benzyl er en vanlig substituentgruppe i organisk kjemi hvis formel er C6H5CHto- eller Bn-. Strukturelt består den ganske enkelt av foreningen av en metylengruppe, CHto, med en fenylgruppe, C6H5; det vil si en karbon sp3 direkte bundet til en benzenring.
Derfor kan benzylgruppen sees på som en aromatisk ring festet til en liten kjede. I noen tekster foretrekkes bruk av forkortelsen Bn i stedet for C6H5CHto-, lett gjenkjennes i en hvilken som helst forbindelse; spesielt når det er festet til et oksygen- eller nitrogenatom, O-Bn eller NBnto, henholdsvis.

Denne gruppen finnes også implisitt i en rekke allment kjente forbindelser. For eksempel til benzoesyre, C6H5COOH, kan betraktes som en benzyl hvis karbon sp3 den har gjennomgått omfattende oksidasjon; eller benzaldehyd, C6H5CHO, fra en delvis oksidasjon; og benzylalkohol, C6H5CHtoOH, enda mindre rusten.
Et annet noe åpenbart eksempel på denne gruppen finnes i toluen, C6H5CH3, som kan gjennomgå et visst antall reaksjoner som et resultat av den uvanlige stabiliteten som følge av benzylradikaler eller karbokasjoner. Imidlertid tjener benzylgruppen til å beskytte OH- eller NH-gruppene.to av reaksjoner som uønsket endrer produktet som skal syntetiseres.
Artikkelindeks
- 1 Eksempler på forbindelser med benzylgruppe
- 2 benzylhydrogener
- 3 Karbokasjoner og benzylradikaler
- 3.1 Resonans i benzylgruppen
- 3.2 Andre radikaler
- 4 Reaksjoner
- 5 Referanser
Eksempler på forbindelser med benzylgruppe
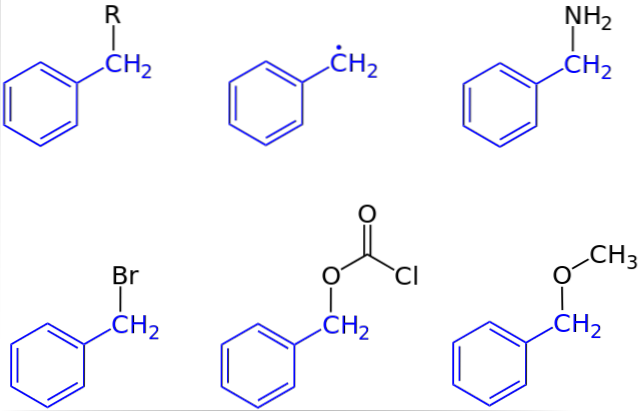
På det første bildet ble den generelle representasjonen av en forbindelse med en benzylgruppe vist: C6H5CHto-R, hvor R kan være et hvilket som helst annet molekylært fragment eller atom. Ved å variere R kan det således oppnås et høyt antall eksempler; noen enkle, andre bare for en bestemt region av en større struktur eller et sett.
Benzylalkohol er for eksempel avledet fra å erstatte OH med R: C6H5CHto-ÅH. Hvis det er NH-gruppen i stedet for OHto, deretter oppstår benzylaminforbindelsen: C6H5CHto-NHto.
Hvis Br er atomet som erstatter R, er den resulterende forbindelsen benzylbromid: C6H5CHto-Br; R for COtoCl gir opphav til en ester, benzylklorkarbonat (eller karbobensoksylklorid); og OCH3 gir opphav til benzylmetyleter, C6H5CHto-OCH3.
Selv (men ikke helt riktig), kan R antas av et enslig elektron: benzylradikalen, C6H5CHto·, Produkt av frigjøringen av den radikale R ·. Et annet eksempel, selv om det ikke er inkludert i bildet, er fenylacetonitril eller benzylcyanid, C6H5CHto-CN.
Det er forbindelser der benzylgruppen neppe representerer en spesifikk region. Når dette er tilfelle, brukes ofte forkortelsen Bn for å forenkle strukturen og illustrasjonene..
Benzylhydrogener
Ovennevnte forbindelser har til felles ikke bare den aromatiske eller fenylringen, men også benzyliske hydrogener; dette er de som tilhører sp carbon3.
Slike hydrogener kan representeres som: Bn-CH3, Bn-CHtoR eller Bn-CHRto. Bn-CR-forbindelsen3 mangler benzylhydrogen, og derfor er reaktiviteten mindre enn for de andre.
Disse hydrogenene er forskjellige fra de som vanligvis er festet til et sp karbon3.
Tenk for eksempel på metan, CH4, som også kan skrives som CH3-H. For at CH-bindingen skal brytes3-H i en heterolytisk sammenbrudd (radikal dannelse), må det tilføres en viss mengde energi (104kJ / mol).
Imidlertid går energien for den samme C-bindingen6H5CHto-H er lavere sammenlignet med metan (85 kJ / mol). Siden denne energien er mindre, innebærer det at den radikale C6H5CHtoDet er mer stabilt enn CH3·. Det samme skjer i større eller mindre grad med andre benzyliske hydrogener.
Følgelig er benzyliske hydrogener mer reaktive når de genererer mer stabile radikaler eller karbokasjoner enn de som er forårsaket av andre hydrogener. Hvorfor? Spørsmålet blir besvart i neste avsnitt.
Karbokasjoner og benzylradikaler
Den radikale C var allerede vurdert6H5CHto·, Mangler benzylkarboksjonen: C6H5CHto+. I det første er det et enslig, uparret elektron, og i det andre en elektronisk mangel. De to artene er veldig reaktive og representerer forbigående forbindelser som sluttproduktene fra reaksjonen stammer fra..
Carbon sp3, etter å ha mistet en eller to elektroner for å danne henholdsvis radikal eller karbokasjon, kan den vedta sp-hybridiseringto (trigonalplan), på en slik måte at det er minst mulig frastøting mellom dets elektroniske grupper. Men hvis det tilfeldigvis er spto, I likhet med de aromatiske ringkarbonene, kan bøyning forekomme? Svaret er ja.
Resonans i benzylgruppen
Denne konjugasjonen eller resonansen er nøkkelfaktoren for å forklare stabiliteten til disse benzyl- eller benzyl-avledede artene. Følgende bilde illustrerer et slikt fenomen:
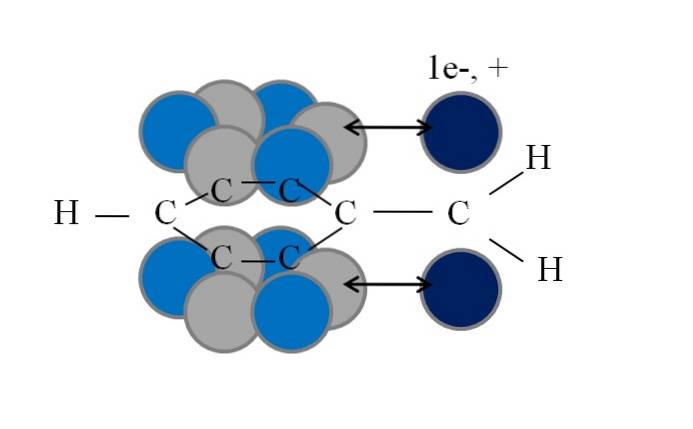
Legg merke til at der et av de benzyliske hydrogenene var, forble en bane s med et uparret elektron (radikal, 1e-), eller ugyldig (karbocation, +). Som det kan sees, denne orbitalen s er parallelt med det aromatiske systemet (de grå og lyseblå sirkler), med den doble pilen som indikerer begynnelsen på bøyningen.
Dermed kan både det uparrede elektronet og den positive ladningen overføres eller spres gjennom den aromatiske ringen, siden parallelliteten til deres orbitaler favoriserer det geometrisk. Disse ligger imidlertid ikke i noen bane s aromatisk ring; bare i de som tilhører karbonene i orto- og paraposisjoner med hensyn til CHto.
Det er grunnen til at de lyseblå sirklene skiller seg ut over de grå: i dem er den negative eller positive tettheten av henholdsvis radikal eller karbokonsentrasjon konsentrert..
Andre radikaler
Det bør nevnes at denne konjugasjonen eller resonansen ikke kan forekomme i sp-karbonatomer3 mest fjernt fra den aromatiske ringen.
For eksempel den radikale C6H5CHtoCHtoDet er mye mer ustabilt fordi det uparrede elektronet ikke kan konjugere med ringen når CH-gruppen griper innto i mellom og med sp hybridisering3. Det samme gjelder C6H5CHtoCHto+.
Reaksjoner
Oppsummert: benzyliske hydrogener er tilbøyelige til å reagere, enten genererer en radikal eller en karbokasjon, som igjen ender med å forårsake sluttproduktet av reaksjonen. Derfor reagerer de via en SN-mekanisme.1.
Et eksempel er bromering av toluen under ultrafiolett stråling:
C6H5CH3 + 1 / 2Brto => C6H5CHtoBr
C6H5CHtoBr + 1/2 Brto => C6H5CHBrto
C6H5CHBrto + 1 / 2Brto => C6H5CBr3
Faktisk produseres Br-radikaler i denne reaksjonen..
På den annen side reagerer benzylgruppen selv for å beskytte OH- eller NH-gruppene.to i en enkel substitusjonsreaksjon. Dermed kan en ROH-alkohol 'benzyleres' ved bruk av benzylbromid og andre reagenser (KOH eller NaH):
ROH + BnBr => ROBn + HBr
ROBn er en benzyleter, som den opprinnelige OH-gruppen kan returneres til hvis den blir utsatt for et reduktivt medium. Denne eteren skal forbli uendret mens andre reaksjoner utføres på forbindelsen..
Referanser
- Morrison, R.T. og Boyd, R. N. (1987). Organisk kjemi. (5. utgave). Addison-Wesley Iberoamericana.
- Carey, F. A. (2008). Organisk kjemi. (6. utgave). McGraw-Hill, Interamerica, Editores S.A.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. Amines. (10. utgave.). Wiley pluss.
- Wikipedia. (2019). Benzyl-gruppen. Gjenopprettet fra: en.wikipedia.org
- Dr. Donald L. Robertson. (5. desember 2010). Fenyl eller benzyl? Gjenopprettet fra: home.miracosta.edu
- Gamini Gunawardena. (2015, 12. oktober). Benzylic Carbocation. Kjemi LibreTexts. Gjenopprettet fra: chem.libretexts.org



Ingen har kommentert denne artikkelen ennå.