
Hypobrome syreegenskaper, struktur, bruksområder

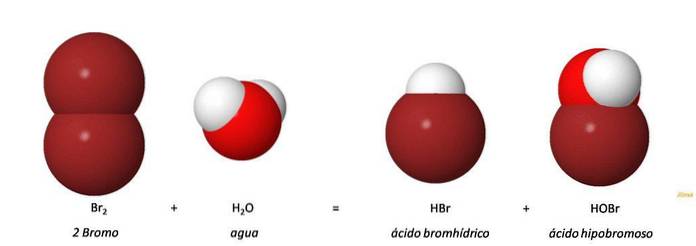
De hypobromøs syre (HOBr, HBrO) er en uorganisk syre produsert ved oksidasjon av bromidanionet (Br-). Tilsetningen av brom til vann gir hydrobromsyre (HBr) og hypobromøs syre (HOBr) gjennom en disproporsjoneringsreaksjon. Br2 + H2O = HOBr + HBr
Hypobromsyre er en veldig svak syre, noe ustabil, som eksisterer som en fortynnet løsning ved romtemperatur. Den produseres i varmblodige virveldyrorganismer (inkludert mennesker) ved virkningen av enzymet eosinophil peroxidase.
Oppdagelsen av at hypobromøs syre kan regulere kollagen IV-aktivitet har vakt stor oppmerksomhet..
Artikkelindeks
- 1 Struktur
- 1.1 2D
- 1.2 3D
- 2 Fysiske og kjemiske egenskaper
- 3 bruksområder
- 4 Biomolekylære interaksjoner
- 5 Referanser
Struktur
2D
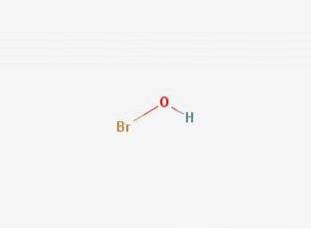
3D

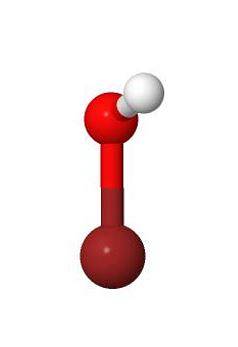
Fysiske og kjemiske egenskaper
- Utseende gule faste stoffer: gule faste stoffer.
- Utseende: gule faste stoffer.
- Molekylvekt: 96,911 g / mol.
- Kokepunkt: 20-25 ° C.
- Tetthet: 2,470 g / cm3.
- Surhet (pKa): 8,65.
- De kjemiske og fysiske egenskapene til hypobromøs syre er lik de andre hypohalittene..
- Den kommer som en fortynnet løsning ved romtemperatur.
- Hypobromitt faste stoffer er gule i fargen og har en spesiell aromatisk lukt.
- Det er et sterkt bakteriedrepende og vanndesinfiserende middel.
- Den har en pKa på 8,65 og dissosieres delvis i vann ved pH 7.
applikasjoner
- Hypobromous acid (HOBr) brukes som blekemiddel, oksidant, deodorant og desinfiserende middel, på grunn av dets evne til å drepe cellene til mange patogener.
- Den brukes av tekstilindustrien som blekemiddel og tørkemiddel.
- Brukes også i boblebad og spa som et bakteriedrepende middel.
Biomolekylære interaksjoner
Brom er allestedsnærværende hos dyr som ionisk bromid (Br-), men inntil nylig var dets essensielle funksjon ukjent..
Nyere forskning har vist at brom er viktig for kjellermembranarkitektur og vevsutvikling.
Enzymet peroksidain bruker HOBr for å tverrbinde sulfilimin, som er tverrbundet i kollagen IV-stillasene i kjellermembranen..
Hypobromøs syre produseres i varmblodige virveldyrorganismer ved virkningen av enzymet eosinophil peroxidase (EPO).
EPO genererer HOBr fra H2O2 og Br- i nærvær av en plasmakonsentrasjon av Cl-.
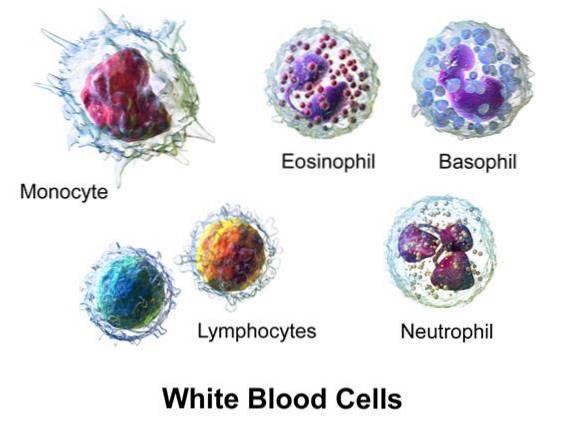
Myeloperoksidase (MPO), fra monocytter og nøytrofiler, genererer hypoklorsyre (HOCl) fra H2O2 og Cl-.
EPO og MPO spiller en viktig rolle i vertsforsvarsmekanismer mot patogener ved bruk av henholdsvis HOBr og HOCl.
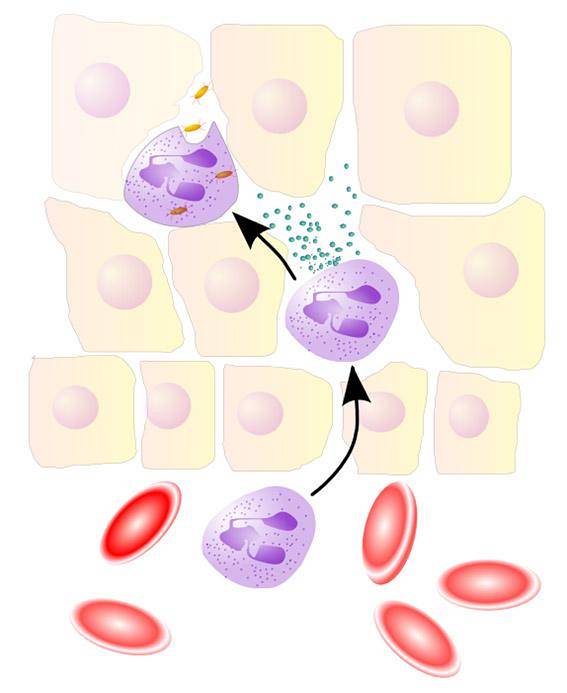
MPO / H2O2 / Cl-systemet i nærvær av Br- genererer også HOBr ved å reagere den dannede HOCl med Br-. Mer enn en kraftig oksidant, HOBr er en kraftig elektrofil.
Plasmakonsentrasjonen av Br- er mer enn 1000 ganger lavere enn kloridanionen (Cl-). Følgelig er endogen produksjon av HOBr også lavere sammenlignet med HOCl.
HOBr er imidlertid betydelig mer reaktiv enn HOCl når oksiderbarheten til forbindelsene som er studert ikke er relevant, så reaktiviteten til HOBr kan være mer assosiert med dens elektrofile styrke enn med sin oksidasjonsevne (Ximenes, Morgon & de Souza, 2015).
Selv om redokspotensialet er lavere enn HOCl, reagerer HOBr med aminosyrer raskere enn HOCl.
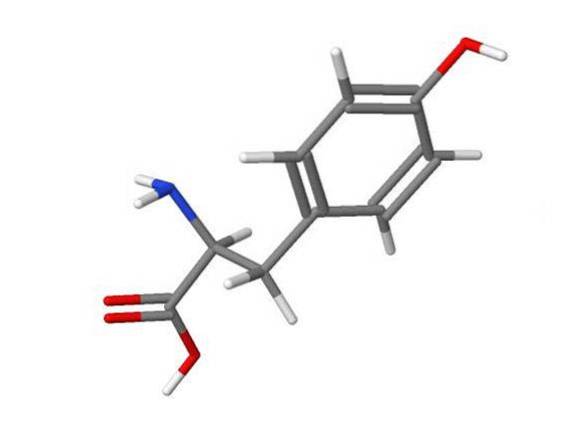
Halogeneringen av tyrosinringen med HOBr er 5000 ganger raskere enn den for HOCl.
HOBr reagerer også med nukleosidnukleobaser og DNA.
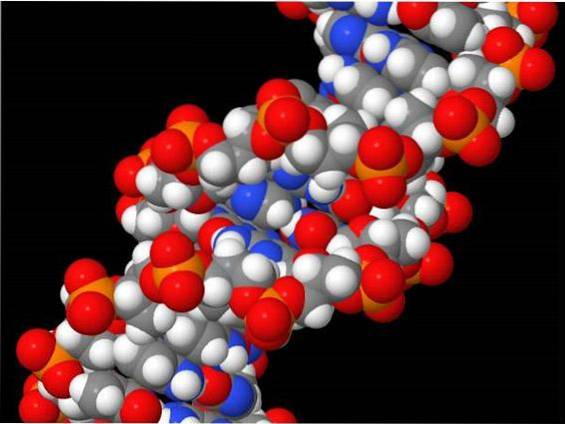
2'-deoksycytidin, adenin og guanin, genererer 5-brom-2'-deoksycytidin, 8-bromadenin og 8-bromoguanin i EPO / H2O2 / Br- og MPO / H2O2 / Cl- / Br- systemer (Suzuki, Kitabatake og Koide , 2016).
McCall, et al. (2014) har vist at Br er en nødvendig kofaktor for dannelsen av sulfilimin-tverrbindinger katalysert av enzymet peroxidasine, en posttranslasjonell modifikasjon som er viktig for arkitekturen av kollagen IV i kjellermembranene og utvikling av vev..
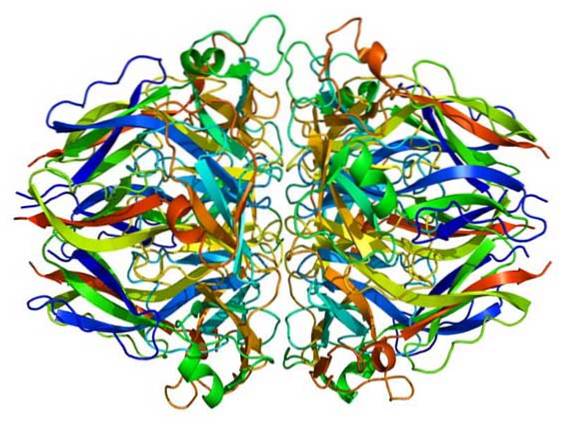
Kjellermembraner er spesialiserte ekstracellulære matriser som er viktige formidlere av signaltransduksjon og mekanisk støtte av epitelceller..
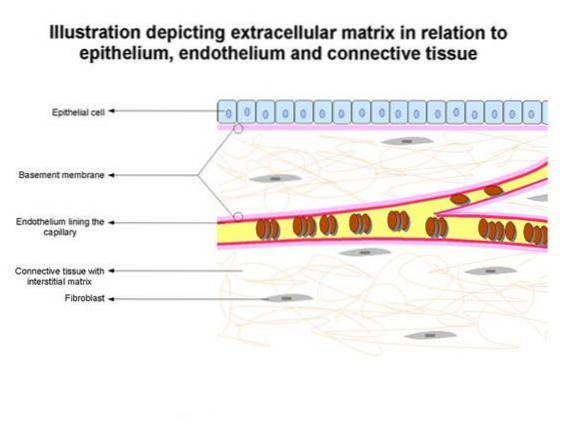
Basalmembraner definerer arkitekturen til epitelvev og letter vevsreparasjon etter skade, blant andre funksjoner..
Innebygd i kjellermembranen er et kollagen IV stillas tverrbundet med sulfilimin, som gir matrisefunksjonaliteten i flercellede vev hos alle dyr..
Kollagen IV stillas gir mekanisk styrke, fungerer som en ligand for integriner og andre celleoverflate reseptorer, og samhandler med vekstfaktorer for å etablere signalgradienter..
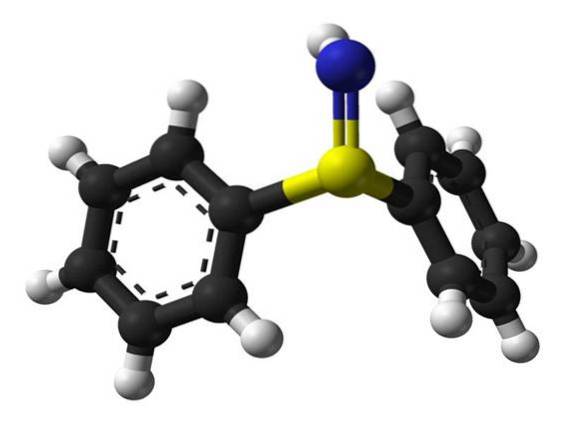
Sulfilimin (sulfimid) er en kjemisk forbindelse som inneholder en svovel til nitrogen dobbeltbinding. Sulfiliminbindinger stabiliserer kollagen IV-tråder som finnes i den ekstracellulære matrisen.
Disse bindingene kobler kovalent metionin 93 (Met93) og hydroksylysin 211 (Hyl211) rester av tilstøtende polypeptidstrenger for å danne en større kollagen-trimer..
Peroksidain danner hypobromøs syre (HOBr) og hypoklorsyre (HOCl) fra henholdsvis bromid og klorid, som kan formidle dannelsen av sulfilimin-tverrbindinger..
Bromidet, omdannet til hypobrom syre, danner et mellomprodukt av bromsulfoniumionen (S-Br) som deltar i dannelsen av tverrbindinger.
McCall, et al. (2014) demonstrerte at Br-mangel i kosten er dødelig i Drosophila-flua, mens Br-erstatning gjenoppretter levedyktigheten.
De konstaterte også at brom er et essensielt sporelement for alle dyr på grunn av dets rolle i dannelsen av sulfiliminbindinger og kollagen IV, noe som er av avgjørende betydning for dannelsen av kjellermembraner og utviklingen av vev..
Referanser
- ChemIDplus, (2017). 3D-struktur av 13517-11-8 - Hypobromøs syre [bilde] Hentet fra nih.gov.
- ChemIDplus, (2017). 3D-struktur på 60-18-4 - Tyrosin [USAN: INN] [bilde] Hentet fra nih.gov.
- ChemIDplus, (2017). 3D-struktur av 7726-95-6 - Brom [bilde] Hentet fra nih.gov.
- ChemIDplus, (2017). 3D-struktur av 7732-18-5 - Vann [bilde] Gjenopprettet fra nih.gov.
- Emw, (2009). Protein COL4A1 PDB 1li1 [image] Gjenopprettet fra wikipedia.org.
- Mills, B. (2009). Difenylsulfimid-fra-xtal-2002-3D-baller [bilde] Gjenopprettet fra wikipedia.org.
- PubChem, (2016). Hypobromøs syre [bilde] Hentet fra nih.gov.
- Steane, R. (2014). DNA-molekylet - roterbart i 3 dimensjoner [bilde] Gjenopprettet fra biotopics.co.uk
- Thormann, U. (2005). NeutrophilerAktion [image] Gjenopprettet fra wikipedia.org.



Ingen har kommentert denne artikkelen ennå.