
Klordioksid (ClO2) struktur, bruk, oppnåelse, risiko, egenskaper

De klordioksid Det er en uorganisk forbindelse dannet av elementet klor (Cl) og oksygen (O). Den kjemiske formelen er ClOto. Det er en grønn-gul til rødlig gass. Det finnes ikke naturlig i miljøet.
Det er ekstremt reaktivt, så det er vanlig at det tilberedes der det skal brukes. En av de viktigste bruksområdene er som et mikrobicid, antiseptisk middel og deodoriserende middel fordi det eliminerer bakterier, virus og sopp veldig enkelt og i svært lave konsentrasjoner..

Lar deg desinfisere matvarer som grønnsaker, frukt, kjøtt, fjærfe og sjømat. Den brukes til å rense overflater, gulv, bad, ventilasjonsanlegg, svømmebassenger, laboratorieutstyr, tannutstyr, etc..
Av den grunn brukes den i matforedling, på sykehus og klinikker, i bransjer og butikker. Det brukes til å rense drikkevann og kommunalt avløpsvann.
Det er veldig effektivt som et oksidasjonsmiddel, og det er derfor det brukes til å bleke papirmasse, oljer, mel, lær, tekstilfibre, blant andre..
Når det er i form av en gass, er det veldig farlig, siden det er svært eksplosivt, og brukes hovedsakelig i vandige løsninger. Det er giftig ved innånding.
Artikkelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Kokepunkt
- 3,5 Tetthet
- 3.6 Løselighet
- 3.7 Kjemiske egenskaper
- 3.8 Egenskaper for dets vandige løsninger
- 3.9 Andre egenskaper
- 4 Motta
- 5 Brukes som desinfeksjonsmiddel
- 5.1 I mat
- 5.2 På papir og papp som kommer i kontakt med mat
- 5.3 I drikkevann
- 5.4 I tannlegen
- 5.5 I medisinske applikasjoner
- 6 Andre bruksområder
- 7 Risiko
- 8 Referanser
Struktur
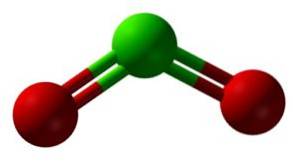
Klordioksid dannes ved foreningen av et kloratom (Cl) med to oksygenatomer (O). Bindinger av klor med hvert oksygen er kovalente og doble. Klor i denne forbindelsen har en valens på +4.
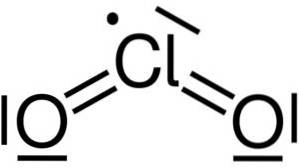
Den har en symmetrisk og vinklet struktur, siden den har frie elektroner. Det vil si at de ikke danner et bånd med noe annet atom.
Nomenklatur
- Klordioksid
- Kloroksid (iv)
Eiendommer
Fysisk tilstand
Grønn-gul til rød-gul gass.
Molekylær vekt
67,45 g / mol.
Smeltepunkt
-59 ºC.
Kokepunkt
11 ºC.
Tetthet
Væske ved 0 ° C = 1642 g / cm33
Gass = 2,33 (relativ tetthet til luft, luft = 1).
Løselighet
Løselig i vann: 2000 cm3 av ClOto gass i 100 cm3 kaldt vann eller 0,8 g / 100 ml vann ved 20 ° C. Løselig i alkalisk løsning og i svovelsyreoppløsning HtoSW4.
Kjemiske egenskaper
ClOto det er ekstremt reaktivt og kan eksplodere voldsomt. Det er et veldig effektivt oksidasjonsmiddel.
ClOto den nedbrytes voldsomt hvis den kommer i kontakt med organiske materialer. Hvis det er i luft i en konsentrasjon som er større enn 10%, kan den eksplodere på grunn av sollys eller varme.
Det kan også detonere i nærvær av kvikksølv (Hg) eller karbonmonoksid (CO).
Under påvirkning av ultrafiolett (UV) lys eller ozon, ClOto blir klorheksoksyd CltoELLER6, veldig ustabil forbindelse.
Egenskapene til de vandige løsningene dine
De vandige løsningene er gule eller rødgule. De er stabile hvis de holdes kjølig, godt forseglet og beskyttet mot sollys. I nærvær av lys nedbrytes disse løsningene sakte for å gi saltsyre-HCl og klorsyre-HClO.3.

I alkaliske løsninger, ClOto nedbrytes til klorioner ClOto- og klorat ClO3-. Klorsyre HClO dannes i syreoppløsningerto og deretter spaltes dette til saltsyre HC1 og klorsyre HC13.
Andre egenskaper
De konsentrerte damper av ClOto de er potensielt eksplosive, så det har ikke vært mulig å komprimere den alene eller blandet med andre gasser. Av denne grunn er det foretrukket å tilberede det på nettstedet der det skal brukes..
Når det er ved veldig lave temperaturer i hydrert form, som det er måten det noen ganger overføres, er det et blokkformet fast stoff som ligner på is og oransje..
Den har en lukt som ligner på klor. Det er giftig ved innånding.
Å skaffe
Det kan fås på flere måter. For eksempel i noen tilfeller ClO-løsningerto fremstilles ved å føre en blanding av klorgass (Clto) og luft (eller klorgass og nitrogen Nto) gjennom en kolonne som inneholder natriumklorittgranuler (NaClOto).
2 NaClOto + Clto → 2 NaCl + 2ClOto
Det genererte produktet inneholder omtrent 90% ClOto, blant andre klorforbindelser.
Det er også hentet fra kaliumklorat (KClO3) og svovelsyre (HtoSW4) i nærvær av oksalsyre som et reduksjonsmiddel. I dette tilfellet er karbondioksid (COto) brukes til å fortynne ClOto.
Den kan tilberedes på bruksstedet med utgangspunkt i natriumklorat (NaClO3), svovelsyre (HtoSW4) og metanol (CH3ÅH).
I industrien oppnås det med natriumklorat (NaClO3) og svoveldioksid (SOto) i nærvær av svovelsyre.
2 NaClO3 + SWto + HtoSW4 → 2 ClOto + 2 NaHSO4
Brukes som desinfeksjonsmiddel
Det kan brukes som et kraftig antimikrobielt middel. Det har vist seg å være svært effektivt mot forskjellige mikroorganismer, slik som Escherichia coli og Staphylococcus aureus.
Med sistnevnte er en konsentrasjon på bare 5 ppm ClO tilstrekkeligto for å eliminere 100% av dem. Det er bakteriedrepende, antiseptisk og deodoriserende. Det er effektivt over et bredt pH-område.
I mat
Det brukes som et antimikrobielt middel i vann for å fumigere frukt og grønnsaker, i prosessering av fjærfe, rødt kjøtt, både stykker kjøtt og organer, og marine produkter som skalldyr..

Klordioksydløsninger bør brukes i en konsentrasjon som ikke overstiger 3 ppm (deler per million) ClOto resterende, slik at det ikke påvirker maten.
Etter behandling med ClOto all mat må skylles grundig med drikkevann, eller være beregnet på blanchering, matlaging eller hermetisering.
Når det gjelder marine produkter, ClO-løsningento Den skal brukes i vann og is som brukes til skylling, vasking, tining, transport eller oppbevaring. Rå skalldyr skal vaskes grundig med drikkevann før forbruk..

På papir og papp som kommer i kontakt med mat
ClO-løsningerto brukes til å eliminere slimdannende mikroorganismer (som alger, bakterier og sopp) i prosessvannet som brukes til fremstilling av papir og papp som kommer i kontakt med mat.
I drikkevann
Det brukes til å rense vann og gjøre det drikkbart (trygt å drikke). Det brukes i forbehandlingen av vann som senere blir tappet på flaske for drikke eller vann som vil bli brukt som en ingrediens ved fremstilling av drikkevarer eller brus..

I tannlegen
Det brukes i instrumentene som brukes av tannlegen eller tannlegen for å desinfisere dem og ødelegge patogene organismer i dem.
I medisinske applikasjoner
Vandige løsninger av ClOto har blitt brukt til å behandle orale gjærinfeksjoner (infeksjon i munnen). Candidiasis er en infeksjon forårsaket av soppen Candida albicans.
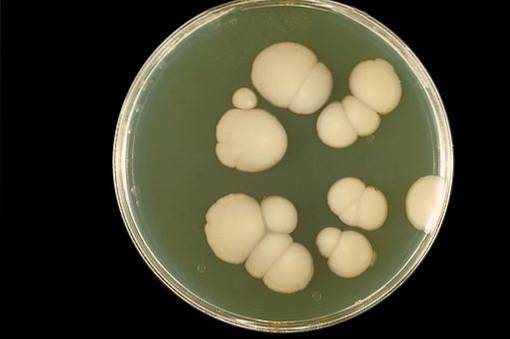
Klordioksid dreper munnsopp og forbedrer utseendet på oralt vev betydelig uten bivirkninger.
Noen medisinske forskere indikerer at ClO-løsningerto påført sår fra kirurgiske inngrep kan redusere eller undertrykke dannelse av vedheft uten å påvirke legingen, med den ekstra fordelen av dens antiseptiske egenskaper.
Andre bruksområder
På grunn av dets oksiderende og mikrobicidiske egenskaper, ClOto brukes til:
- Blek masse fra tre i papir- og papirindustrien, og gir en stabil glans.
- Bleking av fett og oljer, lær, bleking av mel og tekstiler.
- Landbruksapplikasjoner som desinfisering av harde overflater, utstyr, vannsystemer og soppdrivhus.
- Bruksområder i bransjer, butikker og sykehus som desinfisering av harde overflater (vegger, gulv, bad), ventilasjonssystemer, laboratorieutstyr.
- Desinfiser gulv og bad i boliger, klimaanlegg, vann i sirkulasjon.
- Kommunal og industriell avløpsrensing.
- Opprensing av oljefeltforurensning.
- Produksjon av kloridsalter (Cl-).
Risiko
- De konsentrerte damper av ClOto er potensielt eksplosive.
- Det er giftig ved innånding og svelging. Det irriterer øynene, nesen og halsen, kan forårsake lungeødem og kronisk bronkitt.
- I følge kildene som ble konsultert, var ClOto forårsaker ikke DNA-mutasjoner eller forårsaker kreft hos mennesker.
Referanser
- OSS. National Library of Medicine. (2019). Klordioksid. Gjenopprettet fra pubchem.ncbi.nlm.nih.gov.
- Dean, J.A. (redaktør). (1973). Lange's Handbook of Chemistry (Ellevte utgave). McGraw-Hill Book Company.
- Ullmann's Encyclopedia of Industrial Chemistry. (1990). Femte utgave. VCH Verlagsgesellschaft mbH.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Bajpai, P. (2012). Klordioksidbleking. Effekt av klordioksidbleking på massekvalitet. In Environmentalally Benign Approaches for Pulp Bleaching (Second Edition). Gjenopprettet fra sciencedirect.com.
- Moran, S. (2018). Vannkjemi. Klordioksid. I en anvendt guide til design av vann og avløpsrenseanlegg. Gjenopprettet fra sciencedirect.com.
- McKeen, L. (2012). Introduksjon til matbestråling og medisinsk sterilisering. Gassformet klordioksid. In The Effect of Sterilization on Plastics and Elastomers (Tredje utgave). Gjenopprettet fra sciencedirect.com.



Ingen har kommentert denne artikkelen ennå.