
Nitrogenfiksering biotiske og abiotiske prosesser

De Fiksering av nitrogen Det er settet med biologiske og ikke-biologiske prosesser som produserer kjemiske former for nitrogen tilgjengelig for levende vesener. Nitrogentilgjengelighet styrer på en viktig måte funksjonen til økosystemer og global biogeokjemi, siden nitrogen er en faktor som begrenser nettoprimærproduktiviteten i terrestriske og akvatiske økosystemer..
I vevet til levende organismer er nitrogen en del av aminosyrer, enheter av strukturelle og funksjonelle proteiner som enzymer. Det er også et viktig kjemisk element i sammensetningen av nukleinsyrer og klorofyll..
I tillegg forekommer de biogeokjemiske reaksjonene av karbonreduksjon (fotosyntese) og karbonoksidasjon (respirasjon) gjennom formidling av nitrogenholdige enzymer, siden de er proteiner.
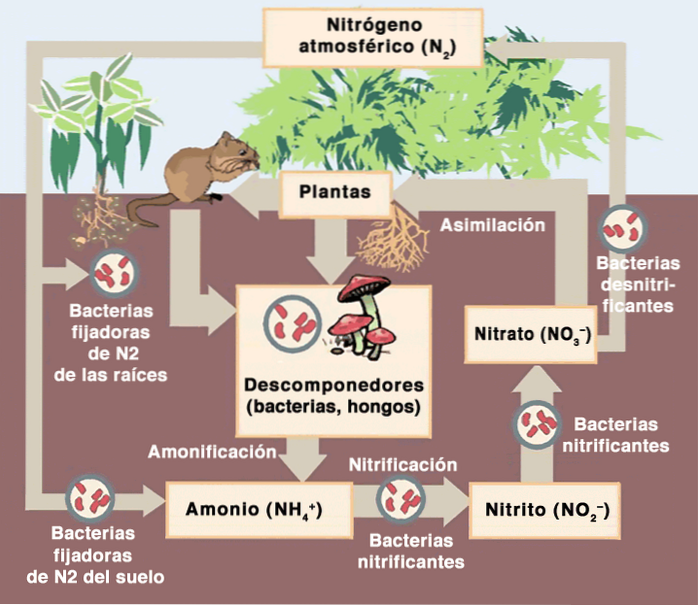
I de kjemiske reaksjonene av den biogeokjemiske syklusen av nitrogen endrer dette elementet oksidasjonstilstandene fra null til Nto, en 3- i NH3, 3+ i NOto - og NH4+ , og 5+ i NO3 -.
Flere mikroorganismer utnytter energien som genereres i disse nitrogenoksidreduksjonsreaksjonene og bruker den i sine metabolske prosesser. Det er disse mikrobielle reaksjonene som samlet driver den globale nitrogensyklusen..
Den mest utbredte kjemiske formen for nitrogen på planeten er gassformet molekylært diatomisk nitrogen Nto, som utgjør 79% av jordens atmosfære.
Det er også den minst reaktive kjemiske typen av nitrogen, praktisk talt inert, veldig stabil, på grunn av trippelbindingen som forbinder begge atomene. Av denne grunn er nitrogenet så rikelig i atmosfæren ikke tilgjengelig for de aller fleste levende vesener..
Nitrogen i kjemiske former tilgjengelig for levende vesener oppnås gjennom "nitrogenfiksering." Nitrogenfiksering kan skje på to hovedveier: abiotiske former for fiksering og biotiske former for fiksering..
Artikkelindeks
- 1 Abiotiske former for nitrogenfiksering
- 1.1 Elektriske stormer
- 1.2 Brenner fossilt brensel
- 1.3 Biomasseforbrenning
- 1.4 Nitrogenutslipp fra jorderosjon og bergforvitring
- 2 Biotiske former for nitrogenfiksering
- 2.1 Frilevende eller symbiotiske mikroorganismer
- 2.2 Mekanismer for å holde nitrogenasesystemet aktivt
- 2.3 Biotisk nitrogenfiksering av frilevende mikroorganismer
- 2.4 Energi som kreves under N2-fikseringsreaksjonen
- 2.5 Enzymet nitrogenasekompleks og oksygen
- 2.6 Biotisk nitrogenfiksering av mikroorganismer i symbiotisk liv med planter
- 3 Referanser
Abiotiske former for nitrogenfiksering
Elektriske stormer

Lynet eller "lynet" som produseres under tordenvær er ikke bare støy og lys; de er en kraftig kjemisk reaktor. På grunn av lynets virkning produseres nitrogenoksider NO og NO under storm.to, generisk kalt NEIx.
Disse elektriske utladningene, observert som lyn, genererer forhold med høye temperaturer (30.000ellerC) og høyt trykk, som fremmer den kjemiske kombinasjonen av oksygen Oto og nitrogen Nto fra atmosfæren, og produserer nitrogenoksider NOx.
Denne mekanismen har en svært lav andel av bidrag til den totale hastigheten av nitrogenfiksering, men den er den viktigste blant abiotiske former..
Brenner fossilt brensel
Det er et menneskeskapt bidrag til produksjonen av nitrogenoksider. Vi har allerede sagt at den sterke trippelbinding av nitrogenmolekylet Nto, kan bare bryte under ekstreme forhold.
Forbrenningen av fossile brensler avledet fra petroleum (i næringer og i kommersiell og privat transport, sjø, luft og land) gir enorme mengder NO-utslipp.x til atmosfæren.
DerettertoEller slippes ut ved forbrenning av fossile brensler, det er en kraftig klimagass som bidrar til global oppvarming av planeten..
Biomasseforbrenning
Det er også et bidrag av nitrogenoksider NOx ved å brenne biomasse i området med høyeste temperatur i flammen, for eksempel i skogbranner, bruk av ved til oppvarming og matlaging, forbrenning av organisk avfall og enhver bruk av biomasse som kilde til varmeenergi.
Nitrogenoksider NOx som slippes ut i atmosfæren av menneskeskapte veier, forårsaker alvorlige miljøforurensningsproblemer, for eksempel fotokjemisk smog i urbane og industrielle miljøer, og viktige bidrag til surt regn.
Nitrogenutslipp fra jorderosjon og bergforvitring
Jorderosjon og nitrogenrik bergforvitring utsetter mineraler for elementene som kan frigjøre nitrogenoksider. Bergforvitring oppstår på grunn av eksponering for miljøfaktorer, forårsaket av fysiske og kjemiske mekanismer som virker sammen..
Tektoniske bevegelser kan fysisk utsette nitrogenrike bergarter for elementene. Deretter forårsaker nedbør av surt regn kjemiske reaksjoner som frigjør NOx, både fra denne typen bergarter og fra bakken.
Det er fersk forskning som tildeler 26% av planetens totale biotilgjengelige nitrogen til disse mekanismene for jorderosjon og bergforvitring..
Biotiske former for nitrogenfiksering
Noen bakterielle mikroorganismer har mekanismer som er i stand til å bryte trippelen av Nto og produsere NH-ammoniakk3, som lett omdannes til ammoniumion, NH4+ metaboliserbar.
Frilevende eller symbiotiske mikroorganismer
Formene for nitrogenfiksering av mikroorganismer kan forekomme gjennom frilevende organismer eller gjennom organismer som lever i symbiotiske assosiasjoner med planter..
Selv om det er store morfologiske og fysiologiske forskjeller mellom nitrogenfikserende mikroorganismer, er fikseringsprosessen og nitrogenaseenzymsystemet som brukes av alle disse veldig like..
Kvantitativt er biotisk nitrogenfiksering gjennom disse to mekanismene (fritt liv og symbiose) den viktigste globalt..
Mekanismer for å holde nitrogenasesystemet aktivt
Nitrogenfikserende mikroorganismer har strategiske mekanismer for å holde nitrogenase enzymatisk system aktivt..
Disse mekanismene inkluderer åndedrettsvern, konformasjonell kjemisk beskyttelse, reversibel inhibering av enzymaktivitet, tilleggssyntese av en alternativ nitrogenase med vanadium og jern som kofaktorer, dannelse av diffusjonsbarrierer for oksygen og romlig separasjon av nitrogenase.
Noen har mikroaerofilisitet, for eksempel de kjemotrofiske bakteriene i slekten Azospirilium, Aquaspirillum, Azotobacter, Beijerinkia, Azomonas, Derxia, Crynebacterium, Rhizobium, Agrobacterium, Thiobacillus og fototrofer av sjangrene Gleocapsa, Anabaena, Spirulina, Nostoc, Oscillatoria, Calothrix, Lingbya.
Andre presenterer fakultativ anaerobiose, for eksempel de kjemostrofiske slektene: Klebsiella, Citrobacter, Erwinia, Bacillus, Propionibacterium og fototrofer av sjangrene Rhodospirillum, Rhodopsuedomonas.
Biotisk nitrogenfiksering av frilevende mikroorganismer
Nitrogenfikserende mikroorganismer som lever i jorden i fri (asymbiotisk) form er i utgangspunktet arkebakterier og bakterier.
Det er flere typer bakterier og cyanobakterier som kan omdanne atmosfærisk nitrogen, Nto, i ammoniakk, NH3. I henhold til den kjemiske reaksjonen:
Nto+8H++8e-+16 ATP → 2 NH3+Hto+16 ADP + 16Pi
Denne reaksjonen krever formidling av nitrogenaseenzymsystemet og en kofaktor, vitamin B12. I tillegg bruker denne nitrogenfikseringsmekanismen mye energi, er endoterm og krever 226 Kcal / mol Nto; det vil si at den bærer høye metabolske kostnader, og det er derfor den må kobles til et system som produserer energi.
Energi som kreves under N-fikseringsreaksjonento
Energien for denne prosessen er hentet fra ATP, som kommer fra oksidativ fosforylering koblet til elektrontransportkjeden (som bruker oksygen som den siste elektronakseptoren)..
Prosessen med å redusere molekylært nitrogen til ammoniakk reduserer også hydrogen i protonform H+ til molekylært hydrogen Hto.
Mange nitrogenasesystemer har koblet et hydrogengjenvinningssystem formidlet av hydrogenaseenzymet. Nitrogenfikserende cyanobakterier kobler fotosyntese til nitrogenfiksering.
Enzymet nitrogenase kompleks og oksygen
Nitrogenaseenzymkomplekset har to komponenter, komponent I, dinitrogenase med molybden og jern som kofaktorer (som vi vil kalle Mo-Fe-protein), og komponent II, dinitrogenase-reduktase med jern som kofaktor (Fe-protein).
Elektronene som er involvert i reaksjonen blir donert først til komponent II og senere til komponent I, hvor nitrogenreduksjonen oppstår..
For at overføring av elektroner fra II til I skal skje, kreves Fe-proteinet å binde seg til et Mg-ATP på to aktive steder. Denne foreningen genererer en konformasjonsendring i Fe-proteinet. Et overskudd av oksygen kan produsere en annen konformasjonsendring i Fe-proteinet ugunstig, siden det kansellerer sin elektronmottakende kapasitet.
Dette er grunnen til at nitrogenaseenzymkomplekset er veldig utsatt for tilstedeværelse av oksygen over tålelige konsentrasjoner, og at noen bakterier utvikler mikroaerofile livsformer eller fakultativ anaerobiose..
Blant de frittlevende nitrogenfikserende bakteriene kan nevnes cellegifene som tilhører slektene Clostridium, Desulfovibrio, Desulfotomaculum, Methanosarcina, og fototrofene til sjangrene Chromatium, Thiopedia, Ectothiordospira, blant andre.
Biotisk nitrogenfiksering av mikroorganismer i symbiotisk liv med planter
Det er andre nitrogenfikserende mikroorganismer som er i stand til å etablere symbiotiske assosiasjoner med planter, spesielt med belgfrukter og gress, enten i form av ektosymbiose (der mikroorganismen befinner seg utenfor planten), eller endosymbiose (der mikroorganismen lever i celler eller intercellular mellomrom av planten).
Det meste av nitrogenet som er fiksert i terrestriske økosystemer kommer fra de symbiotiske foreningene av bakterier av slektene Rhizobium, Bradyrhizobium, Sinorhizobium, Azorhizobium, Allorhizoium Y Mesorhizobium, med belgfrukter.
Det er tre interessante typer nitrogenfikserende symbioser: assosiative rhizocenoser, systemer med cyanobakterier som symbionter, og mutualistiske endorizobioser..
Rhizocenosis
I assosiative rhizocenosis-lignende symbioser dannes ingen spesialiserte strukturer i plantens røtter.
Eksempler på denne typen symbiose er etablert mellom maisplanter (Zea mais) og sukkerrør (Saccharum officinarum) med Gluconacetobacter, Azoarcus, Azospirillum Y Herbaspirillum.
I rhizocenosis bruker de nitrogenfikserende bakteriene roteksudatet til planten som et næringsmedium og koloniserer de intercellulære rommene i rotbarken..
Cyanobakterier symbionter
I systemer der cyanobakterier deltar, har disse mikroorganismene utviklet spesielle mekanismer for sameksistens av anoksisk nitrogenfiksering og deres oksygeniske fotosyntese..
For eksempel i Gleothece Y Synechococcus, de er midlertidig atskilt: de utfører fotosyntese på dagtid og nitrogenfiksering om natten.
I andre tilfeller er det romlig separasjon av begge prosesser: nitrogen er fiksert i grupper av differensierte celler (heterocyster), hvor fotosyntese ikke utføres.
Nitrogenfikserende symbiotiske assosiasjoner av cyanobakterier av slekten Nostoc med ikke-vaskulære planter (antóceras), som i hulrom av Nothocerus endiviaefolius, med liverworts Gakstroemia magellanica og Chyloscyphus obvolutus i ektosymbiose separat, med bryophytes (som danner lav i mos rhizoids), og med høyere angiosperm planter, for eksempel med de 65 flerårige urter av slekten Gunnnera.
For eksempel har den nitrogenfikserende symbiotiske foreningen av cyanobakterier blitt observert Anabaena med en bryophyte, ikke-vaskulær plante, på blader av den lille bregnen Azolla anabaenae.
Endorizobiose
Som eksempler på endorhizobiose kan vi nevne foreningen kalt actinorhiza som er etablert mellom Frankia og noen treaktige planter som casuarina (Casuarina cunninghamiana) Y orAlnus glutinosa), og foreningen Rhizobium-belgfrukter.
De fleste artene i familien Leguminosae, danne symbiotiske assosiasjoner med bakterie Rhizobium og denne mikroorganismenhar evolusjonær spesialisering i overføring av nitrogen til planten.
I røttene til planter assosiert med Rhizobium, de såkalte radikale nodulene dukker opp, stedet hvor nitrogenfiksering finner sted.
I belgfrukter Sesbania Y Aechynomene, i tillegg dannes knuter på stilkene.
- Kjemiske signaler
Det er en utveksling av kjemiske signaler mellom symbioten og verten. Planter har vist seg å utstråle visse typer flavonoider som induserer ekspresjon av nikkegener i Rhizobium, som produserer nodulasjonsfaktorer.
Nodulasjonsfaktorene genererer modifikasjoner i rothårene, dannelse av en infeksjonskanal og celledeling i rotbarken, som fremmer dannelsen av knuten.
Noen eksempler på nitrogenfikserende symbiose mellom høyere planter og mikroorganismer er vist i følgende tabell..
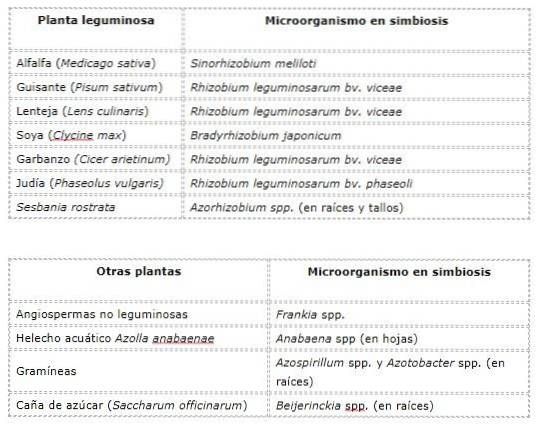
Mykorrhizobiose
I tillegg er det i de fleste økosystemer nitrogenfikserende mycorrhizal sopp, som tilhører phyla Glomeromycota, Basidiomycota og Ascomycota.
Mycorrhizal sopp kan leve i ektosymbiose, danne en hyphal kappe rundt de fine røttene til noen planter og spre ytterligere hyfer i jorden. Også i mange tropiske områder er planter vert for mycorrhizae i endosymbiose, hvis hyfer trenger gjennom rotceller.
Det er mulig at en sopp danner mycorrhizae med flere planter samtidig, i hvilket tilfelle det er etablert innbyrdes forhold mellom dem; eller at den mykorrhizale soppen parasiteres av en plante som ikke fotosyntetiserer, mycoheterotrofisk, slik som de fra slekten Monotrope. Også flere sopper kan etablere symbiose med en enkelt plante samtidig.
Referanser
- Inomura, K., Bragg, J. and Follows, M. (2017). En kvantitativ analyse av de direkte og indirekte kostnadene ved nitrogenfiksering. ISME Journal. 11: 166-175.
- Masson-Bovin, C. og Sachs, J. (2018). Symbiotisk nitrogenfiksering av rhizobia - røttene til en suksesshistorie. Plantebiologi. 44: 7-15. doi: 10.1016 / j.pbi.2017.12.001
- Menge, D.N.L., Levin, S.A. og Hedin, L.O. (2009). Fakultativ versus obligatorisk nitrogenfikseringsstrategi og deres økosystemkonsekvenser. Den amerikanske naturforskeren. 174 (4) doi: 10.1086 / 605377
- Newton, W.E. (2000). Nitrogenfiksering i perspektiv. I: Pedrosa, F.O. Redaktør. Nitrogenfiksering fra molekyler til avlingens produktivitet. Nederland: Kluwer Academic Publishers. 3-8.
- Pankievicz; V.C.S., gjør Amaral; F.P., Santos, K.D.N., Agtuca, B., Xu, Y., Schultes, M.J. (2015). Robust biologisk nitrogenfiksering i en modell gress-bakteriell forening. Plantejournalen. 81: 907-919. doi: 10.1111 / tpj.12777.
- Wieder, W.R., Cleveland, C.C., Lawrence, D. og Bonau, G.B. (2015). Effekter av modellens strukturelle usikkerhet på karbonsyklusprojeksjoner: biologisk nitrogenfiksering som et studiefall. Miljøforskningsbrev. 10 (4): 1-9. doi: 10.1088 / 1748-9326 / 10/4/044016



Ingen har kommentert denne artikkelen ennå.