
Oksidative fosforyleringstrinn, funksjoner og hemmere
De oksidativ fosforylering er en prosess der ATP-molekyler blir syntetisert fra ADP og PJeg (uorganisk fosfat). Denne mekanismen utføres av bakterier og eukaryote celler. I eukaryote celler foregår fosforylering i den mitokondrielle matrisen til ikke-fotosyntetiske celler.
ATP-produksjon er drevet av overføring av elektroner fra koenzymer NADH eller FADHto til Oto. Denne prosessen representerer den høyeste energiproduksjonen i cellen og er avledet fra nedbrytningen av karbohydrater og fett..
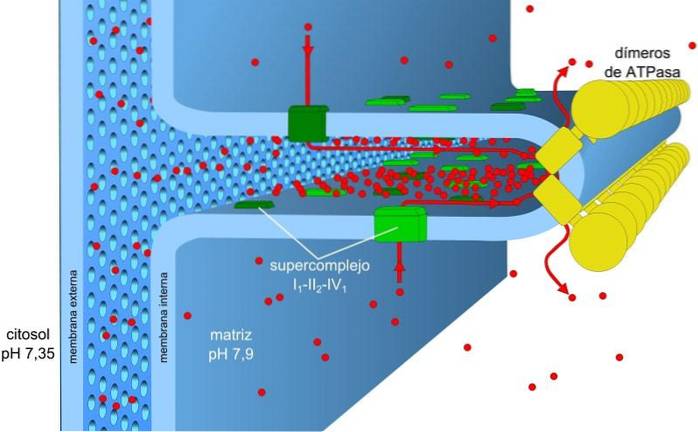
Energien lagret i ladnings- og pH-gradienter, også kjent som protonmotivkraften, gjør at denne prosessen kan finne sted. Protongradienten som genereres får den ytre delen av membranen til å ha en positiv ladning på grunn av konsentrasjonen av protoner (H+) og mitokondriell matrise er negativ.
Artikkelindeks
- 1 Hvor forekommer oksidativ fosforylering?
- 1.1 Cellekraftverk
- 2 trinn
- 2.1 Elektron transportkjede
- 2.2 Succinate CoQ-reduktase
- 2.3 Kobling eller energitransduksjon
- 2.4 Kjemosmotisk kobling
- 2.5 ATP-syntese
- 3 produkter
- 4 funksjoner
- 5 Kontroll av oksidativ fosforylering
- 5.1 Koordinert kontroll av ATP-produksjon
- 5.2 Kontroll av akseptor
- 5.3 Frakoblingsmidler
- 5.4 Hemmere
- 6 Referanser
Hvor forekommer oksidativ fosforylering?
Prosessene med elektrontransport og oksidativ fosforylering er assosiert med en membran. I prokaryoter utføres disse mekanismene gjennom plasmamembranen. I eukaryote celler assosieres de med mitokondriell membran.
Antall mitokondrier som finnes i celler varierer avhengig av celletype. For eksempel hos pattedyr mangler erytrocytter disse organellene, mens andre celletyper, for eksempel muskelceller, kan ha opptil millioner av dem..
Den mitokondrielle membranen består av en enkel ytre membran, en noe mer kompleks indre membran, og mellom dem intermembranrommet, der mange ATP-avhengige enzymer er lokalisert.
Den ytre membranen inneholder et protein kalt porin som danner kanalene for enkel diffusjon av små molekyler. Denne membranen er ansvarlig for å opprettholde strukturen og formen på mitokondriene.
Den indre membranen har høyere tetthet og er rik på proteiner. Det er også ugjennomtrengelig for molekyler og ioner, så for å krysse det trenger de intermembrane proteiner for å transportere dem..
Inne i matrisen strekker brettene av den indre membranen seg og danner rygger som gjør at den har et stort område i et lite volum.
Cellekraftverk
Mitokondrien anses å være den sentrale produsenten av cellulær energi. Den inneholder enzymene som er involvert i prosessene av sitronsyresyklus, fettsyreoksidasjon og redoks-enzymer og proteiner for elektrontransport og ADP-fosforylering.
Protonkonsentrasjonsgradienten (pH-gradienten) og ladningsgradienten eller det elektriske potensialet i den indre membranen i mitokondriene er ansvarlige for protonmotivkraften. Den lave permeabiliteten til den indre membranen for ioner (annet enn H+) tillater mitokondriene å ha en stabil spenningsgradient.
Elektronisk transport, protonpumping og ATP-oppnåelse skjer samtidig i mitokondriene, takket være protonmotivkraften. PH-gradienten opprettholder sure forhold i intermembranen og mitokondriematrisen med alkaliske forhold.
For hver to elektroner overført til Oto Omtrent 10 protoner pumpes gjennom membranen, og skaper en elektrokjemisk gradient. Energien som frigjøres i denne prosessen produseres gradvis ved passering av elektroner gjennom transportkjeden.
Stadier
Energien som frigjøres under oksidasjonsreduksjonsreaksjonene til NADH og FADHto er betydelig høy (rundt 53 kcal / mol for hvert par elektroner), så for å kunne brukes til fremstilling av ATP-molekyler, må den produseres gradvis med passering av elektroner gjennom transportører.
Disse er organisert i fire komplekser plassert på den indre mitokondriale membranen. Koblingen av disse reaksjonene til syntesen av ATP utføres i et femte kompleks.
Elektron transportkjede
NADH overfører et par elektroner som kommer inn i kompleks I i elektrontransportkjeden. Elektroner overføres til flavinmononukleotidet, og deretter til ubiquinon (koenzym Q) gjennom en jern-svoveltransportør. Denne prosessen frigjør en stor mengde energi (16,6 kcal / mol).
Ubiquinone transporterer elektroner over membranen til kompleks III. I dette komplekset passerer elektronene gjennom cytokromer b og c1 takket være en jern-svovel-transportør.
Elektroner passerer fra kompleks III til kompleks IV (cytokrom c oksidase), overført en etter en i cytokrom c (perifert membranprotein). I kompleks IV passerer elektronene gjennom et par kobberioner (Cutilto+), etterfulgt av cytokrom ctil, deretter til et annet par kobberioner (Cubto+) og fra dette til cytokrom a3.
Til slutt overføres elektronene til Oto som er den siste akseptoren og danner et vannmolekyl (HtoO) for hvert mottatte elektronpar. Passasjen av elektroner fra kompleks IV til Oto Det genererer også en stor mengde fri energi (25,8 kcal / mol).
Succinate CoQ reduktase
Kompleks II (succinat CoQ reduktase) mottar et par elektroner fra sitronsyresyklusen ved oksidasjon av et succinatmolekyl for å fumarere. Disse elektronene overføres til FAD, og passerer deretter gjennom en jern-svovelgruppe, til ubiquinon. Fra dette koenzymet passerer de til kompleks III og følger ruten tidligere beskrevet.
Energien som frigjøres i elektronoverføringsreaksjonen til FAD er ikke nok til å drive protonene gjennom membranen, så det genereres ingen protonkraftkraft i dette trinnet i kjeden, og følgelig gir FADH mindre H+ at NADH.
Kobling eller transduksjon av energi
Energien som genereres i elektrontransportprosessen beskrevet tidligere, må kunne brukes til produksjon av ATP, en reaksjon katalysert av enzymet ATP-syntase eller kompleks V. Konserveringen av denne energien er kjent som energikobling, og mekanismen har vært vanskelig å karakterisere.
Flere hypoteser er beskrevet for å beskrive denne energitransduksjonen. Den best aksepterte er den kjemiosmotiske koblingshypotesen, beskrevet nedenfor..
Kjemosmotisk kobling
Denne mekanismen foreslår at energien som brukes til ATP-syntese kommer fra en protongradient i cellemembraner. Denne prosessen griper inn i mitokondriene, kloroplaster og bakterier og er knyttet til transport av elektroner.
Komplekser I og IV i elektrontransport fungerer som protonpumper. Disse gjennomgår konformasjonsendringer som gjør at de kan pumpe protoner inn i mellomrommet. I kompleks IV, for hvert par elektroner, pumpes to protoner ut av membranen, og to blir igjen i matrisen og danner HtoELLER.
Ubiquinone i kompleks III aksepterer protoner fra kompleks I og II og frigjør dem til utsiden av membranen. Kompleksene I og III tillater hver passering av fire protoner for hvert par transporterte elektroner.
Den mitokondrielle matrisen har en lav konsentrasjon av protoner og et negativt elektrisk potensial, mens intermembranrommet presenterer de omvendte forholdene. Strømmen av protoner gjennom denne membranen representerer den elektrokjemiske gradienten som lagrer den nødvendige energien (± 5 kcal / mol per proton) for syntesen av ATP..
ATP-syntese
Enzymet ATP-syntetase er det femte komplekset som er involvert i oksidativ fosforylering. Det er ansvarlig for å utnytte energien til den elektrokjemiske gradienten for å danne ATP.
Dette transmembrane proteinet består av to komponenter: F0 og F1. Komponent F0 tillater retur av protoner til mitokondriell matrise som fungerer som en kanal og F1 katalyserer syntesen av ATP av ADP og PJeg, ved å bruke energien fra nevnte retur.
ATP-synteseprosessen krever en strukturendring i F1 og montering av komponenter F0 og F1. Proton translokasjon gjennom F0 forårsaker konformasjonsendringer i tre underenheter av F1, slik at den kan fungere som en rotasjonsmotor som styrer dannelsen av ATP.
Underenheten som er ansvarlig for binding av ADP med PJeg den går fra en svak tilstand (L) til en aktiv (T). Når ATP dannes, går en andre underenhet i åpen tilstand (O) som tillater frigjøring av dette molekylet. Etter at ATP er utgitt, går denne underenheten fra åpen tilstand til en inaktiv tilstand (L).
ADP- og P-molekylerJeg binde seg til en underenhet som har gått fra en O-tilstand til en L-tilstand.
Produkter
Elektrontransportkjeden og fosforylering produserer ATP-molekyler. Oksidasjonen av NADH gir ca. 52,12 kcal / mol (218 kJ / mol) fri energi.
Den samlede reaksjonen for oksidasjon av NADH er:
NADH + 1⁄2 Oto +H+ ↔ HtoO + NAD+
Overføring av elektroner fra NADH og FADHto oppstår gjennom forskjellige komplekser, slik at den frie energiendringen ΔG ° kan deles inn i mindre energi "pakker", som er koblet til ATP-syntese.
Oksidasjonen av ett NADH-molekyl genererer syntesen av tre ATP-molekyler. Mens oksidasjonen av et FADH-molekylto par til syntesen av to ATP-er.
Disse koenzymer kommer fra glykolyse- og sitronsyresyklusprosesser. For hvert molekyl glukose som brytes ned, produserer de 36 eller 38 molekyler ATP, avhengig av plasseringen av cellene. 36 ATP produseres i hjernen og skjelettmuskelen, mens 38 ATP produseres i muskelvev..
Funksjoner
Alle organismer, encellede og flercellede, trenger minimal energi i cellene for å utføre prosessene i dem, og i sin tur opprettholde vitale funksjoner i hele organismen..
Metabolske prosesser krever energi for å finne sted. Det meste av brukbar energi oppnås ved nedbrytning av karbohydrater og fett. Denne energien kommer fra den oksidative fosforyleringsprosessen.
Kontroll av oksidativ fosforylering
ATP-utnyttelsesgraden i celler styrer syntesen, og på grunn av koblingen av oksidativ fosforylering med elektrontransportkjeden, regulerer den også generelt hastigheten på elektrontransport..
Oksidativ fosforylering har en streng kontroll som sørger for at ATP ikke genereres raskere enn det forbrukes. Det er visse trinn i prosessen med elektrontransport og koblet fosforylering som regulerer hastigheten på energiproduksjonen..
Koordinert kontroll av ATP-produksjon
Hovedveiene for energiproduksjon (cellulær ATP) er glykolyse, sitronsyresyklusen og oksidativ fosforylering. Koordinert kontroll av disse tre prosessene regulerer ATP-syntese.
Kontrollen av fosforylering av ATP-masseforholdet avhenger av det nøyaktige bidraget til elektroner i transportkjeden. Dette avhenger igjen av [NADH] / [NAD+] som holdes forhøyet av virkningen av glykolyse og sitronsyresyklusen.
Denne koordinerte kontrollen utføres ved å regulere glykolysekontrollpunktene (PFK inhibert av citrat) og sitronsyresyklusen (Pyruvat dehydrogenase, citrat tapease, isocitrate dehydrogenase og α-ketoglutarat dehydrogenase)..
Kontroll av akseptor
Kompleks IV (cytokrom c oksidase) er et enzym regulert av et av dets substrater, det vil si at dets aktivitet blir kontrollert av redusert cytokrom c (cto+), som igjen er i likevekt med konsentrasjonsforholdet mellom [NADH] / [NAD+] og masseforhold på [ATP] / [ADP] + [PJeg].
Jo høyere forholdet [NADH] / [NAD+] og senk [ATP] / [ADP] + [PJeg], jo høyere er konsentrasjonen av cytokrom [cto+] og jo større aktivitet av kompleks IV. Dette tolkes for eksempel hvis vi sammenligner organismer med forskjellige hvile- og høyaktivitetsaktiviteter.
Hos et individ med høy fysisk aktivitet, forbruket av ATP og derfor hydrolysen til ADP + PJeg vil være veldig høy, og generere en forskjell i masseforhold som forårsaker en økning i [cto+] og derfor en økning i ATP-syntese. Hos en person i ro oppstår den omvendte situasjonen.
Til slutt øker frekvensen av oksidativ fosforylering med konsentrasjonen av ADP i mitokondriene. Denne konsentrasjonen avhenger av ADP-ATP-translokatorene som er ansvarlige for transporten av adeninnukleotider og PJeg fra cytosol til mitokondriell matrise.
Frakoblingsmidler
Oksidativ fosforylering påvirkes av visse kjemiske midler, som tillater elektrontransport å fortsette uten at ADP-fosforylering forekommer, og kobler fra energiproduksjon og konservering.
Disse midlene stimulerer oksygenforbrukshastigheten til mitokondriene i fravær av ADP, og forårsaker også en økning i ATP-hydrolyse. De handler ved å eliminere et mellomledd eller bryte en energitilstand i elektrontransportkjeden.
2,4-dinitrofenol, en svak syre som passerer gjennom mitokondriale membraner, er ansvarlig for å spre protongradienten, da de binder seg til dem på den sure siden og frigjør dem på basissiden.
Denne forbindelsen ble brukt som en "slankepille" da den ble funnet å gi en økning i respirasjonen, derfor en økning i metabolisk hastighet og tilhørende vekttap. Imidlertid ble det vist at den negative effekten til og med kan føre til død.
Spredningen av protongradienten produserer varme. Celler i brunt fettvev bruker hormonstyrt frakobling for å produsere varme. Dvalende pattedyr og nyfødte som mangler hår, består av dette vevet som fungerer som et slags termisk teppe..
Hemmere
Forbindelser eller inhiberende midler forhindrer begge inntaket av Oto (elektrontransport) slik som tilhørende oksidativ fosforylering. Disse midlene forhindrer dannelsen av ATP ved å bruke energien som produseres i elektronisk transport. Derfor stopper transportkjeden ettersom energiforbruket ikke er tilgjengelig..
Det antibiotiske oligomycinet fungerer som en fosforyleringshemmer i mange bakterier, og forhindrer stimulering av ADP til ATP-syntese..
Det er også ionoformidler som danner fettløselige komplekser med kationer som K+ og Na+, og de passerer gjennom mitokondriell membran med disse kationene. Mitokondriene bruker deretter energien som produseres i elektrontransport til å pumpe kationer i stedet for å syntetisere ATP..
Referanser
- Alberts, B., Bray, D., Hopkin, K., Johnson, A., Lewis, J., Raff, M., Roberts, K. & Walter, P. (2004). Essensiell cellebiologi. New York: Garland Science.
- Cooper, G. M., Hausman, R. E. & Wright, N. (2010). Cellen. (s. 397-402). Marban.
- Devlin, T. M. (1992). Lærebok for biokjemi: med kliniske sammenhenger. John Wiley & Sons, Inc..
- Garrett, R. H., & Grisham, C. M. (2008). Biokjemi. Thomson Brooks / Cole.
- Lodish, H., Darnell, J. E., Berk, A., Kaiser, C. A., Krieger, M., Scott, M. P., & Matsudaira, P. (2008). Molekylær cellebiologi. Macmillan.
- Nelson, D. L., og Cox, M. M. (2006). Lehninger prinsipper for biokjemi 4. utgave. Ed Omega. Barcelona.
- Voet, D., og Voet, J. G. (2006). Biokjemi. Panamerican Medical Ed..



Ingen har kommentert denne artikkelen ennå.