
Sykliske hydrokarboner struktur, egenskaper, eksempler

De sykliske hydrokarboner De er organiske forbindelser som består av karbon- og hydrogenatomer som knytter seg for å danne ringer eller sykliske strukturer. Det er hovedsakelig av tre typer: alisykliske, aromatiske og polysykliske.
Disse typer hydrokarboner kan da bestå av lukkede versjoner av alkaner, alkener og alkyner; har ringer med aromatiske systemer, slik som benzen og dets derivater; eller presentere intrikate og fascinerende strukturer. Av alle er alicykliske stoffer de enkleste og blir vanligvis representert ved bruk av polygoner.
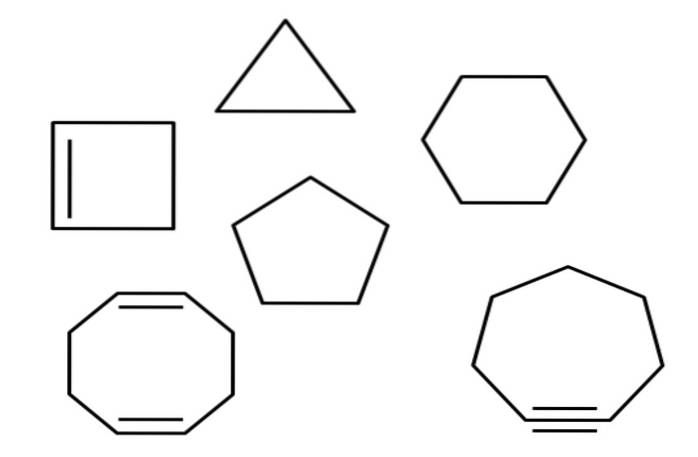
Ovenfor har du for eksempel flere alicykliske hydrokarboner. De ser ut som enkle polygoner: en firkant, trekant, femkant, sekskant osv. Hvis en av dens C-C-bindinger kunne kuttes med en saks, ville resultatet være en alkan, alken (hvis den har dobbeltbindinger) eller alkan (hvis den har trippelbindinger).
Egenskapene deres skiller seg ikke for mye fra de åpne kjeden hydrokarboner som de stammer fra; selv om, kjemisk, jo større de er, desto mer stabil vil de være, og deres interaksjon med et molekylært medium blir mer uttalt (på grunn av deres større kontaktareal).
Artikkelindeks
- 1 Struktur
- 1.1 Konformasjoner
- 2 eiendommer
- 2.1 Intermolekylære krefter
- 3 Nomenklatur
- 4 Eksempler
- 5 Referanser
Struktur
Når vi går direkte til saken som gjelder strukturene deres, bør det avklares at de ikke er flate, selv når de ser ut til å være polygoner. Det eneste unntaket fra denne påstanden finnes i cyklopropan (trekanten), siden de tre punktene nødvendigvis må hvile på samme plan..
Det er også nødvendig å presisere at begrepene "sykluser" og "ringer" ofte er utskiftbare. en ring trenger ikke å være sirkulær, og derfor kan den få endeløse geometrier så lenge det er en lukket struktur. Syklopropan sies da å ha en trekantet ring eller syklus.
Alle karbon har SP-hybridisering3, slik at geometriene deres er tetraedriske, og deres bindinger bør ideelt sett skilles med en vinkel på 109,5 °; Dette er imidlertid ikke mulig for strukturer som er lukkede som cyklopropan, cyklobutan (kvadrat) eller cyklopentan (pentagon).
Vi snakker da om en spenning som destabiliserer molekylet, og bestemmes eksperimentelt ved å måle gjennomsnittlig forbrenningsvarme for hver CH-gruppe.to.
Konformasjoner
Og hva skjer når det er dobbelt- eller trippelbindinger? Spenningen øker, for der det er en av dem, vil strukturen bli tvunget til å "krympe" og holde seg flat; som, etter hverandre, ville tvinge en konformasjon over andre, sannsynligvis formørke nærliggende hydrogenatomer.

På bildet ovenfor er to konformatorer for cykloheksan vist for å prøve å forklare det ovennevnte. Atomer som er i posisjonene til eller og de sies å være henholdsvis aksiale eller ekvatoriale. Merk at i stedet for en flat sekskant har du en stol (venstre) og en båt (høyre).
Disse strukturene er dynamiske og skaper en balanse mellom dem. Hvis atomene kommer inn til de er veldig voluminøse, ringen vil "imøtekomme" for å plassere dem i ekvatoriale stillinger; siden de er orientert mot sidene av ringen (som vil forsterke eller svekke intermolekylære interaksjoner).
Hvis vi ser på hvert karbon separat, vil det sees at de er tetraedrale. Dette ville ikke være tilfelle hvis det var en dobbeltbinding: deres sp-hybridiseringerto de ville tvinge strukturen til å flate seg ut; og hvis det er en trippelbinding, for å justere. Den plane strukturen til benzen er den maksimale representasjonen av dette.
Eiendommer
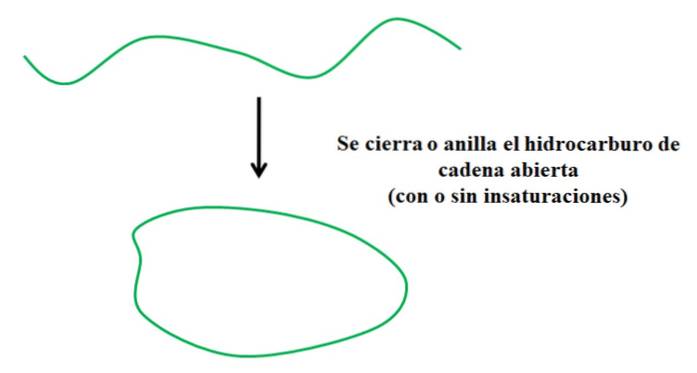
Anta at du har et åpent hydrokarbon (med eller uten umettninger eller grener). Hvis vi kunne bli med på endene, ville det skape en ring eller syklus (som på bildet ovenfor).
Fra et organisk syntese synspunkt skjer ikke dette bare slik; det må være gode forlatende grupper knyttet til enden av kjeden, som når de forlater, fremmer kjedestengingen (hvis løsningen er veldig fortynnet).
Med dette i bakhodet kan det sees at det grønne spor hydrokarbonet bare gjennomgår en transformasjon med hensyn til dets struktur; uten å bryte eller legge til nye bindinger med andre atomer. Det betyr at det kjemisk fortsetter å være det samme før og etter lukking eller belte..
Derfor skiller de kjemiske eller fysiske egenskapene til disse alicykliske hydrokarboner seg ikke for mye fra deres kolleger med åpen kjede. Begge er reaktive mot samme art (dvs. halogener under ultrafiolett lys), og kan gjennomgå sterk oksidasjon eller forbrenning ved å frigjøre varme..
Intermolekylære krefter
Det er et unektelig faktum: ringen har større kontaktareal enn den åpne kjeden, og derfor er intermolekylære interaksjoner sterkere.
Resultatet er at kokepunktene og smeltepunktene har en tendens til å være høyere, det samme gjør dens tettheter. Så mange forskjeller kan noteres i deres brytningsindeks eller damptrykk.
Nomenklatur
Når vi går tilbake til eksemplet med hydrokarbon med et grønt slag, forblir nomenklaturen uendret når den har lukket seg inn (som en slange som biter i sin egen hale). Derfor forblir navngivningsreglene de samme; med mindre polysykliske eller aromatiske hydrokarboner er adressert.
Tre forbindelser er vist nedenfor, som vil få de rette navnene:
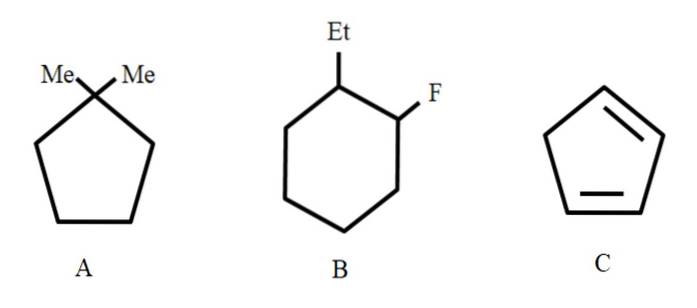
Til å begynne med, ettersom de er lukkede strukturer, brukes prefikssyklusen til å referere til dem (her blir ordet ring henvist).
Fra venstre til høyre har vi: en cyklopentan, en cykloheksan og en annen cyklopentan. Karbonene er oppført på en slik måte at substituentene tildeles de minste tallene, og de er også nevnt i alfabetisk rekkefølge..
Dermed er A: 1,1-dimetylcyklopentan. I B begynner vi med å nevne etylsubstituenten før fluor, så navnet er: 1-etyl-2-fluorsykloheksan. Og så for C, blir dobbeltbindingene tatt som substituenter, antall karbonatomer som danner det må angis: 1,3-cyklopentadien.
Eksempler
Gjennom artikkelen er det nevnt flere sykliske hydrokarboner. I det første bildet kan du finne: cyklopropan, cyclobutane, cyclopentane, cyclohexane, cycloheptane and cyclooctane.
Et bredt spekter av derivater kan fås fra dem, og det er nok å plassere dobbelt- eller trippelbindinger på dem for å ha henholdsvis cykloalkener eller cykloalkiner. Og med hensyn til aromatiske hydrokarboner er det nok å huske benzenringen og erstatte den eller reprodusere den i to dimensjoner..
Imidlertid er de mest ekstraordinære (og problematiske når det gjelder å forstå nomenklaturen deres) polysykliske hydrokarboner; det vil si at enkle polygoner ikke er nok til å representere dem på en enkel måte. Tre av dem det er verdt å nevne er: Cuban, Canastano og Pagoda (bilder nedenfor).
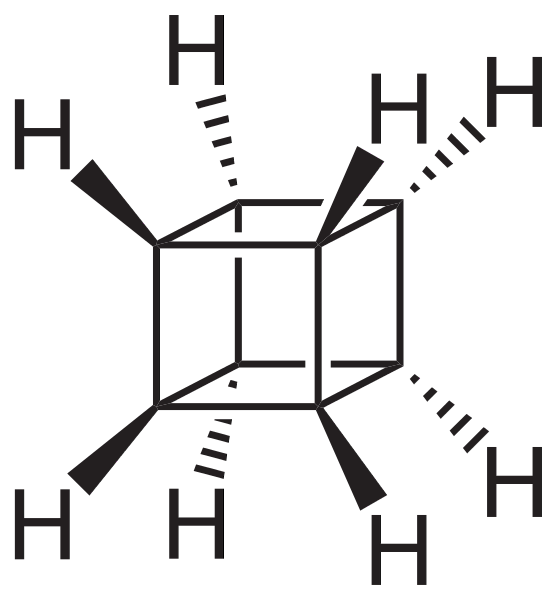
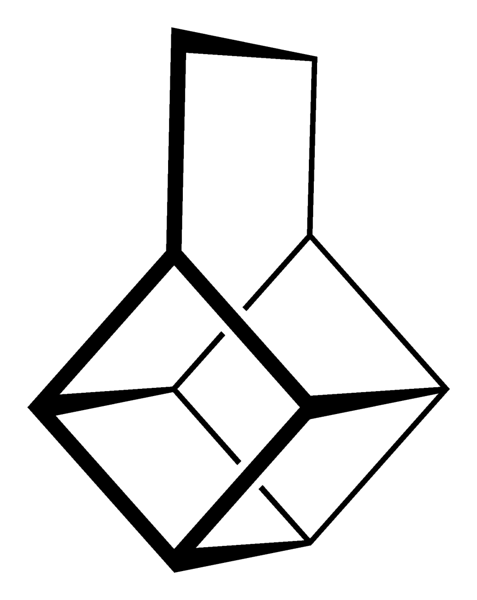

Hver og en av dem har sin komplekse syntesemetode, sin historie, kunst og en latent fascinasjon for de uendelige strukturelle mulighetene som enkle hydrokarboner kan nå..
Referanser
- Morrison, R. T. og Boyd, R, N. (1987). Organisk kjemi. 5. utgave. Redaksjonell Addison-Wesley Interamericana.
- Carey F. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. Amines. (10. utgave.). Wiley pluss.
- Reid Danielle. (2019). Sykliske hydrokarboner: definisjon og eksempel. Studere. Gjenopprettet fra: study.com
- CK-12 Foundation. (5. juni 2019). Sykliske hydrokarboner. Kjemi LibreTexts. Gjenopprettet fra: chem.libretexts.org
- Wikipedia. (2019). Syklisk forbindelse. Gjenopprettet fra: en.wikipedia.org
- Cowboy Miguel. (2019). Sykliske hydrokarboner. Gjenopprettet fra: deciencias.net



Ingen har kommentert denne artikkelen ennå.