
Kaliumhydroksydstruktur, egenskaper, bruksområder

De kaliumhydroksyd det er et hvitt krystallinsk uorganisk fast stoff. Den kjemiske formelen er KOH. Krystallene absorberer lett vann fra luften, og det er derfor det sies å være en hygroskopisk forbindelse. Det er en sterk base og absorberer karbondioksid (COto) av miljøet.
Industrielt produseres den ved elektrolyse av kaliumklorid (KCl). Av hensyn til energibesparelse og for produktets renhet brukes kvikksølv (Hg) celler i denne metoden..

Men i mange år har det vært bekymring for kvikksølvforurensning generert av denne prosessen. Faktisk er utslipp i miljøet av avløpsholdig kvikksølv strengt forbudt. Det er andre prosesser som membran og membran, men kvikksølv foretrekkes fordi det produserer en 50% ren KOH-løsning..
Det er også ikke-elektrokjemiske prosesser som spaltning av kaliumnitritt (KNOto) i nærvær av jernoksid (FetoELLER3).
KOH-løsninger oppnådd i industrielle prosesser fordampes for å oppnå 90-95% KOH. Restinnholdet på 5-10% vann er bundet til KOH i form av kaliumhydroksydmonohydrat (KOH.HtoELLER).
På grunn av de kaustiske egenskapene og den sterke grunnleggende bruken har den et bredt spekter av applikasjoner. Det fungerer som råmateriale i såper og vaskemidler, trykkfarger eller kosmetikk, blant annet. Det brukes også til å vaske industrigasser, ved påvisning av sopp i mikroskop og kan brukes i næringsmiddelindustrien.
Selv om det er en veldig stabil forbindelse, er det klassifisert som etsende. Det må håndteres med forsiktighet, da det kan forårsake forbrenning i øyne, hud og slimhinner.
Artikkelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Kokepunkt
- 3,5 Tetthet
- 3.6 Løselighet
- 3,7 pH
- 3.8 Andre egenskaper
- 4 bruksområder
- 4.1 Ved produksjon av andre kaliumforbindelser
- 4.2 I forskjellige applikasjoner
- 4.3 I medisinske applikasjoner
- 4.4 I kosmetikkindustrien
- 4.5 I landbruket
- 4.6 I industrielle kjemiske prosesser
- 4.7 I næringsmiddelindustrien
- 4.8 Ved å skaffe biodiesel
- 4.9 Nyere studier
- 5 Referanser
Struktur
KOH-krystallet ved vanlige temperaturer er monoklinisk, med hvert kalium (K) -atom omgitt av en forvrengt oktaeder av oksygen (O) -atomer. I sin tur danner hydroksylgruppene (OH) en kjede i form av en sikksakk bundet av hydrogener, hvor O-O-avstandene er 3,35 A, og utelukker enhver betydelig hydrogenbinding..
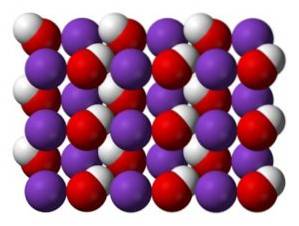
Ved høye temperaturer har KOH en kubisk krystallinsk form.
Nomenklatur
- Kaliumhydroksyd.
- Kaustisk potash.
- Kaliumhydrat.
- Kaliumblekemiddel.
Eiendommer
Fysisk tilstand
Hvitt krystallinsk fast stoff.
Molekylær vekt
56,106 g / mol.
Smeltepunkt
380 ° C; 406 ºC er også rapportert (varierer avhengig av vanninnhold). Teknisk karakter (90-92% KOH) smelter ved ca. 250 ° C.
Kokepunkt
1327 ºC.
Tetthet
2,044 g / cm3
Løselighet
Løselig i kaldt vann (107 g / 100 ml ved 15 ° C) og i varmt vann (178 g / 100 ml ved 100 ° C). Dens oppløsning i vann er en veldig eksoterm prosess, dette betyr at det genereres en stor mengde varme.
Løselig i alkoholer. Løselig i glyserin. Uoppløselig i eter.
pH
13,5 (i 0,1 molær vandig oppløsning).
Andre egenskaper
Dens krystaller er lekker eller hygroskopisk, noe som betyr at den absorberer vann fra luften. Det absorberer også lett COto fra luften.
Dens kjemiske reaksjoner er egenskapene til en sterk base. I vandig løsning reagerer den med en hvilken som helst svak syre og danner kaliumsaltet av syren. For eksempel reagerer den med karbonsyre (HtoCO3) eller med karbondioksid (COto) for å danne bikarbonat eller kaliumkarbonat.
Reagerer med alkoholer for å danne kaliumalkoksider, eller med hydrogensulfid HtoS for å danne kaliumsulfid eller bisulfid.
I vandige systemer danner KOH forskjellige hydrater: mono-, di- og tetrahydrater.
Vannholdige KOH-løsninger er fargeløse, sterkt basiske, såpegods og kaustiske. Det er et etsende materiale, både fast og i oppløsning.
Det er ikke brannfarlig, men når det oppvarmes til nedbrytning, avgir det giftige og etsende K-røyktoELLER.
Det forårsaker alvorlige forbrenninger i øyne, hud og slimhinner og i kontakt med metaller, som aluminium, tinn, bly eller sink, kan det generere utviklingen av hydrogengass (Hto), som er svært brannfarlig.
Varmen som produseres ved å komme i kontakt med fuktighet eller andre stoffer, kan skape nok varme til å antenne brennbare materialer..
applikasjoner
Ved produksjon av andre kaliumforbindelser
Kaliumhydroksid brukes som råvare for den kjemiske og farmasøytiske industrien. Den brukes til å produsere kaliumkarbonat (KtoCO3), kaliumpermanganat (KMnO4), kaliumfosfat (K3PO4), kaliumsilikat (KtoJa3) og kaliumcyanid (KCN), blant andre forbindelser.
I forskjellige applikasjoner
KOH med høy renhet har anvendelse i produksjonen av plantevernmidler, syntese av blekk og fargestoffer, kjemikalier for tannkjøtt, i fotografering som en alkali-fotoutvikler, som en elektrolytt i alkaliske batterier og brenselceller, i elektrolyse av vann, ved galvanisering eller galvanisering, litografi osv.
Teknisk kvalitet KOH brukes som råvare i såpe- og vaskemiddelindustrien; i produksjon av kosmetikk, glass og tekstiler; å avsvovle råolje; som tørkemiddel og i malings- og lakkfjernere, blant annet.
Det er også nyttig som et kaustisk middel i treindustrien, ved bomullsmercerisering, i analytisk kjemi for alkalimetriske titreringer, i organisk syntese og i vannbehandling..
I medisinske applikasjoner
I medisin brukes det i våt montering under utarbeidelse av kliniske prøver for mikroskopisk visualisering av sopp og andre soppelementer i hud, hår, negler, blant andre.
KOH-preparatet brukes til å klargjøre klinisk materiale slik at soppelementer lettere kan sees.
Et klinisk prøvefragment tilsettes til en del av 10% KOH-løsning på et glass. Deretter dekkes det med et dekselobjekt og får stå ved romtemperatur for å tillate vertscellene å fordøye. Til slutt observeres det med mikroskopet.

På den annen side er KOH i form av en aktuell løsning effektiv i behandling av vorter..
I den kosmetiske industrien
Den brukes i noen rengjøringsprodukter for negler, barberkremer og såper, ettersom den etsende egenskapen gjør den veldig effektiv i spaltning eller fjerning av bløtvev og hårfjerning..

I landbruket
Den brukes i gjødsel og andre landbruksprodukter som herbicider og plantevernmidler.
I industrielle kjemiske prosesser
KOH er nyttig i rengjøringsoperasjoner og i vask eller rensing av industrigasser, spesielt når syrefjerning er nødvendig..
For eksempel på grunn av den enkle reaksjonen med COto, den brukes til å absorbere denne gassen. I tillegg er den ideell for å reagere med syrer, og det er derfor den brukes til å fjerne hydrogensulfid (HtoS). Og på samme måte for å fjerne nitrogenoksider.

I næringsmiddelindustrien
Den brukes til å justere pH, som en stabilisator og som et fortykningsmiddel i næringsmiddelindustrien.
Det har blitt vurdert av US Food and Drug Administration, eller FDA. Food and Drug Administration), som en direkte ingrediens i menneskelig mat, forutsatt at den brukes under forhold knyttet til god fremstillingspraksis.
Ved å skaffe biodiesel
Biodiesel er en erstatning for flytende drivstoff for diesel eller diesel. Det er hentet fra vegetabilske oljer eller animalsk fett. KOH har blitt brukt som katalysator i produksjonen av biodiesel.
Nylige studier
I flere år har det vært rettet oppmerksomhet mot forurensning av havene med plastavfall, som påvirker mer enn 550 arter av marine fauna, både ved å innta plast og ved å bli fanget i avfallet..
Av denne grunn blir det forsøkt å finne metoder som tillater bearbeiding av prøver fra fordøyelseskanalen til dyr, oppløsende det organiske materialet, men uten å løse opp plasten som prøvene inntar..
I denne forstand har det blitt funnet at bruk av KOH-løsninger for å skille plast fra organisk materiale er en praktisk og effektiv metode, som kan være veldig nyttig i kvantitative studier av inntak av plast av vill marine fauna..
Referanser
- Mahmoud A. Ghannoum og Nancy C. Isham. (2009). Dermatofytter og dermatofytoser. I klinisk mykologi. Andre utgave. Gjenopprettet fra sciencedirect.com.
- Kühn, S. et al. (2016). Bruk av kaliumhydroksid (KOH) løsning som en passende tilnærming for å isolere plast inntatt av marine organismer. I Marine Pollution Bulletin. Gjenopprettet fra sciencedirect.com.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Kirk-Othmer (1994). Encyclopedia of Chemical Technology. Volum 19. Fjerde utgave. John Wiley & Sons.
- Ullmann's Encyclopedia of Industrial Chemistry. (1990). Femte utgave. Volum A22. VCH Verlagsgesellschaft mbH.
- National Library of Medicine. (2019). Kaliumhydroksyd. Gjenopprettet fra: pubchem.ncbi.nlm.nih.gov
- Krisada Noiroj, et al. (2009). En komparativ studie av KOH / AltoELLER3 og KOH / NaY-katalysatorer for produksjon av biodiesel via omestring fra palmeolje. I fornybar energi. Gjenopprettet fra sciencedirect.com.



Ingen har kommentert denne artikkelen ennå.