
Rasemisk blanding av kiralitet, eksempler

EN rasemisk blanding eller racemat er en sammensatt av to enantiomerer i like deler og som derfor er optisk inaktiv. Denne optiske aktiviteten refererer til mulighetene til løsningene for å rotere, med eller mot klokken, en stråle av polarisert lys som beveger seg gjennom dem i en retning..
En enantiomer har evnen til å rotere polarisert lys, for eksempel til venstre (venstrehendt), så den rene løsningen vil være optisk aktiv. Imidlertid, hvis enantiomeren som roterer lyset mot høyre (dekstroterende) begynner å bli lagt til den, vil dens optiske aktivitet reduseres til den inaktiveres..

Når dette skjer, sies det at det er like store mengder av venstre og høyre enantiomer; Hvis et molekyl roterer det polariserte lyset til venstre, vil dets effekt umiddelbart bli kansellert når det "snubler" med et annet molekyl som roterer det til høyre. Og så videre. Derfor vil vi ha en rasemisk blanding.
Den første observasjonen av enantiomerisme ble gjort av den franske kjemikeren Louis Pasteur i 1848, som studerte en blanding av enantiomere krystaller av vinsyre (på den tiden kalt raceminsyre). Da denne syren kom fra druene som ble brukt til å lage viner, ble denne blandingen tilført generelt på alle molekyler.
Artikkelindeks
- 1 Sko og chirality
- 2 Eksempler
- 2.1 Vinsyre
- 2.2 kinin
- 2.3 Talidomid
- 2,4 1,2-epoksypropan
- 2,5 1-fenyletylamin
- 2.6 Avsluttende kommentar
- 3 Referanser
Sko og chirality
For det første, for at det skal være en racemisk blanding, må det være to enantiomerer (vanligvis), noe som betyr at begge molekylene er chirale, og at speilbildene deres ikke er overliggende. Et par sko illustrerer dette perfekt: uansett hvor hardt du prøver å legge den venstre skoen til høyre, vil de aldri kunne passe..
Den høyre skoen, for å si, avbøyer det polariserte lyset til venstre; mens den venstre skoen gjør det til høyre. I en hypotetisk løsning der skoene er molekylene, hvis det bare er rette, chirale sko, vil dette være optisk aktivt. Det samme vil skje hvis det bare er igjen sko i løsningen.
Imidlertid, hvis det er tusen venstre sko blandet med tusen høyre sko, så har vi en racemisk blanding, som også er optisk inaktiv, siden avvikene som lyset på innsiden avbryter hverandre..
Hvis de i stedet for sko var baller, gjenstander som er achirale, ville det være umulig for racemiske blandinger av disse å eksistere, siden de ikke engang kunne eksistere som par enantiomerer..
Eksempler
Vinsyre
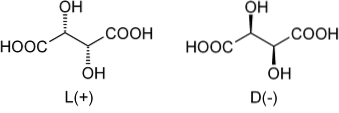
Når vi kom tilbake til vinsyre, var dens racemiske blanding den første som ble kjent. På det øvre bildet vises de to enantiomerene, hver i stand til å danne krystaller med morfologiske "venstre" eller "høyre" ansikter. Pasteur lyktes ved hjelp av et mikroskop og en streng innsats å skille disse enantiomere krystallene fra hverandre..
Krystallene til L (+) og D (-) enantiomerer viser separat optisk aktivitet ved å avbøye polarisert lys til henholdsvis høyre eller venstre. Hvis begge krystaller i like molære proporsjoner oppløses i vann, oppnås en optisk inaktiv racemisk blanding..
Merk at begge enantiomerene har to chirale karbonatomer (med fire forskjellige substituenter). I L (+) ligger OH-ene bak planet dannet av karbonskjelettet og COOH-gruppene; mens i D (-) er disse OH-ene over nevnte plan.
De som syntetiserer vinsyre vil få en racemisk blanding. For å skille L (+) enantiomeren fra D (-), er en chiral oppløsning nødvendig, hvor denne blandingen reageres med en chiral base for å produsere diastereoisomere salter, som er i stand til å bli separert senere ved fraksjonell krystallisering..
Kinin

I eksemplet ovenfor, for å referere til en racemisk blanding av vinsyre, blir det vanligvis skrevet som (±) -vinsyre. I tilfelle kinin (øvre bilde) vil det være (±) -kinin.
Kinomerens isomerisme er kompleks: den har fire chirale karbonatomer, som gir opphav til seksten diastereoisomerer. Interessant, to av dens enantiomerer (den ene med OH over flyet og den andre under den), er egentlig diastereoisomerer, siden de skiller seg ut i konfigurasjonene til de andre chirale karbonene (de fra bicyclo med N-atomet).
Imidlertid er det vanskelig å bestemme hvilken av stereoisomerer av kinin som vil avbøye polarisert lys til høyre eller til venstre..
Talidomid
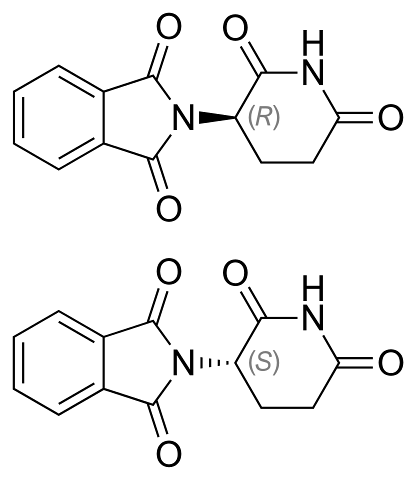
Enantiomerene av talidomid er vist ovenfor. Den har bare ett chiralt karbon: det som er knyttet til nitrogenet som forbinder begge ringene (en av ftalimid og den andre av gluteramid).
I R enantiomeren (med beroligende egenskaper) er ftalimidringen (den til venstre) orientert over planet; mens du er i S enantiomeren (med mutagene egenskaper), nedenfor.
Det er ikke kjent for øyeprosenten hvilken av de to som avbøyer lyset til venstre eller høyre. Det som er kjent er at en 1: 1 eller 50% blanding av begge enantiomerer danner den racemiske blandingen (±) -talidomid.
Hvis du bare vil markedsføre talidomid som et hypnotisk beroligende middel, er det obligatorisk å underkaste dets racemiske blanding den allerede nevnte chirale oppløsningen, på en slik måte at den rene R-enantiomeren oppnås..
1,2-epoksypropan
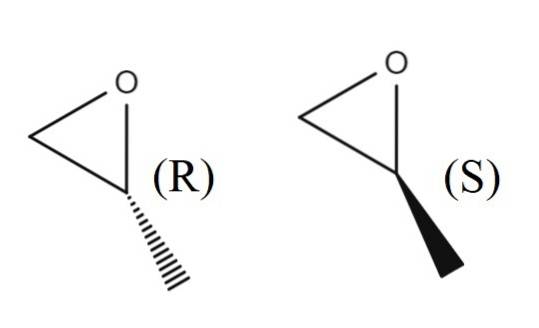
På det øvre bildet har du enantiomerparet 1,2-epoxypropane. R-enantiomeren avbøyer polarisert lys til høyre, mens S-enantiomeren avbøyer det mot venstre; det vil si at den første er (R) - (+) - 1,2-epoxypropane, og den andre er (S) - (-) - 1,2-epoxypropane.
Den racemiske blandingen av de to, igjen, i forholdet 1: 1 eller 50%, blir (±) -1,2-epoksypropan.
1-fenyletylamin
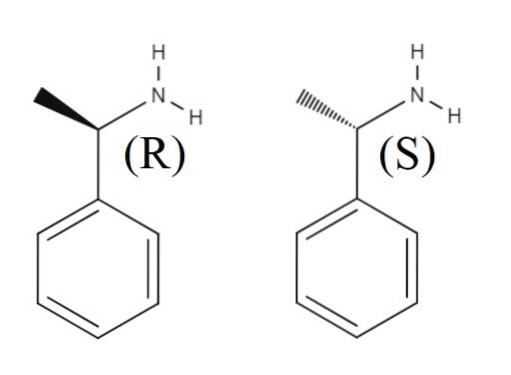
Ovenfor er en annen racemisk blanding dannet av de to enantiomerene av 1-fenyletylamin. R-enantiomeren er (R) - (+) - 1-fenyletylamin, og S-enantiomeren er (S) - (-) - 1-fenyletylamin; man har metylgruppen, CH3, peker ut av den aromatiske ringens plan, og den andre peker under den.
Merk at når konfigurasjonen er R, sammenfaller det noen ganger med det faktum at enantiomeren roterer det polariserte lyset mot høyre; det gjelder imidlertid ikke alltid og kan ikke tas som en generell regel.
Endelig kommentar
Viktigere enn at racemiske blandinger eksisterer eller ikke, er deres chirale oppløsning. Dette gjelder spesielt forbindelser med farmakologiske effekter som er avhengige av nevnte stereoisomerisme; det vil si at en enantiomer kan være gunstig for pasienten, mens den andre kan påvirke den.
Det er derfor disse chirale oppløsninger brukes til å skille de racemiske blandingene inn i komponentene, og dermed kunne markedsføre dem som rene stoffer uten skadelige urenheter..
Referanser
- Morrison, R. T. og Boyd, R, N. (1987). Organisk kjemi. 5. utgave. Redaksjonell Addison-Wesley Interamericana.
- Carey F. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- Graham Solomons T.W., Craig B. Fryhle. (2011). Organisk kjemi. Amines. (10. utgave.). Wiley pluss.
- Steven A. Hardinger. (2017). Illustrert ordliste for organisk kjemi: rasemisk blanding. Institutt for kjemi og biokjemi, UCLA. Gjenopprettet fra: chem.ucla.edu
- Nancy Devino. (2019). Racemic Blanding: Definisjon & Eksempel. Studere. Gjenopprettet fra: study.com
- James Ashenhurst. (2019). Stereokjemi og kiralitet: Hva er en racemisk blanding? Gjenopprettet fra: masterorganicchemistry.com
- John C. Leffingwell. (2003). Kiralitet og bioaktivitet I.: Farmakologi. [PDF]. Gjenopprettet fra: leffingwell.com



Ingen har kommentert denne artikkelen ennå.