
Hva er karyolyse?
De karyolyse er en av endringene som identifiseres i cellens kjerner når de dør som følge av noxa eller ytre skader, for eksempel på grunn av hypoksi (utilstrekkelig oksygentilførsel) eller giftige stoffer.
Navnet stammer fra det greske karyon, som betyr "kjerne" og lysis, som kan tolkes som "dempning" eller oppløsning "; derfor betyr begrepet karyolyse bokstavelig talt "utslipp av kjernen".
Dette fenomenet oppstår under nekrofanerosestadiet, slik som pyknose og karyorrhexis, og kan være den eneste kjernefysiske endringen eller være inkludert i et kontinuum som begynner med pyknosis, går gjennom karyorrhexis og ender i karyolyse..
Som ved karyorrhexis, kommer kjerneforandringen forut for de cytoplasmatiske endringene, og prosessen som helhet er ledsaget av betennelse i den ekstracellulære matrisen, noe som er karakteristisk for nekrose, og som kan betraktes som en grunnleggende forskjell med apoptose, der ingen er det inflammatoriske komplement.
Karyolyse oppstår på grunn av virkningen av nukleære enzymer som under normale forhold hjelper med å koble av og fragmentere DNA slik at det kan transkriberes, men at det i tilstander med celledød på grunn av noxa (nekrose) begynner å oppløses kjernen i sin helhet.
Artikkelindeks
- 1 Atomenzymer
- 1.1 Klassifisering av nukleare enzymer
- 2 Typer nukleaser
- 2.1 Endonukleaser
- 2.2 Begrensningsendonukleaser
- 2.3 Eksonukleaser
- 3 Patofysiologi av karyolyse
- 4 Funn ved lysmikroskopi
- 5 Referanser
Nukleare enzymer
Enzymer i cellekjernen er flere og veldig spesifikke, og er avgjørende for fysiologien til DNA og RNA.
Siden gener og kromosomer er strukturert og danner kromatin, er det praktisk talt umulig for DNA-transkripsjon og replikering å finne sted, siden det er en kontinuerlig kjede, ekstremt lang og med en svært kompleks tredimensjonal romlig konformasjon..
For å lette replikerings- og transkripsjonsprosessen, "kutter" kjernenezymer DNA-fragmentet som skal transkriberes, slik at RNA kan kobles til en lineær kjede av deoksyribonukleinsyre med en veldig klar start og slutt..
Også kjent som "fosfodiesteraser", er kjernenezymer i stand til å spalte fosfodiesterbindinger, viktige deler i strukturen til nukleinsyrer, og regulerer også intracellulære nivåer av syklisk AMP og GMP.
Klassifisering av nukleare enzymer
Avhengig av stedet der endonukleaser utøver sin effekt, klassifiseres de i to brede kategorier: nukleaser og ligaser..
Inntil nå har virkningene av nukleaseenzymer, som er ansvarlige for å "skjære" biter av DNA for å tillate replikasjon, blitt beskrevet omtrent, men når transkripsjonen av et DNA-fragment er fullført, må det integreres på nytt i den store strengen av deoksyribonukleinsyre som den tilhører, og også å gjøre det i en bestemt posisjon.
Det er her "ligasene" spiller inn, enzymer som er i stand til å "stikke" i stedet en DNA-kjede som tidligere er spaltet av fosfodiesteraser..
Den delikate balansen mellom nukleaser og ligaser gjør at genetisk materiale kan opprettholdes, slik at når det ene enzymets aktivitet overstiger det andre, kan det forutsies problemer.
Typer nukleaser
For å forstå rollen som fosfodiesterase i karyolyse, er det viktig å kjenne til de forskjellige typene som eksisterer, siden de er ansvarlige for hele prosessen.
I denne forstand har ligasene praktisk talt ingen rolle, faktisk blir aktiviteten deres kansellert, noe som gjør det umulig å reversere prosessen initiert av nukleasene..
I følge nettstedet der de utøver sin handling, er nukleaser således delt inn i:
- Endonukleaser
- Exonukleaser
- Begrensning endonukleaser
I tillegg til enzymene som er i stand til å spalte DNA (også kjent som DNaser), er det i kjernen også enzymer med evnen til å "kutte" og modellere RNA-segmenter, disse er kjent som ribonukleaser eller RNaser..
Selv om disse enzymene er viktige i cellens normale fysiologi, spiller de under nekrose-prosessen en sekundær rolle..
Endonukleaser
Endonukleaser er enzymer som er i stand til å skjære DNA-kjeder vekk fra den frie enden, det vil si at de er i stand til å skille DNA når som helst i kjeden.
Endonukleaser kan kutte DNA tilfeldig i hvilken som helst region uten å matche en bestemt nukleotidsekvens.
Begrensning endonukleaser
Restriksjonsendonukleaser er en veldig spesiell type endonukleaser som er i stand til å identifisere en spesifikk sekvens av baser for å kutte DNA-kjeden på det spesifikke punktet..
De er klassifisert i tre grupper: Type I, Type II og Type III.
Type I restriksjonsendonukleaser krever ATP for å fungere (og dermed forbruke energi) og er i stand til å spalte opptil 1000 basepar fra gjenkjenningssekvensen.
For sin del er Type II den enkleste versjonen av restriksjonsendonukleaser; i en prosess som ikke krever energi, er disse enzymene i stand til å kutte DNA i variable lengder fra restriksjonssekvensen.
Til slutt kutter Type III-restriksjonsendonukleaser, i en prosess som også bruker energi (ATP), DNA-kjeden i små fragmenter som ikke overstiger 25 basepar fra gjenkjenningspunktet (restriksjon).
Exonukleaser
Til slutt er exonukleaser de enzymene som er i stand til å kutte DNA fra en fri ende av kjeden, det vil si at de er spesialiserte enzymer i lineære DNA-kjeder som tidligere ble spaltet av endonukleaser..
Således refererer begrepet ENDOnuclease til enzymets evne til å kutte DNA-strengen inni (ENDO = innsiden), mens EXOnuclease indikerer at enzymet bare kan kutte DNA i den frie enden (EXO = utenfor).
Den synkroniserte og harmoniske aktiviteten til alle disse enzymene tillater komplekse prosesser med genetisk replikasjon og transkripsjon; Imidlertid taper denne balansen under nekrose, og DNA begynner å fragmentere til bare de frie og uorganiserte basiske komponentene er igjen, noe som er synonymt med celledød..
Patofysiologi av karyolyse
Å vite det store antallet enzymer som er tilstede i kjernen, så vel som måten de utøver sin funksjon på, er det ikke vanskelig å utlede patofysiologien til karyolyse..
Alt begynner som et tap av homeostase mellom nukleaseenzymer og ligaser, effekten av sistnevnte blir langt overgått av førstnevnte; det vil si at mer DNA blir ødelagt enn det som kan repareres.
I første omgang kutter endonukleaser en lang DNA-kjede i små fragmenter, som deretter reduseres ytterligere av andre endonukleaser..
Til slutt lyseres de kortere fragmentene fra endene av eksonukleasene til det ikke er spor av organisert kjernefysisk materiale, som ble enzymatisk nedbrutt..
Funn ved lysmikroskopi
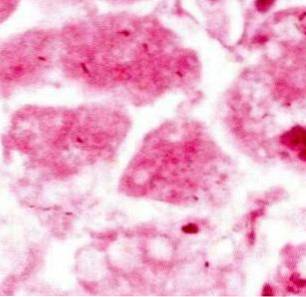
I lysmikroskopi virker celler som har gjennomgått karyolyse helt rosa (eosinofiler), noe som gjør det umulig å identifisere kjernefysisk materiale farget lilla.
I noen tilfeller kan det sees en unnvikende flekk eller "spøkelse" i området der cellekjernen en gang var, men generelt vil den dominerende fargen være rosa, fordi det ikke er flere organiserte kjernefysiske strukturer som er i stand til å fange hematoksylin..
Referanser
- Van Cruchten, S., & Van Den Broeck, W. (2002). Morfologiske og biokjemiske aspekter av apoptose, onkose og nekrose. Anatomi, histologi, embryologi, 31(4), 214-223.
- Parafiniuk, M. (1998). Fenomen av karyolyse ved cytofotomorfometriske undersøkelser. I Annales Academiae Medicae Stetinensis (s. 1-87).
- Tolbert, P. E., Shy, C. M., & Allen, J. W. (1992). Mikrokjerner og andre kjernefysiske anomalier i bukkale utstryk: utvikling av metoder. Mutasjonsforskning / miljømutagenese og relaterte emner, 271(1), 69-77.
- Levin, S., Bucci, T. J., Cohen, S. M., Fix, A. S., Hardisty, J. F., Legrand, E. K., ... & Trump, B. F. (1999). Nomenklaturen for celledød: anbefalinger fra en ad hoc-komité fra Society of Toxicologic Pathologists. Toksikologisk patologi, 27(4), 484-490.
- Zabiti, S. (2002). Endring av ionisk homeostase under metabolsk hypoksi-indusert celleskade. Rollen til monovalente ioner (Doktoravhandling, Universitetet i Granada).

Ingen har kommentert denne artikkelen ennå.