
Jodidperoksidasegenskaper, struktur, funksjoner
De jodidperoksidase o skjoldbruskkjertelperoksidase (TPO) er et hem-glykoprotein som tilhører familien av peroksidaser fra pattedyr (som myeloperoksidase, laktoperoksidase og andre) som deltar i skjoldbruskhormonsynteseveien.
Dens viktigste funksjon er "jodering" av tyrosinrester i tyroglobulin, og dannelsen av 3-3'-5-triiodothyronin (T3) og tyroksin (T4) gjennom en "koblings" -reaksjon. Intramolekylær av joderte tyrosiner.
Triiodothyronine og tyroksin er to hormoner produsert av skjoldbruskkjertelen som har viktige funksjoner i pattedyrs utvikling, differensiering og metabolisme. Virkningsmekanismen avhenger av samspillet mellom dets nukleære reseptorer og spesifikke gensekvenser av målgenene..
Eksistensen av enzymet jodidperoksidase ble bekreftet på 1960-tallet av forskjellige forfattere, og det er nå gjort betydelige fremskritt med å bestemme strukturen, funksjonene og egenskapene til genet som koder det i forskjellige organismer..
I mye av litteraturen relatert til dette enzymet, er det kjent som det mikrosomale "autoantigenet" og er relatert til noen autoimmune skjoldbruskkjertelsykdommer..
Takket være de immunogene egenskapene er dette enzymet et mål- eller målmolekyl for antistoffene som er tilstede i serum hos mange pasienter med skjoldbruskpatologier, og dets mangler kan føre til hormonelle mangler som kan være viktige patofysiologisk sett..
Artikkelindeks
- 1 Funksjoner
- 1.1 Regulering av uttrykk
- 2 Struktur
- 3 funksjoner
- 3.1 Hva er syntesen av skjoldbruskhormon?
- 4 Relaterte sykdommer
- 5 Referanser
Kjennetegn
Jodidperoksidase er kodet av et gen som ligger på kromosom 2 hos mennesker, som måler mer enn 150 kbp og består av 17 eksoner og 16 introner..
Dette transmembrane proteinet, med et enkelt segment nedsenket i membranen, er nært beslektet med myeloperoksidase, som det deler mer enn 40% aminosyresekvenslikhet med..
Syntesen forekommer i polyribosomer (et sett med ribosomer som er ansvarlig for oversettelsen av det samme proteinet) og blir deretter satt inn i membranen i det endoplasmatiske retikulumet, hvor det gjennomgår en prosess med glykosylering.
Når jodidperoksidas er syntetisert og glykosylert, blir den transportert til den apikale polen av thyrocytter (skjoldbruskkjertelceller eller skjoldbruskkjertelceller), hvor den er i stand til å eksponere sitt katalytiske sentrum for skjoldbruskkjertelen..
Regulering av uttrykk
Ekspresjon av genet som koder for skjoldbruskperoksydase eller jodidperoksidase styres av skjoldbrusk-spesifikke transkripsjonsfaktorer som TTF-1, TTF-2 og Pax-8.
De genetiske elementene som tillater økning eller forbedring av ekspresjonen av dette genet hos mennesker er beskrevet i regionene som flankerer 5'-enden av det, vanligvis mellom de første 140 baseparene i denne "flankerende" regionen..
Det er også elementer som undertrykker eller reduserer ekspresjonen av dette proteinet, men i motsetning til "enhancers" har disse blitt beskrevet nedstrøms for gensekvensen..
Mye av reguleringen av den genetiske ekspresjonen av jodidperoksidase skjer på en vevsspesifikk måte, og dette avhenger av virkningen av DNA-bindende elementer som virker på cis, slik som TTF-1 transkripsjonsfaktorer og andre.
Struktur
Dette proteinet med enzymatisk aktivitet har rundt 933 aminosyrerester og en ekstracellulær C-terminal ende på 197 aminosyrer som kommer fra ekspresjon av andre genmoduler som koder for andre glykoproteiner..
Molekylvekten er rundt 110 kDa og er en del av gruppen av type 1 glykosylerte transmembrane proteiner, siden den har et glykosylert transmembransegment og en hemgruppe på sitt aktive sted..
Strukturen til dette proteinet har minst en disulfidbro i det ekstracellulære området som danner en karakteristisk lukket sløyfe som er utsatt på overflaten av tyrocytter..
Funksjoner
Den viktigste fysiologiske funksjonen til jodidperoksidase er relatert til dens deltakelse i syntesen av skjoldbruskkjertelhormon, der den katalyserer "jodering" av tyrosinrester av monoiodotyrosin (MIT) og diiodotyrosin (DIT), i tillegg til koblingen av jodotyrosinrester i thyroglobulin.
Hva er syntesen av skjoldbruskhormon?
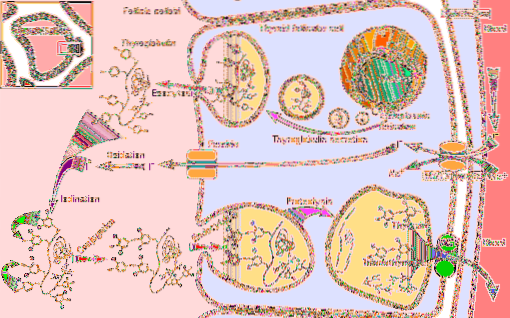
For å forstå funksjonen til skjoldbruskkjertelperoksidaseenzymet, er det nødvendig å vurdere trinnene for hormonsyntese der det deltar:
1-Det begynner med transport av jodid til skjoldbruskkjertelen og fortsetter med
2-Generering av et oksidasjonsmiddel som hydrogenperoksid (H2O2)
3-Deretter syntetiseres et reseptorprotein, tyroglobulin
4-Jodidet oksyderes til en høyere valens tilstand og deretter
5-jodid binder seg til tyrosinrester som er tilstede i tyroglobulin
6-I tyroglobulin dannes jodtyroniner (en type skjoldbruskhormoner) ved kobling av rester av jodotyrosin
7-tyroglobulin lagres og spaltes
8-Jod fjernes fra de frie jodotyrosinene og til slutt,
9-tyroksin og trijodtyronin frigjøres i blodet; Disse hormonene utøver sine effekter ved å samhandle med deres spesifikke reseptorer, som er lokalisert på kjernemembranen og som er i stand til å samhandle med mål-DNA-sekvenser, og fungerer som transkripsjonsfaktorer..
Som det kan utledes av kunnskapen om funksjonene til de to hormonene i hvis syntese den deltar (T3 og T4), har jodidperoksidase viktige implikasjoner på det fysiologiske nivået..
Mangelen på begge hormonene under menneskelig utvikling gir mangler i vekst og mental retardasjon, samt metabolske ubalanser i voksenlivet.
Beslektede sykdommer
Jodidperoksidase er en av de viktigste autoantigenene i skjoldbruskkjertelen hos mennesker og er assosiert med komplement-systemmediert cytotoksisitet. Dens funksjon som et autoantigen fremheves hos pasienter med autoimmune skjoldbruskkjertelsykdommer.
Urinsyregikt, for eksempel, skyldes mangel på jodinnhold under hormonsyntese i skjoldbruskkjertelen, som igjen har vært relatert til mangel på jodering av tyroglobulin som et resultat av visse mangler i jodidperoksidase..
Noen karsinomer er preget av å ha endrede jodidperoksidasefunksjoner, det vil si aktivitetsnivået til dette enzymet er betydelig lavere enn hos ikke-kreftpasienter..
Imidlertid har studier bekreftet at det er en svært variabel karakteristikk, som ikke bare avhenger av pasienten, men også av krefttypen og de berørte regionene..
Referanser
- Degroot, L. J., & Niepomniszcze, H. (1977). Biosyntese av skjoldbruskkjertelhormon: grunnleggende og kliniske aspekter. Fremgang innen endokrinologi og metabolisme, 26(6), 665-718.
- Fragu, P., & Nataf, B. M. (1976). Human skjoldbruskperoksidaseaktivitet ved godartede og ondartede skjoldbruskforstyrrelser. Det endokrine samfunnet, Fire fem(5), 1089-1096.
- Kimura, S., og Ikeda-saito, M. (1988). Menneskelig myeloperoksidase og skjoldbruskkjertelperoksidase, to enzymer med separate og distinkte fysiologiske funksjoner, er evolusjonært relaterte medlemmer av samme genfamilie. Proteiner: Struktur, funksjon og bioinformatikk, 3, 113-120.
- Nagasaka, A., Hidaka, H., & Ishizuki, Y. (1975). Studier på humant jodidperoksidase: dens aktivitet i forskjellige skjoldbruskforstyrrelser. Chimica Acta Clinic, 62, 1-4.
- Ruf, J., & Carayon, P. (2006). Strukturelle og funksjonelle aspekter av skjoldbruskkjertelperoksidase. Arkiv for biokjemi og biofysikk, 445, 269-277.
- Ruf, J., Toubert, M., Czarnocka, B., Durand-gorde, M., Ferrand, M., & Carayon, P. (2015). Forholdet mellom immunologisk struktur og biokjemiske egenskaper av menneskelig skjoldbruskkjertelperoksidase. Endokrine anmeldelser, 125(3), 1211-1218.
- Taurog, A. (1999). Molekylær utvikling av skjoldbruskkjertelperoksidase. Biochimie, 81, 557-562.
- Zhang, J., & Lazar, M. A. (2000). Virkningsmekanismen for skjoldbruskhormoner. Annu. Pastor Physiol., 62(1), 439-466.



Ingen har kommentert denne artikkelen ennå.