
Sodium bisulfite (NaHSO3) struktur, egenskaper, bruksområder, produksjon

De natriumbisulfitt er et uorganisk fast stoff dannet av et natriumion Na+ og et bisulfittion HSO3-. Den kjemiske formelen er NaHSO3. Det er et hvitt krystallinsk fast stoff, og på grunn av dets antioksidantegenskaper blir det mye brukt som et matkonserveringsmiddel (for eksempel i noen syltetøy).
NaHSO3 det er en reduserende kjemisk forbindelse, som er det motsatte av oksidant, og av den grunn fungerer det som en antioksidant i mange av dets applikasjoner, for eksempel i spiselige produkter, da det forhindrer deres forringelse.

Imidlertid har denne bruken blitt stilt spørsmålstegn ved at det er rapportert om tilfeller av astma hos mennesker etter at de har spist mat som inneholder natriumbisulfitt. Det sies til og med å ødelegge vitamin B1 i disse.
Internasjonale helseorganisasjoner har begrenset bruken til mikromengder i mat.
Imidlertid har natriumbisulfitt mange andre bruksområder, for eksempel for å skaffe jod, som et antiinfeksjonsmiddel, for å bleke vev, for fordøyelse av tre under tilberedning av papirmasse, som et desinfeksjonsmiddel for øl og vinfat..
Artikkelindeks
- 1 Kjemisk struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Tetthet
- 3.5 Løselighet
- 3,6 pH
- 3.7 Kjemiske egenskaper
- 3.8 Risiko
- 4 Motta
- 5 bruksområder
- 5.1 I masse- og papirindustrien
- 5.2 I næringsmiddelindustrien
- 5.3 Kontrovers over bruken i mat
- 5.4 I landbruksapplikasjoner
- 5.5 Ved å skaffe jod
- 5.6 I møbel- og treindustrien
- 5.7 I forskjellige applikasjoner
- 6 Referanser
Kjemisk struktur
Sodium bisulfite består av en natriumkation Na+ og et bisulfittanion HSO3-.
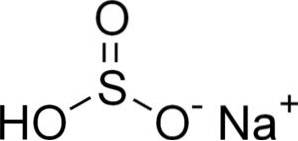
I vandige oppløsninger danner bisulfitt 4 arter. I fortynnet løsning er det en balanse mellom strukturene vist nedenfor:
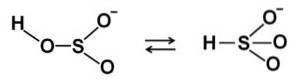
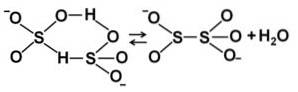
Når konsentrasjonen øker, samhandler to bisulfittmolekyler med hverandre og danner pyrosulfittionen StoELLER5to-:
Nomenklatur
-Natriumbisulfitt
-Sodium hydrogensulfitt
-Natriumhydrosulfitt.
Eiendommer
Fysisk tilstand
Solid hvit krystallinsk.
Molekylær vekt
104,06 g / mol
Smeltepunkt
Det nedbrytes.
Tetthet
1,48 g / cm3 ved 20 ºC.
Løselighet
Løselig i vann: 29 g / 100 g vann.
pH
Dens løsninger er sure, med en pH mellom 2,5 og 5,5.
Kjemiske egenskaper
I vandig løsning natriumbisulfitt NaHSO3 skiller seg inn i ionene: natriumkationen Na+ og bisulfittanion HSO3-.
Hvis natriumbisulfitt utsettes for luft, mister den noe SOto og oksiderer sakte til Na-sulfattoSW4.
Hvis det oppvarmes til nedbrytning, avgir det røyk av svoveloksider og natriummonoksid..
Det er et reduksjonsmiddel, som er det motsatte av oksidant. Og av denne grunn kan det oppføre seg som en antioksidant.
Det har en svak lukt av svovel. Det er ikke brannfarlig.
Risiko
NaHSO natriumbisulfitt3 det er sterkt irriterende for hud og vev. Støv irriterer øynene, nesen og halsen. Ved svelging irriterer det magen. Store doser kan forårsake voldsom kolikk, diaré, depresjon og død..
Det er ikke brennbart, men ved oppvarming produserer det irriterende og giftige gasser.
Å skaffe
Den fremstilles ved å mette en natriumkarbonatoppløsning NatoCO3 med svoveldioksid SOto og krystalliserer i oppløsning.
applikasjoner
I masse- og papirindustrien
NaHSO3 Den brukes i fordøyelsen av tre, slik at den senere kan bli papir. Den fungerer også som en blekemasse.
Det brukes også til å fjerne klor når papirmasse er blitt bleket med det..
I næringsmiddelindustrien
Sodium bisulfite fungerer på grunn av sin reduserende egenskap som en antioksidant.
Det brukes som konserveringsmiddel i et stort antall matvarer og drikkevarer, inkludert vin og øl, for å forhindre ødeleggelse og forbedre smak.
Den brukes til å bleke matvarer, for eksempel visse spiselige stivelser.
Det reduserer eller forhindrer matsvinn, tillater kondisjonering av deigen som brukes i bakevarer og tjener til å myke maiskjernene under våtmaling, blant annet.
I tillegg til å kontrollere gjæringen av vin og øl, fungerer den som et antiseptisk middel i preparatet, da det fungerer som sterilisator og soppdrepende middel i fat og kar..

I tørket frukt finnes det i konsentrasjoner over 100 ppm (ppm betyr "deler per million"), i mange andre matvarer finnes det i konsentrasjoner mellom 10 og 100 ppm, for eksempel frosne og tørkede poteter, sylteagurk, sauser og syltetøy.

Kontrovers over bruken i mat
Det har vært noe bekymring for både de umiddelbare og langsiktige toksiske effektene av natriumbisulfitt i mat. Det er divergerende meninger.
Det er rapportert om bivirkninger hos pasienter med astma, som er en luftveissykdom, etter inntak av mat med NaHSO3. Andre kilder indikerer at bisulfittionen kan ødelegge vitamin B1 eller tiamin.

Imidlertid fant visse forskere i 1985 at natriumbisulfitt tjener til å beskytte mot stråling og kjemiske midler, og hemmer eller forhindrer transformasjon av celler mot kreft. Lave doser er de beste.
Denne beskyttende effekten har blitt forklart basert på dens reduserende eller antioksidantegenskaper og at den på denne måten kan angripe frie radikaler.
På den annen side, Verdens helseorganisasjon, eller WHO (for forkortelsen på engelsk Verdens Helseorganisasjon), anbefaler som et akseptabelt nivå av daglig inntak ca 0,7 mg / kg av personens vekt.
Det betyr at det anbefales at du ikke overskrider den mengden..
United States Food and Drug Administration, eller USFDA. US Food and Drug Administration), klassifisert natriumbisulfitt som "generelt anerkjent som trygt".
I landbruksapplikasjoner
NaHSO brukt i lave konsentrasjoner3 fungerer som en plantevekstregulator for å forbedre fotosyntese og fremme avling.
Det er testet for dette formålet i forskjellige typer planter, for eksempel jordbær og teplanter..

Det er den aktive ingrediensen i mange plantevernmidler og biocider.
I vannmiljøer kan det også akselerere transformasjonen av visse herbicider til mindre giftige produkter ved å eliminere klor..
Ved å skaffe jod
NaHSO3 er den reduserende forbindelsen som brukes til å frigjøre jod fra natriumjodat NaIO3. Dette er en av måtene å få jod fra kilder som nitro fra Chile eller noe saltvann.
Etter krystallisering av natriumnitratet fra den rå Chile-nitratløsningen gjenstår en NaIO-løsning3 som behandles med natriumbisulfitt NaHSO3, genererer gratis jod.
2 NaIO3 + 5 NaHSO3 → 3 NaHSO4 + NatoSW4 + Jegto
I møbel- og treindustrien
NaHSO3 Det er testet for å modifisere soyaproteiner og forbedre deres klebeegenskaper med tre for å lime trebiter sammen for å forberede for eksempel sponplater, papp eller papier-mache, kryssfiner, etc. Alt dette for møbler eller tavler, blant forskjellige bruksområder.

Dette er gjort for å erstatte tradisjonelle formaldehydbaserte lim fordi både i fremstillingsprosessen og under bruk har de en tendens til å frigjøre formaldehyd i atmosfæren, som er en giftig forbindelse..
Sodium bisulfite forbedrer faststoffinnholdet i soyaproteinlimet, og reduserer viskositeten, forbedrer flytbarheten slik at den bedre trenger inn i porene i treet, og øker kohesjonen med den og mellom stykkene..
NaHSO-modifisert soyaproteinlim3 har god vannbestandighet og utmerket lagringsstabilitet på grunn av antioksidantvirkningen av natriumbisulfitt.
Dette bekrefter at NaHSO-modifiserte soyaproteinlim3 er sammenlignbare med formaldehydbaserte lim og kan brukes i møbel- og treindustrien, fordi de er mindre forurensende.
I forskjellige applikasjoner
Den har flere bruksområder, vanligvis basert på reduserende egenskaper (som er det motsatte av oksidant). Her er noen applikasjoner.
-I fotografering.
-Ved skinngarvning for å fjerne hår fra huder.
-Terapeutiske bruksområder: anti-smittsom. Det brukes som en antioksidant i noen øyedråper.
-Ved utvinning av naturgass ved hydraulisk brudd.
-Ved farging av fibre brukes den til fremstilling av varme eller kalde badekar, for å oppløse visse fargestoffer eller fargestoffer.
-Som reduksjonsmiddel for tøy eller bleking for å bleke ull, silke og vegetabilske fibre.
-I kjemilaboratorier for å fjerne permanganatflekker fra hud og klær. I biokjemilaboratorier som konserveringsmiddel for væsker eller løsninger som kan forverres over tid. Som et kjemisk reagens.
-For koagulering av gummilatex.
-I den kosmetiske industrien som en antioksidant.
-Desinfeksjonsmiddel og blekemiddel.
-Ved behandling av avløpsvann for å eliminere klor som ble brukt i siste desinfiseringsfase og for å tømme det allerede behandlede vannet til miljøet.

Referanser
- OSS. National Library of Medicine. (2019). Natriumbisulfitt. Gjenopprettet fra pubchem.ncbi.nlm.nih.gov.
- Qi, G. et al. (2013). Vedheft og fysisk-kjemiske egenskaper av soyaprotein modifisert av natriumbisulfitt. J Am Oil Chem Soc (2013) 90: 1917-1926. Gjenopprettet fra aocs.onlinelibrary.wiley.com.
- Borek, C. et al. (1985). Sodium bisulfite beskytter mot radiogen og kjemisk indusert transformasjon i hamsterembryo og mus C3H / 10T-1/2-celler. Toxicol Ind Health 1985Sep; 1 (1): 69-74. Gjenopprettet fra journals.sagepub.com.
- Friedler, E. et al. (2015). En kontinuerlig aktiv overvåkingsmetode for å identifisere kryssforbindelser mellom drikkevann og distribusjonssystem for avløp. Environ Monit Assess (2015) 187: 131. Gjenopprettet fra link.springer.com.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Sunnyvale Cleanwater Program. (2019). Hovedplan for vannforurensningskontrollanlegg. Gjenopprettet fra sunnyvalecleanwater.com.
- Barros Santos, C. (2008). Tilsetningsstoffer i spansk mat og lovgivningen som regulerer godkjenning og bruk. Visjonsbøker. Gjenopprettet fra books.google.co.ve.



Ingen har kommentert denne artikkelen ennå.