
Fosfatbuffer (PBS) begrunnelse, tilberedning og bruk
De fosfatbuffer, BPS eller fosfatbuffer saltvann Det er en buffer og isoton løsning, hvis funksjon er å opprettholde pH og osmotisk trykk så tett som mulig på det naturlige biologiske (fysiologiske) miljøet. Forkortelsen PBS står for fosfatbufret saltvann..
PH og osmolaritet er to veldig viktige aspekter som må kontrolleres i visse laboratorieprotokoller. Når det gjelder pH, er det viktig at den kontrolleres, spesielt i biokjemiske reaksjoner, siden disse kan variere eller ikke utføres hvis reaktantene har en upassende pH.

I mellomtiden er kontroll av osmolaritet viktig, spesielt når du arbeider med levende celler, siden plasmamembranene i cellene reagerer i henhold til konsentrasjonen av oppløste stoffer der de er funnet..
Hvis cellene overføres til et hypertonisk medium vil de dehydrere, siden vanngradienten vil bli transportert til siden der det er en høyere konsentrasjon av oppløste stoffer. Hvis derimot celler plasseres i et hypotonisk medium, vil cellene absorbere væske til de lyseres..
Derfor brukes PBS-bufferen til laboratorieprotokoller som krever vedlikehold av celler. in vitro, på denne måten vil ikke cellene bli skadet.
PBS består av en kombinasjon av salter, slik som natriumklorid, natriumfosfat, kaliumklorid og kaliumfosfat. Sammensetningen av PBS kan variere avhengig av protokollen..
Artikkelindeks
- 1 Begrunnelse
- 2 Klargjøring
- 2,1-lageroppløsning fosfatbuffer saltløsning (PBS 10X)
- 2,2 -Buffer fosfat saltvann (1X PBS)
- 2.3 Løsninger for pH-justering
- 3 bruksområder
- 4 Begrensninger
- 5 Referanser
Basis
I utgangspunktet er saltfosfatbufferens funksjon å opprettholde en konstant fysiologisk pH sammen med en elektrolyttkonsentrasjon som den som finnes i kroppen..
I dette miljøet er celler i stand til å forbli stabile, da fysiologiske forhold simuleres så mye som mulig..
Andre forbindelser kan tilsettes den opprinnelige PBS-formuleringen om nødvendig, for eksempel er tilsetning av EDTA til bufferen nyttig for vasking av røde blodlegemer i krysskompatibilitetstesten..
EDTA forhindrer at fraksjonen av komplement C1 som er tilstede i serumet spaltes og lyseres til de røde blodcellene, det vil si at det unngår falske inkompatibilitetsresultater. I tillegg hjelper EDTA med å dissosiere celler.
Forberedelse
Mengden salt som må veies for fremstilling av PBS-fosfatbufret saltvann, vil avhenge av mengden som må tilberedes:
-Lagerfosfatbufret saltløsning (10X PBS)
For en liter løsning:
Veie:
80,6 g NaCl,
2,2 g KCl,
11,5 g NatoHPO4,
2,0 g KHtoHPO4
Forberedelsesteknikk
Legg de tunge saltene i et begerglass, tilsett nok vann (80%) og bland på omrøringsplaten med magnetstang til saltene er oppløst..

Filtrer for å fjerne uoppløste partikler. Bruk filtre med porene 0,45 µm. Autoklav og distribuer aseptisk i laminær hette i glasskrukker med lokk.
10X-løsningen (konsentrert) justerer ikke pH. Justeringen gjøres når den er fortynnet til 1X PBS-bufferkonsentrasjon, (1:10 fortynning).
-Fosfatbuffer Saltvann (1X PBS)
1X PBS kan tilberedes direkte, med en vekt på tilsvarende mengder av hvert salt, eller det kan tilberedes ved å fortynne stamløsningen (1:10) med sterilt destillert vann..
-For å tilberede en liter 1X PBS fosfatbufret saltvann direkte, veier:
8,06 g NaCl,
0,22 g KCl,
1,15 g NatoHPO4,
0,20 g KHtoHPO4
Forberedelsesteknikk
Fortsett som forklart for den konsentrerte løsningen. Deretter må pH justeres. For å gjøre dette måler du pH og avhengig av resultatet, bruker du syre (HCl) eller base (NaOH) for å senke eller øke pH henholdsvis etter behov, til den er 7,4.
Syren eller basen tilsettes dråpe for dråpe mens pH-verdien til løsningen overvåkes ved bruk av en pH-meter. Filtrer, autoklaver og fordel aseptisk i koniske rør eller krukker etter behov.
-For å forberede 1X PBS fra 10X lagerløsningen:
Gjør en fortynning på 1:10. For eksempel, for å forberede 1 liter 1X PBS, måle opp 100 ml av stamløsningen og tilsett 700 ml sterilt destillert vann. Juster pH og fyll vannmengden opp til 1000 ml.
Den tilberedte PBS-bufferen er fargeløs og gjennomsiktig.
Den daglige PBS kan oppbevares ved romtemperatur og resten i kjøleskapet.
.Løsninger for pH-justering
HCl
For 100 ml 1 molar HCL (saltsyre).
Mål 91 ml destillert vann og legg det i et 250 ml begerglass.
Mål 8,62 ml konsentrert HCl og tilsett det sakte i begerglasset som inneholder vannet (gjør det aldri omvendt). Ta relevante biotiltak når du håndterer sterke syrer (svært etsende stoff).
Bland i 5 minutter, fortrinnsvis ved hjelp av en omrøringsplate med en magnetstang inne i glasset. Overfør til en 100 ml ballong og fyll opp til 100 ml med HtoEller destillert.
NaOH
For 100 ml NaOH (natriumhydroksyd) 10 molar.
Mål 40 ml destillert vann og legg det i et 250 ml begerglass. Mål 40 g NaOH og tilsett i vannet. Bland med en omrøringsplate med en magnetstang inne i glasset.
Overfør til en 100 ml målekolbe og fyll opp til merket med destillert vann. Følg biosikkerhetsbestemmelsene, fordi denne reaksjonen er eksoterm (den frigjør energi i form av varme).
Hvis du vil tilberede andre mengder fosfat saltløsning, kan du se følgende tabell:
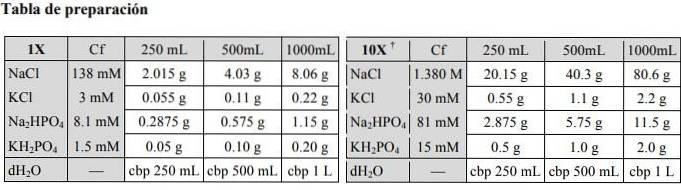
applikasjoner
Brukes hovedsakelig i cellebiologi, immunologi, immunhistokjemi, bakteriologi, virologi og forskningslaboratorier.
Den er ideell for cellevask ved sentrifugering (røde blodlegemer), celle-monolagsvask, i spektroskopiske ellipsometri-teknikker, i kvantifisering av bakterielle biofilmer, vedlikehold av cellekulturer for virus, som en vaskeoppløsning i den indirekte immunfluorescenssteknikken. i teknikker for karakterisering av monoklonale antistoffer.
Det brukes også til å transportere celler eller vev, som et fortynningsmiddel for celletelling, fremstilling av cellulære enzymer (trypsin), som et fortynningsmiddel for metode for uttørking av biomolekyler og for å fremstille andre reagenser..
På den annen side demonstrerte Martin et al. I 2006 at PBS er nyttig i rettsmedisinske laboratorier, spesielt i utvinning av sæd fra vaginale utstryk, eller i utvinning av vaginale celler fra utstryk. På denne måten kan det fastslås om det har vært et seksuelt forhold.
Begrensninger
-Noen PBS-buffere inneholder et stoff som kalles natriumazid som konserveringsmiddel. Denne forbindelsen kan generere eksplosive stoffer hvis den kommer i kontakt med bly eller kobber. Av denne grunn må du være spesielt forsiktig når du kaster dette reagenset i avløpet. Hvis det kastes på denne måten, må det tilsettes mye vann for å fortynne det så mye som mulig..
-Sink skal ikke tilsettes fosfatbufferen, siden det fører til at noen salter faller ut.
-Wangen et al. I 2018 fastslått at bruk av PBS ikke var egnet til å vaske primær akutt myeloid leukemi (AML) celler ekstrahert fra perifert blod, på grunn av det faktum at mange celler går tapt ved lysis, med en stor reduksjon i proteinmateriale.
Derfor bestemte de seg for at primære AML-celler ikke skulle vaskes med PBS etter lagring i flytende nitrogen..
Referanser
- Coll J. (1993). Diagnostiske teknikker i virologi. Ed Díaz de Santos. 360 s
- Rodríguez M, Ortiz T. Cellekultur. Endring av medium. Institutt for normal og patologisk cytologi og histologi Universitetet i Sevilla. Tilgjengelig på personal.us.es
- Fremstilling av fosfatbufret saltvann (PBS). (2008). Standard operasjonsprosedyrer (SOPs) Viral and Human Genomics Laboratory UASLP School of Medicine. Tilgjengelig på: genomica.uaslp.mx
- "Fosfatbuffer saltvann." Wikipedia, The Free Encyclopedia. 3. apr 2019, 19:36 UTC. 13. april 2019, 02:57 en.wikipedia.org.
- Pietrasanta L, Von-Bilderling C. Emner i molekylær biofysikk. Tilgjengelig på: users.df.uba.ar
- Rediar. Håndbok. PBS + EDTA. Tilgjengelig på: felsan.com.ar
- Martin NC, Pirie AA, Ford LV, Callaghan CL, McTurk K, Lucy D, Scrimger DG. Bruk av fosfatbufret saltvann for utvinning av celler og spermatozoer fra vattpinner. Sci Justice. 2006; 46 (3): 179-84. Tilgjengelig på: ncbi.nlm.nih.gov
- Wangen R, Aasebø E, Trentani A, et al. Konserveringsmetode og fosfatbufret saltvask påvirker det akutte myeloide leukemiproteomet. Int J Mol Sci. 2018; 19 (1): 296. Tilgjengelig på: ncbi.nlm.nih.gov
- Martínez R, Gragera R. (2008). Teoretiske og praktiske grunnlag for histokjemi. Superior Council of Scientific Investigations. Madrid. Tilgjengelig på: books.google.co.ve



Ingen har kommentert denne artikkelen ennå.