
Propansyreformel, egenskaper, risiko og bruksområder

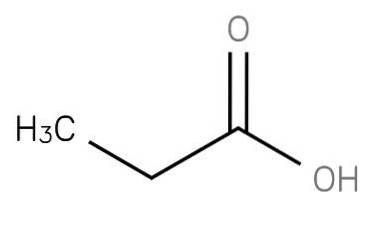
De propansyre er en mettet kortkjedet fettsyre omfattende etan bundet til karbonet i en karboksygruppe. Formelen er CH3-CHto-COOH. CH3CH2COO-anionen samt saltene og estrene av propansyre er kjent som propionater (eller propanoater).
Det kan fås fra rester av tremasse ved gjæringsprosess ved bruk av bakterier av slekten propionibacterium. Det er også oppnådd fra etanol og karbonmonoksid ved bruk av en bor-trifluoridkatalysator (O'Neil, 2001).
En annen måte å oppnå propansyre på er ved oksidasjon av propionaldehyd i nærvær av kobolt- eller manganioner. Denne reaksjonen foregår raskt ved temperaturer så lave som 40-50 ° C:
2CH3CHtoCHO + Oto → 2CH3CHtoCOOH
Forbindelsen er naturlig tilstede ved lave nivåer i meieriprodukter og produseres generelt sammen med andre kortkjedede fettsyrer i mage-tarmkanalen hos mennesker og andre pattedyr som sluttproduktet av mikrobiell karbohydratfordøyelse..
Har betydelig fysiologisk aktivitet hos dyr (Human Metabolome Database, 2017).
Artikkelindeks
- 1 Fysiske og kjemiske egenskaper
- 2 Reaktivitet og farer
- 3 Biokjemi
- 4 bruksområder
- 5 Referanser
Fysiske og kjemiske egenskaper
Propansyre er en fargeløs, oljeaktig væske med en skarp, ubehagelig, harsk lukt. Dens utseende er vist i figur 2 (National Center for Biotechnology Information, 2017).

Propansyre har en molekylvekt på 74,08 g / mol og en tetthet på 0,992 g / ml. Dens frysepunkt og kokepunkt er henholdsvis -20,5 ° C og 141,1 ° C. Propansyre er en svak syre hvis pKa er 4,88.
Forbindelsen er veldig løselig i vann, og er i stand til å oppløse 34,97 gram forbindelse for hver 100 ml løsningsmiddel. Det er også løselig i etanol, eter og kloroform (Royal Society of Chemistry, 2015).
Propansyre har fysiske egenskaper som er mellom de mindre karboksylsyrene, myresyre og eddiksyre, og de større fettsyrene..
Det viser de generelle egenskapene til karboksylsyrer og kan danne amid-, ester-, anhydrid- og kloridderivater. Det kan gjennomgå alfa-halogenering med brom i nærvær av PBr3 som en katalysator (HVZ-reaksjonen) for å danne CH3CHBrCOOH.
Reaktivitet og farer
Propansyre er et brennbart og brennbart materiale. Det kan antennes av varme, gnister eller flammer. Damp kan danne eksplosive blandinger med luft og være i stand til å reise til antennelseskilden og eksplodere.
De fleste damper er tyngre enn luft. De vil spres langs bakken og samles i lave eller begrensede områder (kloakk, kjellere, tanker). Dampeksplosjonsfare innendørs, utendørs eller i kloakk.
Stoffer betegnet med (P) kan polymerisere eksplosivt når de blir oppvarmet eller oppslukt av en brann. Beholdere kan eksplodere ved oppvarming (PROPIONIC ACID, 2016).
Forbindelsen skal holdes borte fra varme eller antennelseskilder. Ved oppvarming til nedbrytning avgir den skarp røyk og irriterende røyk.
Propansyre irriterer huden, øynene, nesen og halsen, men gir ikke akutte systemiske effekter og har ikke påviselig genotoksisk potensial. I tilfelle kontakt, vask med rikelig med vann (Sikkerhetsdatablad propionsyre, 2013).
Biokjemi
Den konjugerte basen av propansyre, propionat, er dannet som det terminale tre-karbonfragmentet (aktivert med koenzym A som propionyl-CoA) i oksidasjon av oddetalls karbonfettsyrer og sidekjedeoksidasjon av kolesterol.
Eksperimenter med radioaktive isotoper av propionat injisert i fastende rotter indikerer at det kan vises i glykogen, glukose, mellomprodukter av sitronsyresyklusen, aminosyrer og proteiner..
Banen til metabolismen av propansyre innebærer interaksjon med koenzym A, karboksylering for å danne metylmalonyl-koenzym A og omdannelse til ravsyre, som går inn i sitronsyresyklusen.
Propansyre kan oksyderes uten å danne ketonlegemer, og i motsetning til eddiksyre er den innlemmet i et karbohydrat så vel som en lipid (Bingham, Cohrssen, & Powell, 2001).
Propionsyreuria er en av de vanligste organiske aciduriene, en sykdom som omfatter mange forskjellige lidelser.
Utfallet av pasienter født med propionsyreuria har dårlig intellektuell utviklingsmønster, med 60% som har en IQ mindre enn 75 og som krever spesialundervisning..
Vellykkede lever- og / eller nyretransplantasjoner hos noen få pasienter har resultert i forbedret livskvalitet, men har ikke nødvendigvis forhindret innvoller og nevrologiske komplikasjoner.
Disse resultatene understreker behovet for permanent metabolsk overvåking, uavhengig av terapeutisk strategi..
applikasjoner
Propansyre hemmer bakterie- og muggvekst i nivåer mellom 0,1 og 1 vekt%. Som et resultat konsumeres det meste av den produserte propansyren som konserveringsmiddel for både fôr og mat til konsum, for eksempel korn og korn..
Konservering av fôr, korn og mat i tillegg til produksjon av kalsium- og natriumpropionater, som representerer nesten 80% av det globale forbruket av propansyre i 2016, mot 78,5% i 2012.
Omtrent 51% av det globale forbruket av propansyre er bestemt til dyrefôr og kornbevaring, mens nesten 29% brukes til produksjon av kalsium- og natriumpropionater, som også brukes i næringsmiddelindustrien.
Andre viktige markeder for propansyre er herbicid og dietylketonproduksjon. Applikasjoner med lavere volum inkluderer fremstilling av celluloseacetatpropionat, farmasøytiske midler, løsemiddelestere, smakstilsetninger og dufter, myknere, tekstil-, lær- og gummifargestoffer og hjelpestoffer.
Etterspørselen etter propansyre er sterkt avhengig av fôr- og kornproduksjon, etterfulgt av pakket mat og bakervarer.
De globale vekstutsiktene for propansyre og dens salter i dyrefôr / korn og konservering av matvarer er betydningsfulle (IHS Markit, 2016).
Andre raskt voksende markeder inkluderer propionatestere for løsningsmidler, slik som n-butyl og pentylpropionat; Disse esterne brukes i økende grad som erstatninger for løsemidler som er oppført som farlige luftforurensninger..
Referanser
- Bingham, E., Cohrssen, B., & Powell, C. (2001). Patty's Toxicology Volumes 1-9 5th ed. New York: John Wiley & Sons.
- EMBL-EBI. (2016, 14. oktober). propionsyre. Gjenopprettet fra ChEBI: ebi.ac.uk.
- Human Metabolome Database. (2017, 2. mars). Propionsyre. Gjenopprettet fra hmdb.ca: hmdb.ca.
- IHS Markit. (2016, desember). Håndbok for kjemisk økonomi propionsyre. Gjenopprettet fra ihs: ihs.com.
- Sikkerhetsdatablad Propionsyre. (2013, 21. mai). Gjenopprettet fra sciencelab: sciencelab.com.
- Nasjonalt senter for bioteknologisk informasjon ... (2017, 22. april). PubChem Compound Database; CID = 1032. Gjenopprettet fra pubchem.ncbi.nlm.nih.gov.
- O'Neil, M. (. (2001). The Merck Index - En Encyclopedia of Chemicals, Drugs, and Biologicals. 13. utgave. New Jersey: Merck and Co., Inc.
- PROPJONSYRE. (2016). Gjenopprettet fra cameochemicals: cameochemicals.noaa.gov.
- Royal Society of Chemistry. (2015). Propionsyre. Gjenopprettet fra chemspider: chemspider.com.



Ingen har kommentert denne artikkelen ennå.