
Fosfatidyletanolaminstruktur, biosyntese og funksjoner
De fosfatidyletanolamin (PE) er et glyserofosfolipid som er rikelig i plasmamembranene til prokaryote organismer. Tvert imot, i eukaryote cellemembraner er dette det nest mest utbredte glyserofosfolipidet på innsiden av plasmamembranen etter fosfatidylkolin..
Til tross for overflod av fosfatidyletanolamin, avhenger dens overflod ikke bare av celletypen, men også av rommet og øyeblikket til den spesifikke cellesyklusen som vurderes..
Biologiske membraner er barrierer som definerer cellulære organismer. Ikke bare har de beskyttelses- og isolasjonsfunksjoner, men de er også nøkkelen til etablering av proteiner som krever et hydrofobt miljø for optimal funksjon..
Både eukaryoter og prokaryoter har membraner som hovedsakelig består av glyserofosfolipider og i mindre grad sfingolipider og steroler..
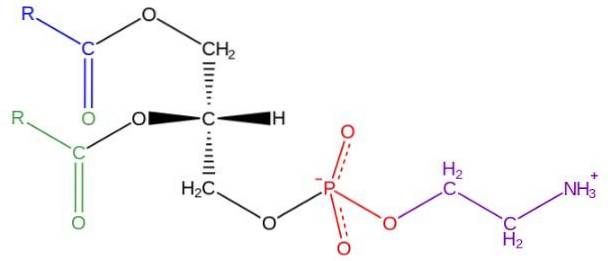
Glyserofosfolipider er amfipatiske molekyler strukturert på en L-glyserol-ryggrad som er forestret i sn-1 og sn-2-posisjonene av to fettsyrer av varierende lengde og grad av metning. I hydroksylen i sn-3-posisjonen forestres den av en fosfatgruppe, som i sin tur kan festes forskjellige typer molekyler som gir opphav til de forskjellige klasser av glyserofosfolipider.
I den mobile verdenen er det et stort utvalg av glyserofosfolipider, men de mest vanlige er fosfatidylkolin (PC), fosfatidyletanolamin (PE), fosfatidylserin (PS), fosfatidylinositol (PI), fosfatidinsyre (PA), fosfatidylglyserol (PG) og kardiolipin (CL).
Artikkelindeks
- 1 Struktur
- 2 Biosyntese
- 2.1 Kennedy-rute
- 2.2 PSD-bane
- 3 funksjoner
- 4 Referanser
Struktur
Strukturen av fosfatidyletanolamin ble oppdaget av Baer et al. I 1952. Som det er blitt bestemt eksperimentelt for alle glyserofosfolipider, dannes fosfatidyletanolamin av et glyserolmolekyl forestret ved sn-1 og sn-2-posisjonene med syrekjeder fettete med mellom 16 og 20 karbonatomer.
Fettsyrene som er forestret i sn-1 hydroksyl er vanligvis mettede (uten dobbeltbindinger) med maksimale lengder på 18 karbonatomer, mens kjedene som er koblet i sn-2 posisjonen er lengre og med en eller flere umettinger (dobbeltbindinger).
Graden av metning av disse kjedene bidrar til elastisiteten til membranen, som har stor innflytelse på innsetting og binding av proteiner i dobbeltlaget..
Fosfatidyletanolamin betraktes som et ikke-lamellært glyserofosfolipid, siden det har en konisk geometrisk form. Denne formen er gitt av den lille størrelsen på dens polare gruppe eller "hode", i forhold til fettsyrekjedene som utgjør de hydrofobe "halene".
"Hodet" eller den polare gruppen av fosfatidyletanolamin har en zwitterionisk karakter, det vil si at den har grupper som kan bli positivt og negativt ladet under visse pH-forhold..
Denne egenskapen gjør det mulig å hydrogenbinde seg med et stort antall aminosyrerester, og dens ladningsfordeling er en viktig faktor for domenetopologien til mange integrerte membranproteiner..
Biosyntese
I eukaryote celler er syntesen av strukturelle lipider geografisk begrenset, og det viktigste biosyntese-stedet er det endoplasmatiske retikulum (ER) og i mindre grad Golgi-apparatet..
Det er fire uavhengige biosyntetiske veier for produksjon av fosfatidyletanolamin: (1) CDP-etanolaminveien, også kjent som Kennedy-banen; (2) PSD-banen for fosfatidylserin (PS) dekarboksylering; (3) acylering av lyso-PE og (4) baseendringsreaksjoner i den polare gruppen av andre glyserofosfolipider.
Kennedy-ruten
Fosfatidyletanolaminbiosyntese ved denne veien er begrenset til ER, og det er vist at i hamsterleverceller er det den viktigste produksjonsveien. Den består av tre påfølgende enzymatiske trinn katalysert av tre forskjellige enzymer.
I det første trinnet produseres fosfoetanolamin og ADP takket være virkningen av etanolaminkinase, som katalyserer den ATP-avhengige fosforylering av etanolamin..
I motsetning til planter er verken pattedyr eller gjær i stand til å produsere dette substratet, så det må konsumeres i dietten eller oppnås ved nedbrytning av eksisterende fosfatidyletanolamin- eller sfingosinmolekyler..
Fosfoetanolamin brukes av CTP: fosfoetanolamin cytidyltransferase (ET) for å danne høyenergiforbindelsen CDP: etanolamin og et uorganisk fosfat.
1,2-diacylglyseroletanolaminfosfotransferase (ETP) bruker energien som finnes i CDP-etanolaminbinding for å kovalent binde etanolamin til et membraninnsatt diacylglyserolmolekyl, noe som gir opphav til fosfatidyletanolamin..
Rute PSD
Denne ruten fungerer både i prokaryoter og i gjær og pattedyr. I bakterier forekommer det i plasmamembranen, men i eukaryoter forekommer det i et område av endoplasmatisk retikulum som er nært beslektet med mitokondriell membran.
I pattedyr blir veien katalysert av et enkelt enzym, fosfatidylserin-dekarboksylase (PSD1p), som er innebygd i mitokondriell membran, hvis gen er kodet av kjernen. Reaksjonen involverer dekarboksylering av PS til fosfatidyletanolamin.
De resterende to banene (PE-lyso-acylering og polar gruppeavhengig kalsiumutveksling) forekommer i endoplasmatisk retikulum, men bidrar ikke nevneverdig til total fosfatidyletanolaminproduksjon i eukaryote celler..
Funksjoner
Glyserofosfolipider har tre hovedfunksjoner i cellen, blant hvilke strukturelle funksjoner, energilagring og cellesignalering skiller seg ut..
Fosfatidyletanolamin er assosiert med forankring, stabilisering og folding av flere membranproteiner, så vel som konformasjonsendringene som er nødvendige for å fungere for mange enzymer..
Det er eksperimentelle bevis som foreslår fosfatidyletanolamin som et avgjørende glyserofosfolipid i det sene stadiet av telofase, under dannelsen av den kontraktile ringen og etableringen av fragmoplasten som tillater deling av membranen til de to dattercellene..
Det har også en viktig rolle i alle prosesser for fusjon og fisjon (forening og separasjon) av membranene i både det endoplasmatiske retikulumet og Golgi-apparatet..
I E. coli har det vist seg at fosfatidyletanolamin er nødvendig for korrekt folding og funksjon av enzymet laktosepermease, og det er derfor det har blitt antydet at det spiller en rolle som en molekylær "chaperone".
Fosfatidyletanolamin er hovedgiveren til etanolaminmolekylet som er nødvendig for posttranslasjonell modifisering av mange proteiner, for eksempel GPI-ankere.
Dette glyserofosfolipidet er forløperen til mange molekyler med enzymatisk aktivitet. I tillegg kan molekyler avledet fra metabolismen, samt diacylglyserol, fosfatidinsyre og noen fettsyrer, fungere som andre budbringere. I tillegg er det et viktig substrat for produksjon av fosfatidylkolin..
Referanser
- Brouwers, J. F. H. M., Vernooij, E. A. A. M., Tielens, A. G. M., & van Golde, L. M. G. (1999). Rask separasjon og identifisering av fosfatidyletanolaminmolekylære arter. Journal of Lipid Research, 40 (1), 164-169. Gjenopprettet fra jlr.org
- Calzada, E., McCaffery, J. M., og Claypool, S. M. (2018). Fosfatidyletanolamin produsert i den indre mitokondrie-membranen er viktig for gjærcytokrom bc1-kompleksfunksjon 3. BioRxiv, 1, 46.
- Calzada, E., Onguka, O., & Claypool, S. M. (2016). Fosfatidyletanolaminmetabolisme i helse og sykdom. International Review of Cell and Molecular Biology (Vol. 321). Elsevier Inc..
- Gibellini, F., & Smith, T. K. (2010). Kennedy pathway-de novo-syntese av fosfatidyletanolamin og fosfatidylkolin. IUBMB Life, 62 (6), 414-428.
- Harayama, T., og Riezman, H. (2018). Forstå mangfoldet av membranlipidsammensetning. Nature Reviews Molecular Cell Biology, 19 (5), 281-296.
- Luckey, M. (2008). Membranstrukturbiologi: med biokjemiske og biofysiske grunnlag. Cambrudge University Press. Gjenopprettet fra cambrudge.org
- Seddon, J. M., Cevc, G., Kaye, R. D., & Marsh, D. (1984). Røntgendiffraksjonsstudie av polymorfismen av hydratiserte diacyl- og dialkylfosfatidyletanolaminer. Biokjemi, 23 (12), 2634-2644.
- Sendecki, A. M., Poyton, M. F., Baxter, A. J., Yang, T., & Cremer, P. S. (2017). Støttede lipiddrivlag med fosfatidyletanolamin som hovedkomponent. Langmuir, 33 (46), 13423-13429.
- van Meer, G., Voelker, D. R., & Feignenson, G. W. (2008). Membranlipider: hvor de er og hvordan de oppfører seg. Nature Reviews, 9, 112-124.
- Vance, J. E. (2003). Molekylær og cellebiologi av fosfatidylserin og fosfatidyletanolaminmetabolisme. I K. Moldave (red.), Progress Nucleic Acid Research and Molecular Biology (s. 69-111). Akademisk presse.
- Vance, J. E. (2008). Fosfatidylserin og fosfatidyletanolamin i pattedyrceller: to metabolisk relaterte aminofosfolipider. Journal of Lipid Research, 49 (7), 1377-1387.
- Vance, J. E., & Tasseva, G. (2013). Dannelse og funksjon av fosfatidylserin og fosfatidyletanolamin i pattedyrceller. Biochimica et Biophysica Acta - Molecular and Cell Biology of Lipids, 1831 (3), 543-554.
- Watkins, S. M., Zhu, X., & Zeisel, S. H. (2003). Fosfatidyletanolamin-N-metyltransferaseaktivitet og diett kolin regulerer lever-plasma lipidstrøm og essensiell fettsyremetabolisme hos mus. The Journal of Nutrition, 133 (11), 3386-3391.


Ingen har kommentert denne artikkelen ennå.