
Metalloids egenskaper, egenskaper og bruksområder
De metalloider eller halvmetaller er en gruppe kjemiske elementer med mellomliggende fysiske og kjemiske egenskaper mellom metaller og ikke-metaller. De fleste kjemiske forskere aksepterer følgende kjemiske elementer som metalloider: bor, silisium, arsen, germanium, antimon og tellur (grønt i bildet nedenfor).
Imidlertid legger en mindre gruppe forskere polonium, astat (blå i fargen) og selen (rosa i fargen) til metalloider..
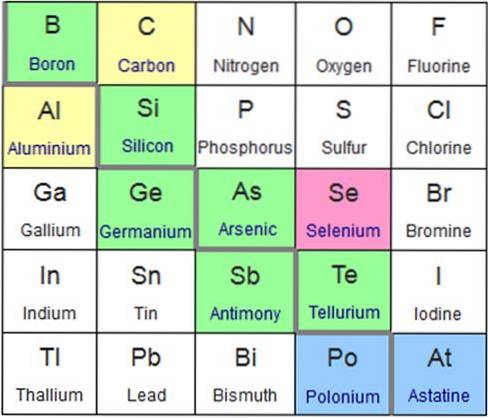
Selv basert på noen egenskaper, foreslår de at de kjemiske elementene karbon og aluminium (gul i fargen) også bør betraktes som metalloider..
Artikkelindeks
- 1 Hovedegenskaper ved metalloider
- 1.1 Situasjon i periodisk tabell
- 1.2 De danner legeringer med metaller
- 1.3 Elektriske halvledere
- 1.4 Basis for elektronikkindustrien
- 1.5 Allotropiske tilstander
- 2 Fysiske og kjemiske egenskaper
- 2.1 Fysiske egenskaper
- 2.2 Kjemiske egenskaper
- 3 bruksområder
- 3.1 Om levende vesener
- 3.2 I briller og emaljer
- 3.3 I produksjon av materialer av høyere kvalitet
- 3.4 I elektronikk og databehandling
- 3.5 Beskyttende handling av metalloider
- 3.6 Andre
- 4 De 8 metalloidelementene
- 5 Referanser
Hovedegenskapene til metalloider
Situasjonen på det periodiske systemet
Metalloider er plassert på det periodiske bordet på en diagonal nedover mellom kolonnene 13, 14, 15, 16 og 17, og starter med bor øverst til venstre og slutter med astatin nede til høyre..
Metaller er til venstre for metalloider og ikke-metaller til høyre; derfor representerer de grensen mellom begge typer materier.
De danner legeringer med metaller
Metalloider danner legeringer med metaller og reagerer med ikke-metaller, for eksempel med oksygen, svovel og halogener..
Elektriske halvledere
For det meste blir de betraktet som elektriske halvledere, hvor konduktansen er temperaturavhengig. Ved lave temperaturer er den elektriske ledningen lav, så de fungerer som elektriske isolatorer, men når de varmes opp, øker deres evne til å lede elektrisitet..
Elektronikkindustri
Halvledere er grunnlaget for utviklingen av elektronikkindustrien, så vel som databehandling og informatikk. På samme måte har applikasjonen som er laget av silisium vært veldig nyttig innen dette feltet.
Allotropiske tilstander
Metalloider har forskjellige allotrope tilstander (forskjellige krystallinske former); således har for eksempel arsen svarte, gule eller grå krystaller.
I naturen blir de vanligvis ikke funnet som rene kjemiske elementer, men snarere assosiert eller dannet tilslag i mineraler sammen med bly, svovel, jern, etc..
Fysiske og kjemiske egenskaper

Fysiske egenskaper
De fremstår som skinnende faste stoffer. I denne forbindelse ligner de metaller. De er sprø og ikke veldig elastiske, så de kan ikke strekkes i form av en ledning, det vil si at de ikke er veldig duktile. I tillegg er transformasjonen til ark vanskelig, så metalloidene er ikke veldig formbare..
De er i stand til å lede elektrisitet og temperatur, men i mindre grad enn metaller. Innenfor metalloidene er det kjemiske elementer som, basert på båndstrukturer, klassifiseres som halvledere.
Denne gruppen består av bor, silisium, germanium og antimon. Arsen og tellur er klassifisert som halvmetaller.
Fusjonspoeng
Bor 2 076 ° C; Silisium 1414 ° C; Germanium 938,25 ° C; Arsen 817 ° C; Antimon 630,13 ° C; Tellurium 449,51 ° C og Polonium 254 ° C.
Kokepunkter
Bor 3 927 ° C; Silisium 3265 ° C; Germanium 2,833 ° C; Arsen 614 ° C; Antimon 1,587 ° C; Tellurium 988 ° C og Polonium 962 ° C.
Tettheter
Bor 2,34 g / cm3: Silisium 2,33 g / cm3; Germanium 5,323 g / cm3; Arsen 5,727; Antimon 6,697 g / cm3; Tellurium 6,24 g / cm3 og Polonium 9,32 g / cm3.
Kjemiske egenskaper
De oppfører seg på samme måte som ikke-metaller, de danner oksasyrer som SiOto og de har en amfoterisk oppførsel. Metalloider kan oppføre seg som en syre eller en base, avhengig av pH i mediet..
applikasjoner
Om levende vesener
-Arsen brukes i landbruket som insektmiddel og herbicid. I tillegg brukes det til å plassere det som et pulver eller i flytende løsning på husdyr for å eliminere insekter og parasitter fra dyret. Kalsiumarsenat brukes til å drepe bomullsboll.
-Arsen brukes som et trebeskyttelsesmiddel på grunn av dets toksisitet for insekter og sopp.
-Arsen brukes til å behandle akutt promyelocytisk leukemi, en type blodkreft. Den brukes til fremstilling av Fowlers løsning for bruk i behandling av psoriasis. En radioaktiv isotop av arsen (74As) brukes i lokaliseringen av kreftsvulster som er tilstede i menneskekroppen.
-Arsen er en del av Melarsoprol, et legemiddel som brukes til behandling av human afrikansk trypanosomiasis. Parasitt sykdom overført av tsetsefluen.
-Telluroksid har blitt brukt til behandling av seboreisk dermatitt. På samme måte brukes andre tellurforbindelser som antimikrobielle midler..
-Bor, i form av borsyre, brukes som et mildt antiseptisk middel i øyne, nese og hals.
I briller og emaljer
-Tellurium brukes i produksjonen av blå, brune og røde briller. Metalloid kan avsettes elektrolytisk på sølv og gir en svartaktig overflate.
-Antimon brukes til å gi briller og emaljer en gul fargetone. Bor brukes i produksjonen av glass og keramikk. Spesielt er borsilikatglass motstandsdyktig mot temperaturendringer, og det er derfor det brukes i laboratorier i kjemiske reaksjoner og destillasjoner..
-Hjemme kan maten bakes med borosilikatglass uten å knuse bruksredskapene..
-Silisium er den viktigste basen i glassindustrien, involvert i produksjon av nesten alle glassgjenstander.
-Germaniumoksid brukes til fremstilling av kameralinser og mikroskoplinser. I tillegg brukes den til fremstilling av kjernen til optiske fibre for mange bruksområder..
I produksjonen av materialer av høyere kvalitet
-Arsen danner legeringer med bly og forårsaker en reduksjon i smeltepunktet. Dette fører til en høyere hardhet i legeringen som brukes i produksjonen av skudd.
-Tilsetningen av en mengde tellur mellom 0,1% og 0,6% av en blyholdig legering øker dens motstand mot korrosjon og mot trekkraft med en økning i fleksibilitet. Tellurium blir ofte tilsatt støpejern for å herde overflatelaget av herdede deler..
-Antimon brukes i legeringer for å produsere lagre, akkumulatorplater og trykkmateriale.
-Silisium brukes i produksjonen av legeringer med høyere motstandsdyktighet mot syrer. Slik er tilfellet Duriron, som inneholder 14% silisium.
Legeringen av silisium, jern og aluminium brukes til utarbeidelse av stykker med stor hardhet, som brukes i bilindustrien.
-Arsen danner legeringer med platina og kobber for å øke korrosjonsmotstanden. I tillegg tilsettes arsen i alfamessing for å øke sinkens styrke. Denne typen messing brukes til fremstilling av tilbehørsmaterialer for rørleggerarbeid.
I elektronikk og databehandling
-Metalloider brukes som halvledere i elektronikk- og dataindustrien. Slik sett er silisium ledende innen handel med halvleder som danner grunnlaget for moderne elektronikk og databehandling. Silisium og dets derivater brukes i datamaskiner, transitorer, solceller og LCD-skjermer..
-Tellurium er en halvleder som har applikasjoner innen elektroptikk og elektronikk.
-Germanium er en halvledermetalloid som brukes i forbindelse med silisium i høyhastighets integrerte kretser for å forbedre ytelsen. Selv om germanium har noe fortrengt silisium i sin halvlederfunksjon, er dets bruk ved fremstilling av miniatyrfliser blitt forbedret.
-Germanium brukes til produksjon av solcellepaneler. Selv utforskende roboter på planeten Mars inneholder germanium i solcellene. I tillegg brukes germanium til produksjon av radarer.
Beskyttende handling av metalloider
Bor og dets relaterte forbindelser gir stor motstand mot materialene det er en del av. Dette tillater bruk i etableringen av romlige strukturer. I tillegg brukes de til produksjon av golfklubber og fiskestenger..
Den beskyttende virkningen av borkarbid brukes som kontrollbarrierer i atomreaktorer, noe som begrenser lekkasje av radioaktivt materiale. I tillegg brukes borkarbid i skuddsikre vester og i rustning av krigstanker..
Silisiumdioksid og silisiumdioksyd, i form av leire eller sand, er viktige komponenter i murstein, betong og sement, brukt i forskjellige former for konstruksjon.
Andre
-Antimonsulfid brukes i fyrverkeri og blitslamper.
-Bor er en del av neodymidium-magneter.
-Silikon, en polymer avledet fra silisium, brukes til fremstilling av oljer og voks, brystimplantater, kontaktlinser, eksplosiver og i pyroteknikk.
-Germanium brukes til fremstilling av lysrør og noen lysdioder. I tillegg brukes germanium i elektriske gitarer for å produsere en karakteristisk forvrengningstone..
-Germanium brukes i termisk bildeapplikasjon for militær bruk og brannslukking.
-Antimon brukes til fremstilling av fyrstikker og sporings- og lokaliseringsgranater, så vel som i grunning for patroner.
-Natriumborat brukes som brannhemmende middel i plast og gummi.
De 8 metalloidelementene
Denne gruppen kjemiske grunnstoffer består av bor, silisium, antimon, tellur, germanium, arsen, polonium og astat. Imidlertid utelukker det største antallet forskere innen kjemi polonium og astat som metalloider..
Derfor vil den mest aksepterte gruppen metalloider bestå av bor, silisium, antimon, tellur, germanium og arsen..
Polonium har blitt bemerket å være karakteristisk metallisk, siden de to allotrope formene er metalliske ledere. På den annen side ble astatin klassifisert i 2013 som et metall, selv om det i 1950 ble utpekt som et halogen, et reaktivt ikke-metallisk.
Grensen mellom gruppene av elementer som betraktes som metaller, metalloider eller ikke-metaller er uklar. Av denne grunn foreslår noen forskere, basert på noen egenskaper, at dette eller det andre elementet skal betraktes som metalloid. Det er for eksempel blitt påpekt at karbon, aluminium eller selen skal klassifiseres som metalloider.
Det er gjort et forsøk på å etablere utvalgskriterier som gjør det mulig å klassifisere et kjemisk element som metall, metalloider eller ikke-metallisk. Andre utvalgskriterier inkluderer ioniseringsenergi, elektronegativitet og pakningseffektivitet for de forskjellige kjemiske elementene..
Referanser
- Eden Francis. (2002). Klassifisering av elementene. Hentet fra: dl.clackamas.edu
- Metaller, metalloider og ikke-metaller. Hentet fra: angelo.edu
- Elementer. Metalloider. Hentet fra: elements.org.es
- Eksempel av. (2013). Metalloider. Hentet fra: examplede.com
- Wikipedia. (2018). Metalloid. Hentet fra: en.wikipedia.org
- Hurtigfaste kjemi. (2011). Metalloider (halvmetaller). Hentet fra: chemistry.patent-invent.com
- Redaksjonen av Encyclopaedia Britannica. (2016, 18. oktober). Metalloid. Hentet fra: britannica.com


Ingen har kommentert denne artikkelen ennå.