
Natriumsilikat (Na2SiO3) struktur, egenskaper, bruksområder, risiko

De natriumsilikat er en uorganisk forbindelse dannet av to natrium-na-ioner+ og et silikatanion SiO3to-. Det sies også å være sammensatt av et molekyl av silisiumdioksyd SiOto og et natriumoksyd NatoO. Dens kjemiske formel kan uttrykkes som NatoJa3 eller også NatoELLER.Jato.
Imidlertid kan sammensetningen av natriumsilikatet variere avhengig av SiO-forholdetto/ NatoEnten etter vekt eller i mol. Det kalles også løselig silikat eller vannglass. Det kan fås i form av pulver, store krystalllignende biter eller i form av løsninger.

Natriumsilikat brukes mye i vaskemidler og såper når det myker opp vannet, noe som gjør rengjøringen mer effektiv. Det er også en del av produkter som barberkrem.
Det er råmaterialet for å fremstille SiO-silikakatalysatorerto. Dens løsninger brukes som lim i mange bruksområder, alt fra selvklebende papir og papp, til glass, porselen, ildfaste former, sement og slipeskiver..
Fordi det er et helt ikke-brennbart materiale, brukes det til å lage brannsikre stoffer, da det er brannhemmende, og som belegg for beskyttelsesutstyr..
Artikkelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Tetthet
- 3.5 Løselighet
- 3,6 pH
- 3.7 Kjemiske egenskaper
- 3.8 Andre egenskaper
- 4 Motta
- 5 bruksområder
- 5.1 I såper og vaskemidler
- 5.2 I katalysatorer og silikageler
- 5.3 Som lim eller lim
- 5.4 I oljebrønnborevæsker
- 5.5 I forskjellige applikasjoner
- 6 Risiko
- 7 Referanser
Struktur
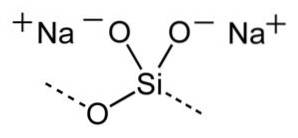
Den generelle formelen for natriumsilikater er xSiOto/ NatoEller hvor x er molar- eller vektforholdet.
Molforholdet betyr antall mol SiOto delt på antall mol NatoO. Vektforhold betyr vekt av SiOto delt på vekt av NatoELLER.
Legge til mer alkali (NatoO) molar- eller vektforholdet endres.
En natriumsilikatoppløsning med lavt molforhold, for eksempel 1/1 (1 mol SiOto og 1 mol NatoO) inneholder hovedsakelig SiO-monomerer44- og S dimerertoELLER5to- i tillegg til Na-ionene+.
En løsning med et høyt molforhold som 3,3 / 1 (3,3 mol SiOto for hver mol NatoO) har en høy andel av polymere arter eller polymerer av silisium og oksygen.
Nomenklatur
-Natriumsilikat
-Sodium Metasilicate
-Løselig glass
-Glass vann (fra engelsk vannglass)
-Løselig silikat
Eiendommer
Fysisk tilstand
-Massivt i store biter som ligner blågrønne krystaller
-Fargeløst til hvitt pulverformig fast stoff
-Fargeløse vandige løsninger.
Molekylær vekt
Fra formelen NatoJa3: 122,063 g / mol.
Smeltepunkt
NatoJa3: 1089 ° C
Tetthet
Det avhenger av SiO-forholdetto/ NatoELLER.
Løselighet
Når det er i form av store biter av grønn krystall, er det løselig i vann ved oppvarming og under høyt trykk. Pulveret er litt mer løselig, men i begge tilfeller er dets løselighet avhengig av mengden natrium eller NatoEller at den eier.
Jo høyere natriuminnholdet (i form av NatoO) raskere oppløses.
pH
De vandige løsningene er sterkt basiske.
Kjemiske egenskaper
Kommersielt forberedt i SiO-forholdto/ NatoEller i vekt fra 1,5 til 3,3. Når SiO økerto i forholdet reduserer løseligheten i vann og alkalinitet.
Oppløsende fast silikat i vann kan danne gelatinøse eller svært viskøse blandinger.
Natriumsilikatpulver kan være lekker, det vil si hvis det har en høy mengde NatoEller det har en tendens til lett å absorbere vann fra miljøet.
Hvis pH i løsningene senkes ved tilsetning av syre, dannes en gel.
Andre egenskaper
Det er ikke brannfarlig.
Å skaffe
Silikatsand SiO smeltes for å oppnå natriumsilikaterto med natriumkarbonat NatoCO3 vannfri i åpen ovn. Molforholdet mellom sand og natriumkarbonat kan variere kommersielt fra 0,5 til 3,75.

applikasjoner
I såper og vaskemidler
Natriumsilikater er blant de første forbindelsene som ble brukt i vaskemiddelformuleringer.

Natriumsilikatbindere kalsium Ca-ionerto+ og magnesium Mgto+, eliminere det som kalles vannets hardhet, det vil si å myke det opp. Ved å gjøre dette dannes uoppløselige bunnfall, så det brukes i små mengder.
Virkningen av natriumsilikatet gjør at vaskemidlet kan fungere uten at de nevnte ionene påvirker rengjøringsprosessen.
I kiselgeler og katalysatorer
Silikageler blir vanligvis fremstilt ved forsuring av en natriumsilikatoppløsning til en pH på mindre enn 10 eller 11. Tiden som kreves for å gelere varierer..

Silisiumdioksyd kan fremstilles ved å blande natriumsilikat med en sterk mineralsyre. Natriumsilikat brukes til fremstilling av baser for katalysatorer, siden det er kilden til silika SiOto.
Som lim eller lim
Konsentrerte vandige natriumsilikatløsninger brukes som lim og tetningsmasse. De tåler temperaturer opp til 1100 ° C.
De viktigste anvendelsene av natriumsilikatlim er i selvklebende papir, bølgepapp eller bølgepapp, esker og kartonger. Også for liming eller agglomerering av tre eller for festing av metall til forskjellige typer materialer.

Den brukes til å lime glass, porselen, keramikk, tekstiler, lær, etc. For liming av glassfiber-, optisk glass- og slagfast glassbeholdere.
Det gjør det mulig å forberede ildfaste sementer for å bygge tanker, vannkoker, ovner og former for metallstøping, samt å lage vanntette eller syrefast mørtel eller sement.
Natriumsilikater kan reagere med silisiumfluorider for å produsere syrebestandige sementer med lav tendens til å krympe og varmeutvidelse som den for stål..
De brukes også til å lage sement for slipeskiver som brukes til polering..
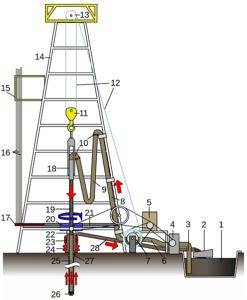
I oljebrønner som borer væsker
Natriumsilikat har blitt brukt i mange år som en kjemisk oppslemming under boring av visse typer formasjoner med meget høy permeabilitet, slik som de som utgjøres av sand..
Høy permeabilitet betyr at den lett slipper væske gjennom.
Det tilsettes sammen med en forbindelse som aktiverer silikatet for å danne en polymer. Denne polymeren gir styrke, stivhet og reduserer permeabilitet i granulær jord..
Siden jorda er mindre gjennomtrengelig, passerer ikke væsken fritt gjennom den, og på denne måten unngås tap av væske under borefasen av brønnen.
I forskjellige applikasjoner
Natriumsilikat har også en rekke bruksområder. Her er det noe.
-I daglig pleieprodukter er det for eksempel en komponent i barberkremer.
-I vannbehandling.
-I bleking av tekstiler som ull.
-I bleking av papirmasse. For å bleke malt tre brukes en blanding som inneholder hydrogenperoksid og natriumsilikat blant andre ingredienser. Natriumsilikat brukes til å sekvestre metallioner, som har en tendens til å akselerere nedbrytningen av peroksid..
-For produksjon av brannsikre stoffer. Som brannhemmende middel og som belegg for verneutstyr.
-I silikapigmenter.
-For å oppdage maiskjerner infisert av insekter. En blanding av natriumsilikat og vann brukes der de angrepne kornene flyter raskt til overflaten.
-I sinkbelegg.
-Å rengjøre metaller.
-I mineralflotasjon brukes det som et dispergeringsmiddel for slam og silt og som et balsam for overflaten av mineraler..
-Å impregnere tre.
Risiko
Natriumsilikat er på grunn av det høye alkaliinnholdet sterkt irriterende for hud, øyne og slimhinner. Ved svelging kan det være giftig og irritere slimhinner på samme måte som kaustisk brusoppløsning..
Det må lagres separat fra sterke syrer, metaller og halogener som fluor, som det reagerer voldsomt med.
Referanser
- Ebnesajjad, S. (2015). Egenskaper for selvklebende materialer. Løselige silikater (kalium og natriumsilikat). I håndbok for lim og overflateforberedelse. Gjenopprettet fra sciencedirect.com.
- Fink, J.K. (2012). Tilsetningsstoffer for væsketap. Sodium metasilicate. I Petroleum Engineer's Guide to Oil Field Chemicals and Fluids (Andre utgave). Gjenopprettet fra sciencedirect.com.
- OSS. National Library of Medicine. (2019). Natriumsilikat. Nasjonalt senter for bioteknologisk informasjon. Gjenopprettet fra pubchem.ncbi.nlm.nih.gov.
- Kirk-Othmer. (1984). Encyclopedia of Chemical Technology, 3. utg., John Wiley og Sons.
- Maeda, K. et al. (2007). Fra zeolitter til porøse MOF-materialer - 40th Jubileum for den internasjonale Zeolitkonferansen. I studier i overflatevitenskap og katalyse. Gjenopprettet fra sciencedirect.com.
- Chopade, S.P. og Nagarajan, K. (2000). Vaskemiddelformuleringer: ionebytte. I Encyclopedia of Separation Science. Gjenopprettet fra sciencedirect.com.
- .


Ingen har kommentert denne artikkelen ennå.