
Kaliumtiocyanat (KSCN) struktur, egenskaper, bruksområder

De kaliumtiocyanat Det er en uorganisk forbindelse dannet av grunnstoffene kalium (K), svovel (S), karbon (C) og nitrogen (N). Den kjemiske formelen er KSCN. Det er et fargeløst eller hvitt fast stoff veldig løselig i vann. Den består av et kalium K-ion+ og et SCN-tiocyanation-. KSCN finnes rikelig i spytt.
Kaliumtiocyanat brukes som laboratoriereagens for forskjellige typer kjemisk analyse. Den brukes også i blekk og maling.

KSCN har blitt brukt til å oppløse dentingelatin (materiale under tannemalje) før du påfører tannreparasjonsmateriale eller harpiks. Det brukes også i forskning på vaksiner, da det tillater utvinning av visse biokjemiske elementer fra bakterier.
Den brukes i form av en løsning der metaller oppløses under poleringsprosessen ved hjelp av elektrisitet eller elektropolering. Det har også blitt brukt til å skaffe falskt blod til filmer og skuespill.
Noen ganger blir det misbrukt for å øke melkens stabilitet når den ikke oppbevares nedkjølt. Men det har ulempen med å forårsake hypotyreose, en sykdom der skjoldbruskkjertelen ikke fungerer..
Artikkelindeks
- 1 Struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Nedbrytningstemperatur
- 3,5 Tetthet
- 3.6 Løselighet
- 3,7 pH
- 3.8 Andre egenskaper
- 4 Motta
- 4.1 Tilstedeværelse i naturen
- 5 bruksområder
- 5.1 I forskjellige applikasjoner
- 5.2 I tannlegeanvendelser
- 5.3 I medisinske laboratorier
- 5.4 I metallindustrien
- 5.5 På settet med filmer eller i teatret
- 5.6 Misbruk av kaliumtiocyanat
- 6 Risiko
- 7 Referanser
Struktur
Kaliumtiocyanat består av et kalium K-kation+ og et NCS-tiocyanatanion-. Sistnevnte er dannet av et nitrogen (N) festet til et karbon (C) gjennom en trippelbinding og et svovel (S) festet til karbon gjennom en enkeltbinding.
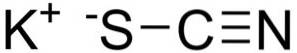
Nomenklatur
- Kaliumtiocyanat
- Kaliumsulfocyanat
- Kaliumsalt av tiocyansyre
- Kalium Rodanat
- Kalium rodanid
Eiendommer
Fysisk tilstand
Fargeløst eller hvitt fast stoff.
Molekylær vekt
97,18 g / mol
Smeltepunkt
173 ºC
Nedbrytningstemperatur
500 ºC
Tetthet
1,88 g / cm3
Løselighet
Svært løselig i vann: 217 g / 100 ml ved 20 ° C, 238 g / 100 ml ved 25 ° C. Løselig i etanol.
pH
En 5% løsning av KSCN har en pH mellom 5,3 og 8,7.
Andre egenskaper
Rene, tørre kaliumtiocyanatprøver er stabile på ubestemt tid når de oppbevares i mørket i tett dekkede glasskrukker. Imidlertid blir de fargeløse krystallene raskt gullige i kontakt med direkte sollys..
Løsninger av rent KSCN-salt beskyttet mot lys er helt stabile.
KSCN er i stand til å hovne opp gelatin og kollagen. Vandige oppløsninger av kaliumtiocyanat når de reagerer med mangandioksid MnOto oksiderer og danner tiocyanogen (SCN)to.
Å skaffe
Kaliumtiocyanat kan fremstilles ved å smelte kaliumcyanid (KCN) med svovel (S). Reaksjonen er rask og kvantitativ.
KCN + S → KSCN
Det kan oppnås i løsning ved å oppløse svovel (S) i benzen eller aceton og tilsette en løsning av kaliumcyanid (KCN) i isopropanol. Denne reaksjonen brukes til å analysere mengden svovel i en løsning.
Kaliumtiocyanat kan oppnås rent ved påfølgende omkrystallisering fra vann eller etanol..
Tilstedeværelse i naturen
Kaliumtiocyanat finnes rikelig i spytt (15 mg / dL), men det er fraværende i blodet.
Også melken til noen pattedyr (som kyr) har veldig små mengder tiocyanat naturlig.
applikasjoner
I forskjellige applikasjoner
Kaliumtiocyanat har blitt brukt i forskjellige kjemiske analyser. Det har blitt brukt til analyse eller titrering av sølvion, også som et reagens og indikator for andre analyser.
KSCN brukes i fargestoffer og pigmenter. Brukes i maling og blekk.
I fotoindustrien brukes den spesielt til fremstilling av fotografifilmer, da den tjener til å tillate fast avsetning av gelatin fra plastfilmer..
Konsentrasjonen av tiocyanat i blod har blitt brukt i medisinsk-vitenskapelige eksperimenter for å bestemme i hvilken grad noen mennesker røyker, siden tiocyanat er et produkt avledet fra hydrogencyanid (HCN) tilstede i tobakkrøyk..
I dental applikasjoner
Kaliumtiocyanat har blitt brukt til reparasjon av dyretenner. Det har blitt påført vellykket på dentinoverflaten som en forbehandling før middelet påføres for å fylle eller plugge det åpne hullet.
Dentin er laget som finnes under emaljen på tennene.
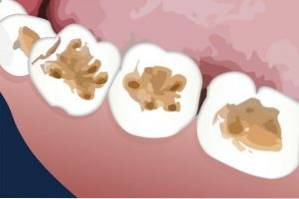
Kaliumtiocyanat favoriserer hevelse i gelatinen som er på dentinet, slik at dette laget lett fjernes, og en bedre vedheft eller binding av materialet som forsegler tannen (harpiks) resulterer..
I medisinske laboratorier
KSCN brukes til fremstilling av vaksiner eller bakterieekstrakter.
De patogene bakteriene dyrkes ved inkubasjon i egnede laboratoriebeholdere. Deretter tilsettes en fosfat pH-regulator og KSCN i beholderen der bakteriekulturen er lokalisert..
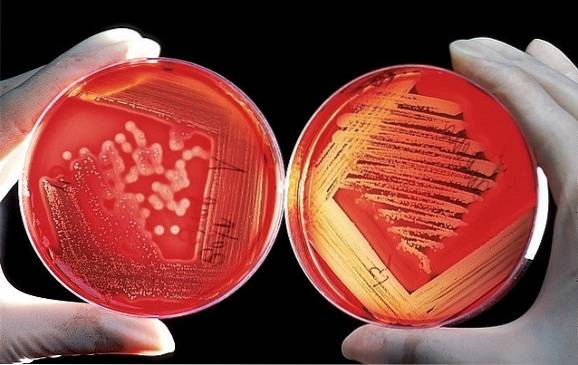
En del av dette bakteriepreparatet tas og legges i en krukke. Den omrøres i et passende tidsrom, og suspensjonen sentrifugeres for å skille væsken fra det faste materialet. Supernatanten (væske) samles og dialyseres.
Resultatet er et ekstrakt som brukes til å vaksinere i vitenskapelige eksperimenter med forsøksdyr..
I metallindustrien
Kaliumtiocyanat brukes til elektropolering av metaller. Elektropolering er en kjemisk prosess som gjør det mulig å behandle overflaten av et metall for å redusere dets mikroruffhet, det vil si for å glatte metalloverflaten..
Dette gjøres med elektrisitet, slik at metallet glattes til å fungere som den positive polen eller anoden til den elektrolytiske cellen. Ruheten løses opp i kaliumtiocyanatoppløsningen, og metallet blir dermed jevnere.
På settet med filmer eller i teatret
KSCN brukes i simulering av blod i film- og TV-filmer eller i skuespill.
For eksempel påføres en løsning av kaliumtiocyanat (KSCN) på området av kroppen som vil "lide" kuttet eller simulert angrep. Plastkniven eller det simulerte skjæreobjektet blir badet i en løsning av jernklorid (FeCl3).
Den “skarpe” gjenstanden som har FeCl passeres forsiktig3 på hud fuktet i KSCN. Umiddelbart vil en rød stripe eller flekk være veldig lik blodets.
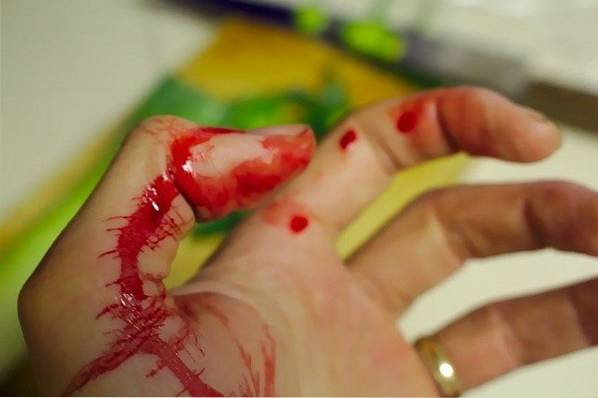
Dette skyldes dannelsen av et kompleks av jerntiocyanat og vann [Fe (NCS) (HtoELLER)5]to+ som har en intens rød farge som ligner på blod:
KSCN + FeCl3 + 5 timertoO → [Fe (NCS) (HtoELLER)5]to+ + 2 Cl- + KCl

Kaliumtiocyanat misbruk
Kaliumtiocyanat brukes skruppelløst for å forhindre at melk blir angrepet av bakterier eller sopp, mister egenskapene og forverres.
I tropiske land brukes en metode som kalles "lakto-peroksidasesystem" eller LP-system, som øker melkens stabilitet når den oppbevares ved høye omgivelsestemperaturer, når kjøling ikke er mulig..

Denne metoden bruker det naturlige antibakterielle systemet av melk, som aktiveres ved å øke konsentrasjonen av tiocyanat (allerede tilstede i små mengder i melk) og hydrogenperoksid (HtoELLERto).
Imidlertid er denne metoden ikke tillatt i mange land av myndighetene som regulerer bearbeidet mat..
Noen skruppelløse mennesker legger til KSCN for å melke irrasjonelt med eller uten HtoELLERto, som utgjør en fare for forbrukerens helse, siden tiocyanater er stoffer som forårsaker skade på skjoldbruskkjertelen og kan forårsake hypotyreose ved inntak i høye konsentrasjoner.

Risiko
Innånding av kaliumtiocyanatpulver bør unngås. Det anbefales å bruke hansker og beskyttelsesbriller når du håndterer det. Etter kort eksponering for kaliumtiocyanat kan det forårsake effekter på nervesystemet, for eksempel overdreven følelse uten motiv, uro og kramper..
Etter en lang eksponering kan skjoldbruskkjertelen og sentralnervesystemet påvirkes, noe som manifesterer seg som henholdsvis hypotyreose og forverring av noen funksjoner. Ved inntak kan det føre til forvirring, kvalme, oppkast, kramper og svakhet..
Ved antennelse eller forbrenning av KSCN frigjøres svært giftige cyanidgasser; dette skjer også når du tilsetter syrer. I laboratoriet skal den håndteres i et godt ventilert avtrekksvifte..
Referanser
- Jarvinen, L.Z. et al. (1998). Induksjon av beskyttende immunitet hos kaniner ved samtidig administrering av inaktiverte Pasteurella multocida Gift- og kaliumtiocyanatekstrakt. Infeksjon og immunitet, aug, 1998, s. 3788-3795. Gjenopprettet fra ncbi.nlm.nih.gov.
- Tani, Y. og Togaya, T. (1995). Dentin overflatebehandling uten syrer. Dental Materials Journal 14 (1): 58-69, 1995. Hentet fra jstage.jst.go.jp.
- Kolthoff, I.M. og Lingane, J.J. (1935). Kaliumtiocyanat som en primær standard substans. Journal of the American Chemical Society 1935, 57, 11, 2126-2131. Gjenopprettet fra pubs.acs.org.
- Balmasov, A.V. et al. (2005). Elektropolering av sølv i vann-organiske løsninger av kaliumtiocyanat. Prot Met 41, 354-357 (2005). Gjenopprettet fra link.springer.com.
- Cotton, F. Albert og Wilkinson, Geoffrey. (1980). Avansert uorganisk kjemi. Fjerde utgave. John Wiley & Sons.
- Lide, D.R. (redaktør) (2003). CRC Håndbok for kjemi og fysikk. 85th CRC Trykk.
- Tyner, T. og Francis, J. (2017). Kaliumtiocyanat. ACS Reagent Chemicals. Gjenopprettet fra pubs.acs.org.
- Kanthale, P. et al. (2015). Kvalitativ test for påvisning av fremmed tiocyanat i melk. J Food Sci Technol (mars 2015) 52 (3): 1698-1704. Gjenopprettet fra ncbi.nlm.nih.gov.
- Roy, D. et al. (2018) Silicon Quantum Dot-Based Fluorescent Probe: Synthesis Characterization and Recognition of Thiocyanate in Human Blood. ACS Omega 2018, 3, 7, 7613-7620. Gjenopprettet fra pubs.acs.org.
- Gammon, K. (2018). Vitenskapen om falskt blod. Inside Science. Gjenopprettet fra insidescience.org.


Ingen har kommentert denne artikkelen ennå.