
Heksan (C6H14) fysiske og kjemiske egenskaper, struktur, bruksområder, toksisitet
De heksan er et hydrokarbon karakterisert ved å være en organisk forbindelse hvis kondenserte kjemiske formel er C6H14. Det er en fargeløs, gjennomsiktig væske som ikke kan blandes med vann. Den har fem isomerer, den lineære er en av de viktigste parafiniske hydrokarboner i industri og forskning.
Heksan oppnås ved fraksjonert destillasjon av råolje. På samme måte er det naturlig til stede i sitrusfrukter og i flyktige fraksjoner av forskjellige planter eller frukt som eple, guava, ristede hasselnøtter, søtpotet og salvie..
Det er en svært brannfarlig flyktig væske som finnes i bensin, hurtigtørkende lim og gummisement. Heksan brukes som løsemiddel i ekstraksjonsprosessen av vegetabilske oljer, så vel som lipider og fett som er tilstede i forurenset vann og jord.
Personer som er profesjonelt utsatt for heksan, kan oppleve skade på perifere nervesystem, manifestert av kriblinger og kramper i ben og armer; i tillegg til generalisert muskelsvakhet og i alvorlige tilfeller skjelettmuskulær atrofi.
Artikkelindeks
- 1 Fysiske og kjemiske egenskaper til heksaner
- 1.1 Fysisk utseende
- 1.2 Molar masse
- 1.3 Lukt
- 1.4 Luktterskel
- 1,5 Tetthet
- 1.6 Smeltepunkt
- 1.7 Kokepunkt
- 1.8 Flammepunkt
- 1.9 Løselighet i vann
- 1.10 Løselighet i løsningsmidler
- 1.11 Relativ damptetthet med luft
- 1.12 Fordelingskoeffisient for oktanol / vann
- 1.13 Damptrykk
- 1.14 Bølgelengde med maksimal optisk tetthet
- 1.15 Brytningsindeks
- 1.16 Viskositet
- 1,17 Kalorikapasitet
- 1.18 Forbrenningsvarme
- 1.19 Fordampningsvarme
- 1.20 Overflatespenning
- 1.21 Ioniseringspotensial
- 1.22 Stabilitet
- 1.23 Reaktivitet
- 2 Struktur av heksan
- 2.1 Intermolekylære interaksjoner
- 2.2 Isomerer
- 3 bruksområder
- 4 Toksisitet
- 4.1 Innånding og kontakt
- 4.2 Sikker dose
- 5 Referanser
Fysiske og kjemiske egenskaper til heksaner
Fysisk utseende
Fargeløs, gjennomsiktig og svært flyktig væske.
Molarmasse
86,178 g / mol
Lukt
I likhet med bensin
Luktterskel
1,5 spm
Tetthet
0,6606 g / ml
Smeltepunkt
-96 til -94 ºC
Kokepunkt
68,5 til 69,1 ºC
antennelsespunkt
-22 ºC (lukket kopp).
Vannløselighet
9,5 mg / l (praktisk talt blandbar med vann)
Løselighet i løsningsmidler
Svært løselig i etanol, løselig i etyleter og kloroform. Blandbar med alkohol, kloroform og eter.
Relativ damptetthet med luft
2,97 (luft = 1)
Fordelingskoeffisient for oktanol / vann
Logg P = 3764
Damptrykk
17,60 kPa ved 20 ºC
Bølgelengde med maksimal optisk tetthet
200 nm
Brytningsindeks
1.375
Viskositet
0,3 mPa s
Kalorikapasitet
265,2 JK-1Muldvarp-1
Forbrenningsvarme
4,163,2 kJ mol-1
Fordampningsvarme
31,56 kJ mol-1
Overflatespenning
17,89 mN / m ved 25 ºC
Ioniseringspotensial
10,18 eV
Stabilitet
Stabil. Uforenlig med oksidasjonsmidler, klor, fluor, magnesiumperklorat. Danner en eksplosiv blanding med luft.
Reaktivitet
Heksan kan reagere kraftig med oksiderende materialer, som kan inkludere flytende klor, konsentrert oksygen, natriumhypokloritt og kalsiumhypokloritt. Det er også inkompatibelt med dinitrogen tetroxide. Heksan kan angripe noen former for plast, gummi og belegg.
Struktur av heksan
Intermolekylære interaksjoner
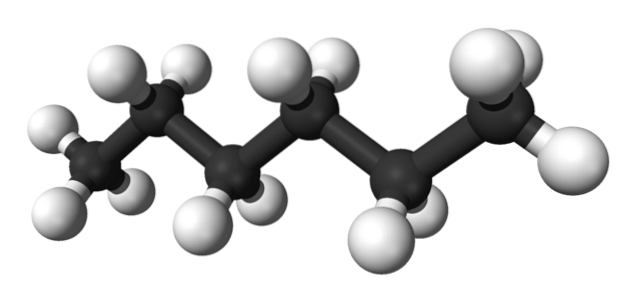
Det første bildet viser molekylet av n-heksan representert med en ball-and-stick-modell. De svarte kulene tilsvarer karbonatomene, og utgjør det sikksakkende karbonskjelettet, mens de hvite kulene er hydrogenatomene. De n-Heksan er derfor et hydrokarbon, lineært og svært dynamisk.
Fordi alle dets C-H-bindinger har lav polaritet, mangler molekylet et dipolmoment. Ved å gjøre dette er deres intermolekylære interaksjoner ikke av dipol-dipol-typen, men avhenger utelukkende av molekylær masse og Londons spredningskrefter..
Hvert molekyl av n-Heksan "passer" på hverandre ved svært lave temperaturer, slik man antar i sin krystallinske struktur. På den annen side, i væsken, bøyes skjelettene og roterer deres C-H-bindinger, noe som får væsken til å være flyktig og koke ved 68,7 ºC..
Isomerer
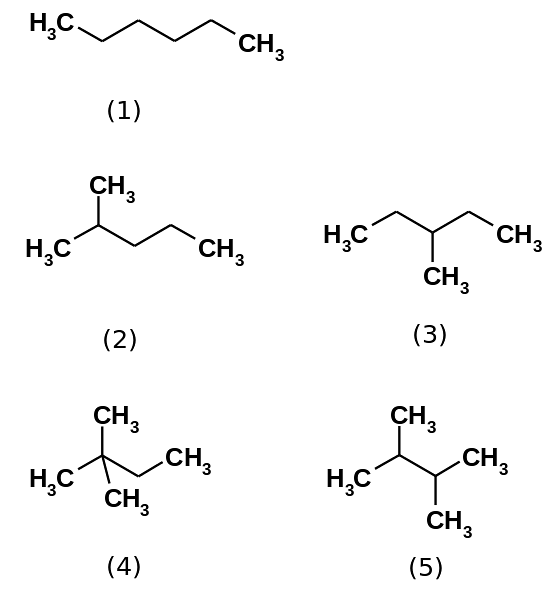
Hydrokarbonheksan består faktisk av fem isomerer, som er n-heksan minst forgrenet, (1). De andre fire isomerer er i økende rekkefølge:
2-metylpropan (2)
3-metylpropan (3)
2,2-dimetylbutan (4)
2,3-dimetylbutan (5)
Vær også oppmerksom på at strukturene blir mer forgrenet fra (1) til (5). Å være mer forgrenet, reduserer dispersjonskreftene, siden det ikke lenger er lineære deler som kiler effektivt. Dette fører til en reduksjon og variasjon i isomerens kokepunkter; selv om det er observert noen akseptable avvik.
Både 2-metylpropan (bp = 60,3 ° C) og 3-metylpropan (bp = 63,3 ° C) er like forgrenede, men kokepunktene er forskjellige. Deretter blir det fulgt av 2,3-dimetylbutan (peb = 58 ºC), for til slutt å lokalisere 2,2-dimetylbutan som den mest flyktige væsken (peb = 49,7 ºC).
applikasjoner
Heksan blandes med lignende kjemikalier for å produsere løsemidler. Blant navnene på disse løsningsmidlene er kommersiell heksan, blandede heksaner, etc. De brukes som rengjøringsmidler i tekstil-, møbel- og gravyrtrykkindustrien..
Heksan er en ingrediens i lim som brukes i vanntetting av tak, fottøy og lær. Den brukes også til å binde bøker, til å støpe piller og tabletter, hermetisering, lage dekk og baseball..
Heksan brukes til å bestemme brytningsindeksen for mineraler og fylle væske for termometre i stedet for kvikksølv; vanligvis med en rød eller blå fargetone. Det brukes også til utvinning av fett og olje fra vann for analyse av forurensningene..
Heksan brukes som løsningsmiddel i utvinning av olje fra vegetabilske frø, som soyabønner, raps eller bjørnebær. I tillegg brukes den til å avfette deler av forskjellig opprinnelse. Den brukes i denaturering av alkohol, i HPLC-analysemetoden og i spektrofotometri.
Toksisitet
Innånding og kontakt
Den akutte toksisiteten til heksan er relativt lav, selv om det er et mildt bedøvelsesmiddel. Akutt eksponering for høye konsentrasjoner av heksan kan produsere, ved innånding, mild sentralnervesystemet (CNS) depresjon, manifestert av svimmelhet, svimmelhet, mild kvalme og hodepine..
Det kan også forårsake dermatitt og irritasjon av øyne og hals. Kronisk innånding av heksan, relatert til arbeidsaktivitet, kan forårsake skade på det perifere nervesystemet (sensorimotorisk polyneuropati).
De første symptomene er prikking og kramper i bena og armene, etterfulgt av muskelsvakhet. I alvorlige tilfeller kan skjelettmuskulær atrofi oppstå, sammen med tap av koordinasjon og synsproblemer.
Heksantoksisitet er relatert til genereringen av heksan-2,5-dionmetabolitten. Det reagerer med aminosyren lysin i en proteinsidekjede og forårsaker tap av proteinfunksjon..
Sikker dose
Miljøvernbyrået (EPA) beregnet en referansekonsentrasjon (RfC) for heksan på 0,2 mg / m3, og en referansedose (RfD) på 0,06 mg / kg kroppsvekt / dag.
På 1960- og 1970-tallet hadde en gruppe arbeidere i skomakerindustrien i Japan tilstedeværelse av nervesykdommer. Årsaken var at de pustet inn en heksanatmosfære på 500 - 2500 ppm, i 8-14 timer per dag.
Arbeiderne viste de kjente symptomene på kronisk innånding av heksan, og oppdaget legene at nervene som kontrollerte musklene i armer og ben var skadet..
Referanser
- Danielle Reid. (2019). Heksan: Struktur, formel og egenskaper. Studere. Gjenopprettet fra: study.com
- Nasjonalt senter for bioteknologisk informasjon. (2019). Heksan. PubChem-database. CID = 8058. Gjenopprettet fra: pubchem.ncbi.nlm.nih.gov
- Wikipedia. (2019). Heksan. Gjenopprettet fra: en.wikipedia.org
- World of Molecules. (s.f.). Heksanmolekyl. Gjenopprettet fra: worldofmolecules.com
- Kjemisk bok. (2017). Heksan. Gjenopprettet fra: chemicalbook.com
- Commonwealth of Australia. (s.f.). n-heksan: Kilder til utslipp. Gjenopprettet fra: npi.gov.au
- EPA. (2000). Heksan. [PDF]. Gjenopprettet fra: epa.gov
- Byrået for giftige stoffer og sykdomsregister. (1999). Folkehelseerklæring for n-Hexane. Gjenopprettet fra: atsdr.cdc.gov


Ingen har kommentert denne artikkelen ennå.