
Trinitrotoluen (TNT) struktur, egenskaper, bruksområder, risiko, eksplosjon
De trinitrotoluen er en organisk forbindelse som består av karbon, oksygen, hydrogen og nitrogen med tre nitro-NO-grupperto. Dens kjemiske formel er C6Hto(CH3)(IKKEto)3 eller også den kondenserte formel C7H5N3ELLER6.
Dets fulle navn er 2,4,6-trinitrotoluen, men det er ofte kjent som TNT. Det er et hvitt krystallinsk fast stoff som kan eksplodere når det varmes opp over en viss temperatur.

Tilstedeværelsen i trinitrotoluen av de tre nitro-NO-gruppeneto favoriserer det faktum at den eksploderer med litt letthet. Av denne grunn har den blitt mye brukt i eksplosive enheter, prosjektiler, bomber og granater..
Den har også blitt brukt til sprengning under vann, i dype brønner og til industrielle eller ikke-krigseksplosjoner..
TNT er et delikat produkt som også kan eksplodere fra veldig sterke slag. Det er også giftig for mennesker, dyr og planter. Stedene der eksplosjonene deres har skjedd, er forurenset og det utføres undersøkelser for å eliminere restene av denne forbindelsen.
En måte som kan være effektiv og billig å redusere konsentrasjonen av TNT i det forurensede miljøet er ved bruk av noen typer bakterier og sopp..
Artikkelindeks
- 1 Kjemisk struktur
- 2 Nomenklatur
- 3 eiendommer
- 3.1 Fysisk tilstand
- 3.2 Molekylvekt
- 3.3 Smeltepunkt
- 3.4 Kokepunkt
- 3.5 Flammepunkt
- 3.6 Tetthet
- 3.7 Løselighet
- 3.8 Kjemiske egenskaper
- 4 Eksplosjonsprosess av TNT
- 4.1 Oksidasjonsreaksjon av TNT
- 5 Skaffe TNT
- 6 Bruk av TNT
- 6.1 I militære aktiviteter
- 6.2 I industrielle applikasjoner
- 7 Risiko for TNT
- 8 Forurensning av miljøet med TNT
- 8.1 Løsning på TNT-forurensning
- 8.2 Sanering med bakterier og sopp
- 8.3 Sanering med alger
- 9 Referanser
Kjemisk struktur
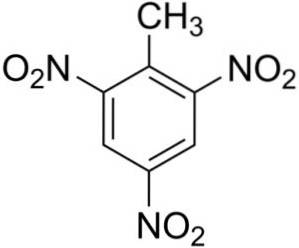
2,4,6-trinitrotoluen består av ett molekyl toluen C6H5-CH3, til hvilke tre nitro-NO-grupper er lagtto.
De tre nitro -NO gruppeneto de er symmetrisk plassert på benzenringen av toluen. De finnes i posisjon 2, 4 og 6, der posisjon 1 tilsvarer metyl-CH3.
Nomenklatur
- Trinitrotoluen
- 2,4,6-trinitrotoluen
- TNT
- Trilite
- 2-metyl-1,3,5-trinitrobenzen
Eiendommer
Fysisk tilstand
Fargeløst til lysegult krystallinsk fast stoff. Nåleformede krystaller.
Molekylær vekt
227,13 g / mol.
Smeltepunkt
80,5 ºC.
Kokepunkt
Det koker ikke. Nedbrytes med en eksplosjon ved 240 ºC.
Flashpoint
Det er ikke mulig å måle det fordi det eksploderer.
Tetthet
1,65 g / cm3
Løselighet
Nesten uoppløselig i vann: 115 mg / L ved 23 ° C. Veldig lett løselig i etanol. Svært løselig i aceton, pyridin, benzen og toluen.
Kjemiske egenskaper
Kan spres eksplosivt ved oppvarming. Når den når 240 ° C eksploderer den. Det kan også eksplodere når du får veldig sterke slag.
Ved oppvarming til nedbrytning produserer det giftige gasser av nitrogenoksider NOx.
TNT eksplosjonsprosess
Eksplosjonen av TNT fører til en kjemisk reaksjon. I utgangspunktet er det en forbrenningsprosess der energi frigjøres veldig raskt. I tillegg slippes det ut gasser som er midler for å overføre energi.

Drivstoff og oksidant må være tilstede for at en forbrenningsreaksjon (oksidasjon) skal finne sted.
Når det gjelder TNT, er begge i samme molekyl, siden karbon (C) og hydrogen (H) atomer er drivstoff og oksidanten er oksygen (O) i nitro-NO-gruppene.to. Dette gjør at reaksjonen kan gå raskere.
TNT oksidasjonsreaksjon
Under forbrenningsreaksjonen til TNT omorganiseres atomene og oksygen (O) holder seg nærmere karbon (C). I tillegg er nitrogenet av -NOto reduseres for å danne nitrogengass Nto som er en mye mer stabil forbindelse.
Eksplosjonen kjemisk reaksjon av TNT kan oppsummeres som følger:
2 C7H5N3ELLER6 → 7 CO ↑ + 7 C + 5 HtoO ↑ + 3 Nto↑
Karbon (C) produseres under eksplosjonen, i form av en svart sky, og det dannes også karbonmonoksid (CO), noe som skyldes at det ikke er nok oksygen i molekylet til å oksidere alle karbonatomer (C) og hydrogen (H) til stede.
Skaffe TNT
TNT er en forbindelse laget kun kunstig av mennesker.
Det finnes ikke naturlig i miljøet. Forekommer bare på noen militære installasjoner.
Den fremstilles ved nitrering av toluen (C6H5-CH3) med en blanding av salpetersyre HNO3 og svovelsyre HtoSW4. Først får du en blanding av orto- Y for å-nitrotoluener som ved påfølgende energisk nitrering danner det symmetriske trinitrotoluenet.
Bruk av TNT
I militære aktiviteter
TNT er et eksplosivt stoff som har blitt brukt i krigslignende enheter og militære eksplosjoner.
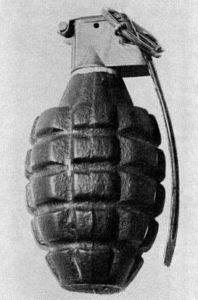
Det brukes til å fylle prosjektiler, granater og luftbårne bomber, siden det er ufølsomt nok for påvirkningen som mottas for å forlate våpenløpet, men det kan eksplodere når det blir truffet av en detonatormekanisme.

Ikke designet for å produsere betydelig fragmentering eller lansering av prosjektiler.
I industrielle applikasjoner
Det har blitt brukt til eksplosjoner av industriell interesse, ved sprengning under vann (på grunn av dets uoppløselighet i vann) og dype brønneksplosjoner. Tidligere ble det oftest brukt til riving. Det brukes for tiden sammen med andre forbindelser.

Det har også vært et mellomledd for fargestoffer og fotografiske kjemikalier.
Risiko for TNT
Kan eksplodere hvis den utsettes for sterk varme, brann eller veldig sterke støt.
Det irriterer øynene, huden og luftveiene. Det er en veldig giftig forbindelse både for mennesker og for dyr, planter og mange mikroorganismer..
Symptomer på eksponering for TNT inkluderer hodepine, svakhet, anemi, giftig hepatitt, cyanose, dermatitt, leverskade, konjunktivitt, dårlig appetitt, kvalme, oppkast, diaré, blant andre..
Det er et mutagen, det vil si at det kan endre genetisk informasjon (DNA) til en organisme og forårsake endringer som kan være relatert til utseendet på arvelige sykdommer.
Det har også blitt klassifisert som kreftfremkallende eller kreftgenerator.
Forurensning av miljøet med TNT
TNT er blitt oppdaget i jord og vann i områder med militære krigføringsoperasjoner, på produksjonsanlegg for ammunisjon og der militære treningsoperasjoner utføres..

Forurensning med TNT er farlig for dyr, mennesker og planter. Selv om TNT for tiden brukes i mindre mengder, er det en av de nitroaromatiske forbindelsene som har blitt brukt mest i eksplosivindustrien..
Av denne grunn er det en av de som bidrar mest til miljøforurensning..
Løsning til forurensning med TNT
Behovet for å "rense" regioner som er forurenset med TNT har motivert utviklingen av flere saneringsprosesser. Utbedring er fjerning av forurensende stoffer fra miljøet.
Utbedring med bakterier og sopp
Mange mikroorganismer er i stand til å bioremediere TNT, for eksempel bakterier av slekten Pseudomonas, Enterobacter, Mycobacterium Y Clostridium.
Det har også blitt funnet at det er visse bakterier som har utviklet seg på steder som er forurenset med TNT, og som kan overleve og også nedbryte eller metabolisere det som næringskilde..
De Escherichia coli For eksempel har den vist en enestående kapasitet for biotransformasjon av TNT, siden den har flere enzymer for å angripe den, og viser samtidig en høy toleranse overfor dens toksisitet..
I tillegg kan noen sopparter biotransformere TNT og gjøre det til ikke-skadelige mineraler..
Algereduksjon
På den annen side har noen forskere funnet ut at algen Spirulina platensis har evnen til å adsorbere på overflaten av cellene dine og assimilere opptil 87% av TNT til stede i vann som er forurenset med denne forbindelsen.
Toleransen til disse algene overfor TNT og dens evne til å rense vann som er forurenset med den, indikerer det høye potensialet til disse alger som fytoremediator..
Referanser
- OSS. National Library of Medicine. (2019). 2,4,6-trinitrotoluen. Gjenopprettet fra pubchem.ncbi.nlm.nih.gov.
- Murray, S.G. (2000). Eksplosiver. Eksplosjonsmekanisme. I Encyclopedia of Forensic Sciences 2000, sider 758-764. Gjenopprettet fra sciencedirect.com.
- Adamia, G. et al. (2018). Om muligheten for alge Spirulina søknad om fytoremediering av vann forurenset med 2,4,6-trinitrotoluen. Annals of Agrarian Science 16 (2018) 348-351. Gjenopprettet fra reader.elsevier.com.
- Serrano-González, M.Y. et al. (2018). Biotransformasjon og nedbrytning av 2,4,6-trinitrotoluen ved mikrobiell metabolisme og deres interaksjon. Defense Technology 14 (2018) 151-164. Gjenopprettet fra pdf.sciencedirectassets.com.
- Iman, M. et al. (2017). Systembiologisk tilnærming til bioremediering av nitroaromatika: begrensningsbasert analyse av 2,4,6-trinitrotoluen-biotransformasjon ved Escherichia coli. Molecules 2017, 22, 1242. Gjenopprettet fra mdpi.com.
- Windholz, M. et al. (redaktører) (1983). Merck-indeksen. En leksikon med kjemikalier, medisiner og biologiske stoffer. Tiende utgave. Merck & CO., Inc..
- Morrison, R.T. og Boyd, R.N. (2002). Organisk kjemi. 6. utgave. Prentice-Hall.


Ingen har kommentert denne artikkelen ennå.