
Aminoglykosider klassifisering, effekter, indikasjoner, kontraindikasjoner

De aminoglykosider De er et sett med antibiotika som har de samme kjemiske og farmakologiske egenskapene. De har en bakteriedrepende effekt mot aerobe gramnegative bakterier (bakterier som flekker blekrosa og ikke mørkeblå eller lilla med gramflekk).
Det første aminoglykosidet som ble oppdaget, var streptomycin, i 1943. Senere fremsto tobramycin og gentamicin som effektive anti-gramnegative antibiotika. På 1970-tallet (1970) ble semisyntetiske aminoglykosider som amikacin, netilmycin og dibekacin utviklet..

De fleste av medlemmene av denne familien har i sin struktur en aminosyklitol (en syklisk alkohol med en aminogruppe R-NH2) bundet av en glykosidbinding til ett eller flere aminosukker, så de er faktisk aminoglykosider - aminocyklitoler.
Disse antibiotika absorberes ikke oralt, så de administreres parenteralt (intravenøst, intramuskulært eller subkutant) eller brukes lokalt. De elimineres ved glomerulær filtrering uten å bli metabolisert tidligere.
Alle medlemmer av denne familien viser en viss grad av nefrotoksisitet (nyretoksiner) og / eller ototoksisitet (giftig for både øret og det vestibulære systemet, kan forårsake hørsels- og balanseforstyrrelser).
De brukes vanligvis i kombinasjon med noe beta-laktam (en annen familie av antibiotika), og bruken er vanligvis begrenset til alvorlige infeksjoner.
Disse antibiotika er kontraindisert hos pasienter som har utviklet allergiske reaksjoner på disse legemidlene. Selv om de overføres til morsmelk, da de ikke absorberes av tarmveien (oral), anses de å være egnede til å administreres til moren, om nødvendig, under amming..
Bruk under graviditet er kun tillatt i tilfeller der de kliniske fordelene oppveier risikoen (risikokategori D).
Artikkelindeks
- 1 Handlingsmekanisme
- 2 Klassifisering
- 2.1 Aminoglykosid med aminocyklitol
- 2.2 Aminocyclitol uten aminoglykosid: Spectinomycin
- 3 Bivirkninger
- 3.1 - Ototoksisitet
- 3.2 - Nyretoksisitet
- 3.3 - Nevrotoksisitet og andre toksiske effekter
- 4 Motstand mot aminoglykosider
- 5 indikasjoner
- 6 Kontraindikasjoner
- 7 Referanser
Virkningsmekanismen
Alle aminoglykosider hemmer proteinsyntese i mottakelige bakterier. Disse holder seg til 30S-enheten av bakterielle ribosomer og hemmer dens funksjon. I motsetning til de fleste antimikrobielle midler som hemmer proteinsyntese som er bakteriostatisk, er disse bakteriedrepende.
"Bakteriostatisk" stammer fra prefikset "bakterie" som betyr bakterier og "stasis" den greske enden som betyr statisk, uten endring. I medisin brukes bakteriostatiske midler for å redusere metabolismen av bakterier og bremse veksten og reproduksjonen..
Hvis det bakteriostatiske middelet elimineres ved oppløsning, vil de tidligere inhiberte bakteriene fortsette å utvikle seg. Et bakteriedrepende middel er et som er i stand til å drepe bakterier. Aminoglykosider er bakteriedrepende.
Den bakteriedrepende effekten av aminoglykosider er konsentrasjonsavhengig. Aminoglykosider trenger inn i det periplasmatiske rommet til aerobe gramnegative bakterier gjennom vannkanaler som kalles aquaporiner..
Transport over den cytoplasmatiske membranen avhenger av elektrontransport og kan inhiberes eller blokkeres av anaerobiose (fravær av oksygen), kalsium, magnesium, sur pH eller hyperosmolaritet..
Vel inne i cellen binder aminoglykosider seg til polysomer (flere ribosomer som oversetter det samme mRNA) ved 30S-underenheten. De forstyrrer proteinsyntese som genererer en lesesvikt og en tidlig avslutning av mRNA-oversettelsesprosessen.
Dette genererer defekte proteiner som, når de settes inn i cellemembranen, endrer permeabiliteten, noe som senere vil lette påfølgende inntasting av disse antibiotika. Senere observeres ionelekkasjer, etterfulgt av større molekyler til proteinene går tapt før bakteriens død..
Klassifisering
Aminoglykosider er klassifisert i to store grupper, avhengig av om de har en aminocyklitol med eller uten aminoglykosidkomponent: aminoglykosider med aminocyklitol og aminocyklitol uten aminoglykosid.
I den første gruppen, som er de som inneholder aminocyklitol med aminoglykosidkomponent, er det to undergrupper. Disse undergruppene er dannet av de forskjellige komponentene i aminocyclitol: streptidin og deoksystreptamin.

Dermed er det en undergruppe med aminocyclitol streptidin og en annen med aminocyclitol deoxystreptamine. De viktigste aminoglykosidene i hver gruppe er vist nedenfor.
Aminoglykosid med aminocyklitol
Aminocyclitol Streptidine: Streptomycin
Aminocyclitol deoxystreptamine: innenfor denne gruppen er Kanamycin, Gentamicin og andre familier.
Kanamycin-familie:
- Kanamycin
- Amikacin
- Tobramycin
- Dibekacin
Gentamicin familie:
- Gentamicin
- Sisomycin
- Netilmycin
- Isepamycin
Andre:
- Neomycin
- Paromomycin
Aminocyclitol uten aminoglykosid: Spectinomycin
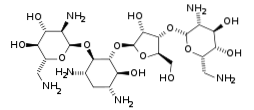
Bivirkninger
Alle aminoglykosider er potensielt giftige for nyresystemet, det auditive systemet og det vestibulære systemet. Disse toksiske effektene kan være reversible eller irreversible. Disse ugunstige sekundære konsekvensene gjør administrering og bruk av disse antibiotika vanskelig..
Når det er nødvendig å tilføre et aminoglykosid i lange perioder og i høye doser, er det nødvendig å overvåke den auditive, vestibulære og nyrefunksjonen, siden i begynnelsen er disse skadene reversible.
- Ototoksisitet
Når aminoglykosider administreres, kan dysfunksjon i både det auditive systemet og det vestibulære systemet oppstå. Disse stoffene akkumuleres og konsentreres i perilymfen og endolymfen i det indre øret, spesielt når det brukes høye doser..
Diffusjon fra disse ørevæskene tilbake i plasma er veldig langsom, og halveringstiden for aminoglykosider i øret er 5 til 6 ganger større enn i blodplasma. Ototoksisitet er mer vanlig hos pasienter som har vedvarende høye plasmakonsentrasjoner.
Ved lave doser observeres skade på sensoriske celler i vestibular organ og cochlea, som påvirker endene (stereocilia) av hårcellene. Ved høyere doser observeres basal skade i disse cellene, til ødeleggelsen av sensoriske celler er generert..
Når sensoriske celler blir ødelagt, er effekten irreversibel, og følgelig oppstår permanente hørselstap. Ettersom cochlea sensoriske celler går tapt med alderen, er eldre pasienter mer utsatt for ototoksisitet ved bruk av disse antibiotika..
Narkotika som furosemid eller syre etakrinisk de forsterker den ototoksiske effekten av aminoglykosider. Begge legemidlene er loop-diuretika (øker urinproduksjonen) som brukes til å behandle høyt blodtrykk og ødem..
Selv om alle aminoglykosider kan påvirke både cochlea og vestibular funksjon, er det en tydelig preferansetoksisitet.
Dermed påvirker streptomycin og gentamicin fortrinnsvis vestibulært system, mens amikacin, kanamycin og neomycin primært påvirker auditiv funksjon og tobramycin påvirker begge funksjonene likt..
Symptomer på cochlear ototoksisitet
Som det første symptomet på ototoksisitet, forekommer vanligvis høyfrekvent tinnitus (susing eller surring som ikke er forbundet med noen lyd fra utsiden). Hvis behandlingen ikke blir avbrutt, vil skaden om noen dager være permanent.
Tinnitus kan vare i opptil to uker, og siden oppfatningen av høyfrekvente lyder går tapt først, er pasienten i utgangspunktet ikke klar over hørselstapet. Hvis behandlingen fortsettes under disse forholdene, utvikler hørselstapet seg til å utvikle taleproblemer.
Vestibulære ototoksisitetssymptomer
I utgangspunktet dukker det opp hodepine med moderat intensitet. Dette følges av oppkast, kvalme og balanse i balansen som kan vedvare i en til to uker. De mest fremtredende symptomene er svimmelhet i oppreist stilling, med problemer med å sitte eller stå uten visuelle signaler.
De akutte symptomene avtar brått og erstattes av manifestasjoner av kronisk labyrintitt i en periode på omtrent to måneder. Gradvis oppstår kompensasjon og da vises bare symptomer når du lukker øynene. Gjenoppretting fra denne fasen krever 12 til 18 måneder.
De fleste av disse pasientene sitter igjen med en viss grad av permanent restskade. Siden det ikke er noen spesifikk behandling for vestibulær skade, er suspensjon av aminoglykosidet ved de første kliniske manifestasjonene det eneste effektive tiltaket for å unngå permanente skader..
- Nyretoksisitet
Omtrent 8 til 25% av pasientene som får behandling med et aminoglykosid i flere dager, utvikler noe reversibel nedsatt nyrefunksjon. Denne toksisiteten er resultatet av akkumulering, konsentrasjon og oppbevaring av aminoglykosider i cellene i den nyrene proksimale tubuli..
Følgelig endres strukturen og funksjonen til den proksimale tubuli. Moderat proteinuria og hyalinavstøt vises først i urinen. Etter flere dager vises en reduksjon i glomerulært filtreringsvolum med en liten økning i plasmakreatininverdier..
Nyreendringer er ofte reversible, siden den proksimale tubuli har kapasitet for regenerering. Nyretoksisitet avhenger av den totale leverte mengden og avhenger av aminoglykosidet som brukes..
Neomycin er et av aminoglykosidene som har større nyretoksisitet, siden det er konsentrert i nyrebarken i mye større mengder enn de andre aminoglykosidene..
- Nevrotoksisitet og andre toksiske effekter
Andre mindre hyppige toksiske effekter er beskrevet, blant dem er nevromuskulær blokkering som kan forårsake luftveisproblemer og / eller lammelse i noen muskler. Endringer i optisk nervefunksjon med utseende av scotomas, som er forbigående områder av blindhet, og perifer neuritt.
Motstand mot aminoglykosider
Motstanden til mikroorganismer mot aminoglykosider kan skyldes en av følgende årsaker: 1) Membranene til bakteriene er ugjennomtrengelige for disse antibiotika 2) ribosomene til disse bakteriene har lav affinitet for antibiotika 3) bakteriene syntetiserer enzymer som inaktiverer aminoglykosidet.
De to første årsakene forklarer den naturlige motstanden mot aminoglykosider. I motsetning til dette forklarer enzyminaktivering den ervervede motstanden som er blitt klinisk beskrevet ved bruk av aminoglykosider..
Genene for syntesen av disse enzymene overføres gjennom plasmider. Plasmider er sirkulære strukturer av ekstrakromosomalt DNA. Disse plasmidene er vidt distribuert i naturen, men spesielt i bakterier rundt sykehusmiljøer..
Plasmider koder for mange enzymer, og disse inaktiverer aminoglykosider. Siden enzymene som inaktiverer hvert aminoglykosid er forskjellige, fører ikke resistens for en nødvendigvis til resistens for en annen..
Imidlertid, selv om dette er tilfelle for streptomycin og gentamicin, vil resistens mot gentamicin (som enzymet som forårsaker det er bifunksjonelt) samtidig presentere motstand mot tobramycin, amikacin, kanamycin og netilmicin..
Indikasjoner
Selv om det er utviklet mindre giftige antibiotika, er bruken av aminoglykosider fortsatt et viktig verktøy for å bekjempe alvorlige infeksjoner forårsaket av enterokokker eller streptokokker..
Gentamicin, amikacin, tobramycin og netilmicin har et bredt spekter mot aerobe gramnegative bakterier. Kanamycin og streptomycin har et smalere spekter og bør ikke brukes til Pseudomonas aeruginosa eller Serratia spp.
Gentamicin brukes sammen med penicillin eller vancomycin for streptokokker og enterokokker. Tobramycin er vant til Pseudomonas aeruginosa og noen arter av Proteus. For nosokomiale infeksjoner (sykehusinfeksjoner) brukes amikacin og netilmicin.
Selv om det foregående representerer de hyppigste indikasjonene for aminoglykosider, bør den rasjonelle bruken av disse antibiotika være basert på kulturen og antibiogrammet til det krenkende middel..
Kontraindikasjoner
Aminoglykosider er kontraindisert hos pasienter med allergiske reaksjoner på disse antibiotika. De bør ikke brukes i tilfeller av sykdommer forårsaket av bakterier som er resistente. De bør ikke brukes under graviditet hvis det er mindre giftige alternativer..
Det er relative kontraindikasjoner hos pasienter med nyresykdom og / eller hørselsproblemer.
Referanser
- Boussekey, N., & Alfandari, S. (2007). Aminoglykosider. EMC-traktaten om medisin, elleve(1), 1-4.
- During-Mangoni, E., Grammatikos, A., Utili, R., & Falagas, M. E. (2009). Trenger vi fortsatt aminoglykosidene? Internasjonal journal over antimikrobielle midler, 33(3), 201-205.
- Goodman og Gilman, A. (2001). Det farmakologiske grunnlaget for terapi. Tiende utgave. McGraw-Hill
- Kotra, L. P., Haddad, J., & Mobashery, S. (2000). Aminoglykosider: perspektiver på virkningsmekanismer og motstand og strategier for å motvirke motstand. Antimikrobielle midler og cellegift, 44(12), 3249-3256.
- Meyers, F. H., Jawetz, E., Goldfien, A., & Schaubert, L. V. (1978). Gjennomgang av medisinsk farmakologi. Lange medisinske publikasjoner.
- Palomino, J. og Pachon, J. (2003) Aminoglykosider, smittsomme sykdommer og klinisk mikrobiologi 21 (2), 105-115.
- Rodríguez-Julbe, M. C., Ramírez-Ronda, C. H., Arroyo, E., Maldonado, G., Saavedra, S., Meléndez, B.,… & Figueroa, J. (2004). Antibiotika hos eldre voksne. Puerto Rico helsevitenskapstidskrift, 2. 3(1).
Ingen har kommentert denne artikkelen ennå.