
Butanal struktur, egenskaper, bruksområder og risikoer
De butanal det er et åpen kjede-aldehyd, som består av fire karbonatomer, og er analogt med butan; det er faktisk den nest mest oksyderte formen av hydrokarbonbutan etter smørsyre. Molekylformelen er CH3CHtoCHtoCHO, hvor -CHO er formylgruppen.
Dette aldehydet, et av de letteste, består av en gjennomsiktig, brennbar væske som er mindre tett enn vann. I tillegg er det løselig i vann og blandbart med de fleste organiske løsningsmidler. derfor kan den brukes til å ha enfasede organiske blandinger.
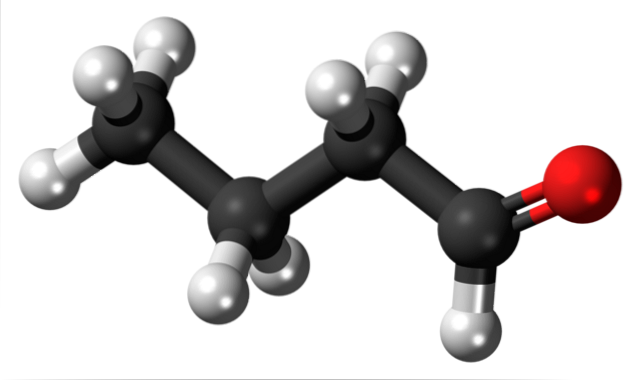
Tilstedeværelsen av karbonylgruppen (den fra den røde sfæren, det øvre bildet) gir kjemisk polaritet til butanalmolekylet, og derfor evnen til å oppleve dipol-dipol-interaksjonen mellom molekylene; selv om det ikke dannes hydrogenbindinger mellom dem.
Dette resulterer i at butanal har høyere kokepunkter og smeltepunkter enn butan, men lavere enn de som presenteres av n-butylalkohol..
Butanal brukes som løsningsmiddel og er et mellomprodukt for å oppnå mange produkter; slik som vulkaniseringsakseleratorer for gummi, harpiks, legemidler og agrokjemikalier.
Butanal er en giftig forbindelse som ved innånding kan forårsake betennelse i øvre luftveier, bronkier og lungeødem som til og med kan få fatale konsekvenser..
Artikkelindeks
- 1 Struktur av butanal
- 1.1 Konformatorer
- 2 eiendommer
- 2.1 Kjemiske navn
- 2.2 Molekylformel
- 2.3 Fysisk utseende
- 2.4 Lukt
- 2.5 Kokepunkt
- 2.6 Smeltepunkt
- 2.7 Flammepunkt
- 2.8 Løselighet i vann
- 2.9 Løselighet i organiske løsningsmidler
- 2.10 Tetthet
- 2.11 Damptetthet
- 2.12 Damptrykk
- 2.13 Selvantennelse
- 2.14 Viskositet
- 2.15 Forbrenningsvarme
- 2.16 Fordampningsvarme
- 2.17 Overflatespenning
- 2.18 Luktterskel
- 2.19 Brytningsindeks
- 2.20 Dipolemoment
- 2,21 Bølgelengder (λ) for maksimal absorpsjon i vann
- 2.22 Polymerisering
- 2.23 Reaktivitet
- 2.24 Aldol-kondens
- 3 Syntese
- 4 bruksområder
- 4.1 Industriell
- 4.2 Andre
- 5 risikoer
- 6 Referanser
Butanal struktur
Det ble nettopp nevnt at formylgruppen, -CHO, overfører polaritet til butanal- eller butyraldehydmolekylet på grunn av den høyere elektronegativiteten til oksygenatomet. Som et resultat av dette, kan molekylene samhandle med hverandre gjennom dipol-dipolkrefter..
På det øvre bildet er det vist, med en modell av kuler og stenger, at butanalmolekylet har en lineær struktur. Kullet i -CHO-gruppen har SP-hybridiseringto, mens de resterende karbonene sp hybridiserer3.
Ikke bare det, men det er også fleksibelt, og koblingene kan rotere på sine egne akser; og dermed genereres forskjellige konformasjoner eller samsvar (samme forbindelse, men med koblingene rotert).
Tilpassere
Følgende bilde forklarer dette poenget bedre:
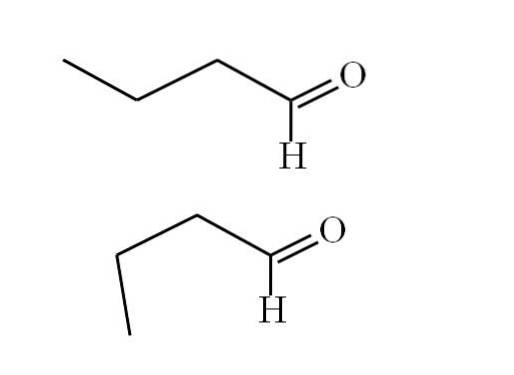
Den første konformeren (den øvre) tilsvarer molekylet i det første bildet: metylgruppen til venstre, -CH3, og gruppen -CHO, er i posisjoner som er parallelle med hverandre; den ene peker opp og den andre ned.
I mellomtiden tilsvarer den andre konformeren (den nedre) molekylet med -CH3 og -CHO i formørkede stillinger; det vil si at de begge peker i samme retning.
Begge konformatorene er raskt utskiftbare, og derfor roterer og vibrerer butanalmolekylet konstant; og la til det faktum at den har en permanent dipol, dette gjør at interaksjonene kan være sterke nok til å koke ved 74,8 ° C..
Eiendommer
Kjemiske navn
-Butanal
-Butyraldehyd
-1-Butanal
-Butyral
-N-butyraldehyd.
Molekylær formel
C4H8O eller CH3CHtoCHtoCHO.
Fysisk utseende
Det er en klar, gjennomsiktig væske.
Lukt
Karakteristisk, skarp, aldehyd lukt.
Kokepunkt
167 ºF til 760 mm Hg (74,8 ºC).
Smeltepunkt
-146 ºF (-96,86 ºC).
antennelsespunkt
-8 ° F (-22 ° C) lukket kopp.
Vannløselighet
7 g / 100 ml ved 25 ºC.
Løselighet i organiske løsningsmidler
Blandbar med etanol, eter, etylacetat, aceton, toluen og mange andre organiske løsningsmidler.
Tetthet
0,803 g / cm3 ved 68 ºF.
Damptetthet
2,5 (i forhold til luft tatt lik 1).
Damptrykk
111 mmHg ved 25 ºC.
Selvantennelse
446ºF. 21,8 ºC.
Viskositet
0,45 cPoise ved 20 ° C.
Forbrenningsvarme
2479,34 kJ / mol ved 25 ºC.
Fordampningsvarme
33,68 kJ / mol ved 25 ºC.
Overflatespenning
29,9 dyne / cm ved 24 ºC.
Luktterskel
0,009 spm.
Brytningsindeks
1,3843 ved 20 ºC.
Dipole øyeblikk
2,72 D.
Bølgelengder (λ) for maksimal absorpsjon i vann
225 nm og 282 nm (ultrafiolett lys).
Polymerisering
Butanal kan polymerisere i kontakt med baser eller syrer, og polymerisering er farlig.
Reaktivitet
Når det utsettes for luft oksiderer det og danner smørsyre. Ved en temperatur på 230 ° C antennes butanal spontant med luft.
Aldol kondens
To molekyler av butanal kan reagere med hverandre, i nærvær av KOH og en temperatur på 6-8 ° C, for å danne forbindelsen 2-etyl-3-hydroksyheksanol. Denne typen forbindelse kalles aldol, siden den i sin struktur har en aldehydgruppe og en alkoholholdig gruppe.
Syntese
Butanal kan produseres ved katalytisk dehydrogenering av n-butylalkohol; katalytisk hydrogenering av krotonaldehyd; og hydroformylering av propylen.
applikasjoner
Industriell
-Butanal er et industrielt løsningsmiddel, men det er også et mellomprodukt i syntesen av andre løsningsmidler; for eksempel 2-etylheksanol, n-butanol og trimetylpropan.
-Det brukes også som et mellomprodukt i produksjonen av syntetiske harpikser, inkludert polyvinylbutyral; gummi vulkanisering akseleratorer; produksjon av farmasøytiske produkter; plantevernprodukter; plantevernmidler; antioksidanter; solarium hjelpemidler.
-Butanal brukes som råvare for produksjon av syntetiske aromaer. I tillegg brukes den som et smaksstoff for mat.
Andre
-Hos mennesker brukes butanal som en biomarkør som indikerer oksidativ skade på lipider, proteiner og nukleinsyrer.
-Det ble brukt eksperimentelt, sammen med formalin og glutardehyd, for å prøve å redusere mykning som storfeens hover opplevde på grunn av eksponering for vann, urin og avføring fra storfeene selv. De eksperimentelle resultatene var positive.
Risiko
Butanal er ødeleggende for slimhinner i øvre luftveier, så vel som for vev i huden og øynene..
Ved hudkontakt forårsaker rødhet og forbrenning. I øynene oppstår de samme skadene, ledsaget av smerte og skade på øyevevet.
Innånding av butanal kan ha alvorlige konsekvenser, siden det kan forårsake betennelse og ødem i strupehodet og bronkiene; mens det er i lungene, produserer det kjemisk lungebetennelse og lungeødem.
Tegn på overeksponering inkluderer: brennende følelser i øvre luftveier, hoste, tungpustethet, dvs. hvesing når du puster; laryngitt, kortpustethet, hodepine, kvalme og også oppkast.
Innånding kan være dødelig som følge av spasmer i luftveiene.
Inntak av butanal forårsaker en følelse av "svie" i fordøyelseskanalen: munnhulen, svelget, spiserøret og magen.
Referanser
- Morrison, R. T. og Boyd, R. N. (1987). Organisk kjemi. (5ta Utgave.). Redaksjonell Addison-Wesley Iberoamericana.
- Carey F. (2008). Organisk kjemi. (Sjette utgave). Mc Graw Hill.
- PubChem. (2019). Butanal. Gjenopprettet fra: pubchem.ncbi.nim.nih.guv
- Wikipedia. (2019). Butanal. Gjenopprettet fra: es.wikipedia.org
- Kjemisk bok. (2017). Butanal. Gjenopprettet fra: chemicalbook.com
- Basf. (Mai 2017). N-butyraldehyd. [PDF]. Gjenopprettet fra: solvents.basf.com

Ingen har kommentert denne artikkelen ennå.