
Ester Bond egenskaper og typer

EN esterbinding er definert som bindingen mellom en alkoholgruppe (-OH) og en karboksylsyregruppe (-COOH), dannet ved eliminering av et vannmolekyl (HtoO) (Futura-Sciences ,, S.F.).
Strukturen til etylacetat er vist i figur 1. Esterbindingen er den enkeltbindingen som dannes mellom oksygenet i karboksylsyren og karbonet i etanol.

R-COOH + R'-OH → R-COO-R '+ HtoELLER
På figuren tilsvarer den blå delen den delen av forbindelsen som kommer fra etanol og den gule delen tilsvarer eddiksyre. Esterbindingen er markert i den røde sirkelen.
Artikkelindeks
- 1 Hydrolyse av esterbindingen
- 2 typer ester
- 2.1 Karbonsyreester
- 2.2 Fosforsyreester
- 2.3 Svovelester
- 3 Referanser
Hydrolyse av esterbindingen
For å forstå litt bedre arten av esterbindinger, blir reaksjonsmekanismen for hydrolysen av disse forbindelsene forklart. Esterbindingen er relativt svak. I surt eller basisk medium hydrolyseres det til å danne henholdsvis alkohol og karboksylsyre. Reaksjonsmekanismen for hydrolyse av estere er godt studert.
I basisk medium angriper nukleofile hydroksider først den elektrofile C av C = O-esteren, bryter π-bindingen og skaper det tetraedriske mellomproduktet..
Mellomproduktet kollapser deretter, og reformerer C = O, noe som resulterer i tap av den utgående gruppen, alkoksydet, RO-, som fører til karboksylsyren..
Til slutt er en syre / basereaksjon en veldig rask likevekt der alkoksidet, RO- fungerer som en base som deprotonerer karboksylsyren, RCO2H, (en syrebehandling vil tillate at karboksylsyren oppnås fra reaksjonen).

Mekanismen for hydrolyse av esterbindingen i et surt medium er litt mer komplisert. En syre / base reaksjon oppstår først, siden du bare har en svak nukleofil og en dårlig elektrofil, trenger du for å aktivere esteren.
Protonering av karbonylesteren gjør den mer elektrofil. I det andre trinnet fungerer oksygenet i vannet som nukleofilen ved å angripe det elektrofile C i C = O, med elektronene som beveger seg mot hydroniumionen, og skaper det tetraedriske mellomproduktet..
I det tredje trinnet oppstår en syre / base-reaksjon, som depoterer oksygenet som kommer fra vannmolekylet for å nøytralisere ladningen..
I det fjerde trinnet oppstår en annen syre / basereaksjon. Du må få -OCH3 ut, men du må gjøre den til en god gruppe som forlater ved protonasjon.
I det femte trinnet bruker de elektroner fra et tilstøtende oksygen for å "presse ut" den utgående gruppen og produsere et nøytralt alkoholmolekyl..
I det siste trinnet oppstår en syre / base reaksjon. Deprotonering av hydroniumion avslører C = O karbonyl i karboksylsyreproduktet og regenererer syrekatalysatoren (Dr. Ian Hunt, S.F.).
Ester-typer
Karbonsyreester
Karbonestere er de vanligste av denne typen forbindelser. Den første karbonesteren var etylacetat eller også kalt etyletanoat. Tidligere var denne forbindelsen kjent som eddiketer, hvis navn på tysk er Essig-Äther hvis sammentrekning ble avledet av navnet på denne typen forbindelse.
Estere finnes i naturen og brukes mye i industrien. Mange estere har karakteristiske fruktluker, og mange er naturlig tilstede i essensielle oljer fra planter. Dette har også ført til vanlig bruk i kunstige dufter og dufter når lukt prøver å bli etterlignet..
Det produseres flere milliarder kilo polyestere årlig, viktige produkter som de er; polyetylentereftalat, akrylatestere og celluloseacetat.
Esterbindingen av karboksylestere er ansvarlig for dannelsen av triglyserider i levende organismer.
Triglyserider finnes i alle celler, men hovedsakelig i fettvev, de er den viktigste energireserven som kroppen har. Triacylglyserider (TAG) er glyserolmolekyler knyttet til tre fettsyrer gjennom en esterbinding. Fettsyrene som er tilstede i TAG er overveiende mettet (Wilkosz, 2013).
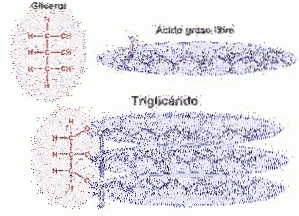
Triacylglyserider (triglyserider) syntetiseres i praktisk talt alle celler. Hovedvevet for syntesen av TAG er tynntarmen, leveren og adipocyttene. Med unntak av tarmen og adipocyttene, begynner TAG-syntese med glyserol.
Glyserol fosforyleres først med glyserolkinase, og deretter aktiveres fettsyrer (fettacyl-CoAer) som substrater for tilsetning av fosfatid-syre-genererende fettsyrer. Fosfatgruppen fjernes og den siste fettsyren tilsettes.
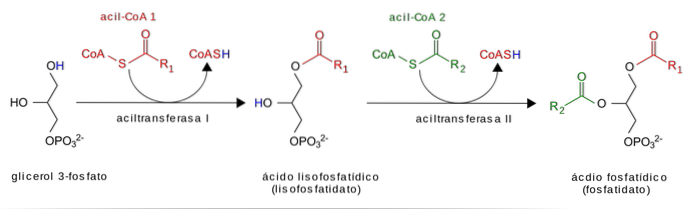
I tynntarmen hydrolyseres diett-TAG-er for å frigjøre fettsyrer og monoacylglyserider (MAG) før opptak av enterocytter. Enterocyte MAGs fungerer som substrater for acylering i en totrinnsprosess som produserer en TAG.
Innen fettvev er det ikke noe uttrykk for glyserolkinase, så byggesteinen for TAG i dette vevet er det glykolytiske mellomproduktet, dihydroxyaceton phosphate, DHAP.
DHAP reduseres til glyserol-3-fosfat av cytosolisk glyserol-3-fosfatdehydrogenase, og den gjenværende TAG-syntesereaksjonen er den samme som for alle andre vev.
Fosforsyreester
Fosforsyreestere produseres ved dannelse av en esterbinding mellom en alkohol og fosforsyre. Gitt strukturen til syren, kan disse estrene være mono, di og trisubstituert.
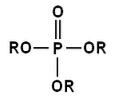
Disse typer esterbindinger finnes i forbindelser som fosfolipider, ATP, DNA og RNA..
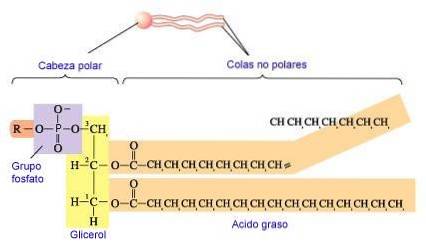
Fosfolipider syntetiseres ved dannelse av en esterbinding mellom en alkohol og fosfatidinsyrefosfat (1,2-diacylglyserol-3-fosfat). De fleste fosfolipider har en mettet fettsyre på C-1 og en umettet fettsyre på C-2 i glyserolrygraden.
De vanligste tilsatte alkoholene (serin, etanolamin og kolin) inneholder også nitrogen som kan bli positivt ladet, mens glyserol og inositol ikke gjør det (King, 2017).
Adenosintrifosfat (ATP) er et molekyl som brukes som energivaluta i cellen. Dette molekylet er sammensatt av et adeninmolekyl knyttet til ribosemolekylet med tre fosfatgrupper (figur 8).
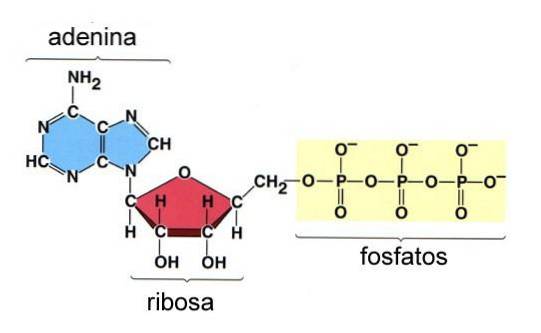
De tre fosfatgruppene i molekylet kalles gamma (γ), beta (β) og Alpha (α), sistnevnte forestrer C-5 hydroksylgruppen av ribose.
Bindingen mellom ribose og α-fosforylgruppen er en fosfoesterbinding fordi den inkluderer et karbonatom og et fosforatom, mens β- og γ-fosforylgruppene i ATP er forbundet med fosfoanhydridbindinger som ikke involverer karbonatomer..
All fosfoanhydro har betydelig kjemisk potensiell energi, og ATP er ikke noe unntak. Denne potensielle energien kan brukes direkte i biokjemiske reaksjoner (ATP, 2011).
En fosfodiesterbinding er en kovalent binding der en fosfatgruppe er bundet til tilstøtende karbon gjennom esterbindinger. Bindingen er resultatet av en kondensasjonsreaksjon mellom en hydroksylgruppe med to sukkergrupper og en fosfatgruppe.
Diesterbindingen mellom fosforsyre og to sukkermolekyler i DNA og ryggrad RNA binder to nukleotider sammen for å danne oligonukleotidpolymerer. Fosfodiesterbindingen knytter et 3'-karbon til et 5'-karbon i DNA og RNA.
(base1) - (ribose) -OH + HO-P (O) 2-O- (ribose) - (base 2)
(base1) - (ribose) - O - P (O) 2 - O- (ribose) - (base 2) + HtoELLER
Under reaksjonen av to av hydroksylgruppene i fosforsyre med en hydroksylgruppe i to andre molekyler, dannes to esterbindinger i en fosfodiestergruppe. En kondensasjonsreaksjon der et vannmolekyl går tapt genererer hver esterbinding.
Under polymerisasjonen av nukleotider for å danne nukleinsyrer, fester hydroksylgruppen i fosfatgruppen seg til 3'-karbonet i et sukker av ett nukleotid for å danne en esterbinding til fosfatet til et annet nukleotid.
Reaksjonen danner en fosfodiesterbinding og fjerner et vannmolekyl (fosfodiest bindingsdannelse, S.F.).
Svovelester
Svovelestere eller tioestere er forbindelser med den funksjonelle gruppen R-S-CO-R '. De er produktet av forestringen mellom en karboksylsyre og en tiol eller med svovelsyre (Block, 2016).
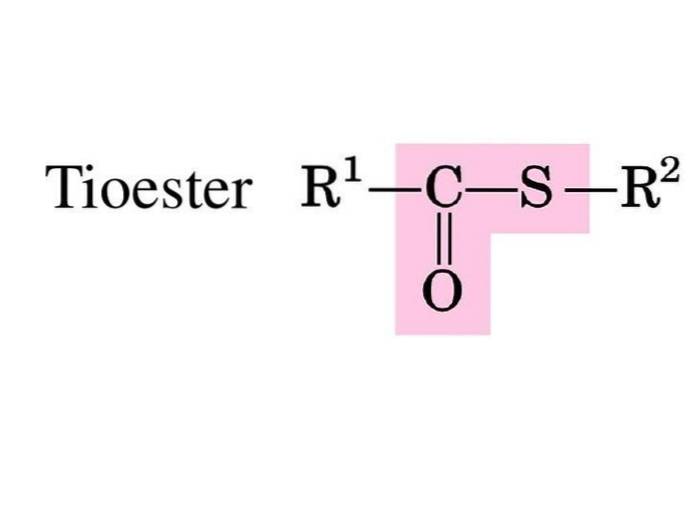
I biokjemi er de mest kjente tioestrene derivater av koenzym A, for eksempel acetyl-CoA.
Acetylkoenzym A eller acetyl-CoA (figur 8) er et molekyl som deltar i mange biokjemiske reaksjoner. Det er et sentralt molekyl i metabolismen av lipider, proteiner og karbohydrater.
Hovedfunksjonen er å levere acetylgruppen til sitronsyresyklusen (Krebs-syklusen) som skal oksyderes for energiproduksjon. Det er også forløpermolekylet for syntese av fettsyrer og er et produkt av nedbrytningen av noen aminosyrer.
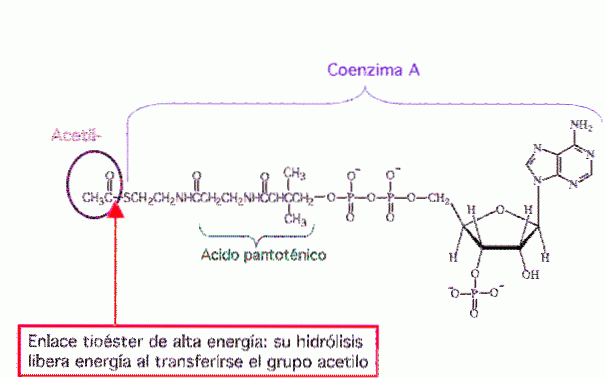
De CoA-aktiverte fettsyrene nevnt ovenfor er andre eksempler på tioestere som stammer fra muskelcellen. Oksidasjonen av fettsyre-CoA-tioestere skjer faktisk i diskrete vesikulære legemer som kalles mitokondrier (Thompson, 2015).
Referanser
- ATP. (2011, 10. august). Gjenopprettet fra learnbiochemistry.wordpress: learnbiochemistry.wordpress.com.
- Block, E. (2016, 22. april). Organisk svovelforbindelse. Hentet fra britannica: britannica.com.
- Ian Hunt. (S.F.). Hydrolyse av estere. Gjenopprettet fra chem.ucalgary.ca: chem.ucalgary.ca.
- Futura-Sciences,. (S.F.). Ester bond. Gjenopprettet fra futura-sciences.us.
- King, M. W. (2017, 16. mars). Fettsyre, triglyserider og fosfolipidsyntese og metabolisme. Gjenopprettet fra themedicalbiochemistrypage.org.
- fosfodiest bindingsdannelse. (S.F.). Gjenopprettet fra biosyn: biosyn.com.
- Thompson, T. E. (2015, 19. august). Lipid. Gjenopprettet fra britannica: britannica.com.
- Wilkosz, R. (2013, 6. november). Dannelsen av esterobligasjoner i syntesen av lipider. Gjenopprettet fra wisc-online.com.



Ingen har kommentert denne artikkelen ennå.