
Fucosa egenskaper, struktur, funksjoner
De fucose (forkortet Fuc), eller 6-L-deoxy-galactose, er et delvis deoxygenated (deoxysugar) seks-karbon monosakkarid hvis empiriske formel er C6H12ELLER5. Som andre monosakkarider, er det et flervann sukker.
Når en hydroksylgruppe erstattes av et hydrogenatom, avledes en deoksysukker. Selv om denne erstatningen teoretisk kan påvirke hvilken som helst hydroksylgruppe av ethvert monosakkarid, er det i naturen lite utvalg av deoksysukker..
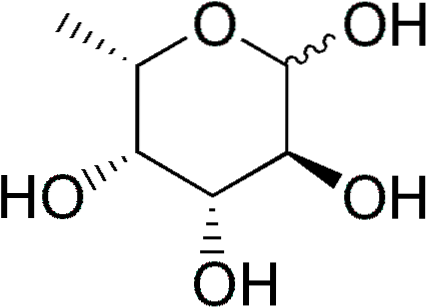
Noen deoksysukker er: 1) deoksyribose (2-deoksy-D-ribose), avledet fra D-ribose, som er en del av DNA; 2) rhamnose (6-D-deoksymannose), avledet fra D-mannose; 3) fukose, avledet fra L-galaktose. Sistnevnte er mer vanlig enn D-fukose, avledet fra D-galaktose.
Artikkelindeks
- 1 Egenskaper og struktur
- 2 Distribusjon i naturen
- 3 Fukosemetabolisme
- 4 funksjoner
- 4.1 Roll i kreft
- 4.2 Roll i andre sykdommer
- 4.3 Biomedisinsk potensial
- 5 Referanser
Kjennetegn og struktur
Fukose er også kjent med navnene 6-deoksy-galakto-heksose, fukopyranose, galaktometylose og rodeose..
Selv om det vanligvis finnes i dannelse av polysakkarider og glykoproteiner, er det isolert som et monosakkarid søtere enn galaktose. Dette skyldes det faktum at erstatning av en hydroksylgruppe med et hydrogenatom øker den hydrofobe karakteren og derfor molekylets søthet..
Hydroksylgruppene av fukose kan gjennomgå de samme reaksjonene som andre sukkerarter, og produsere et bredt utvalg av acetaler, glykosider, etere og estere..
En fukosylert biomolekyl er en som fucosemolekyler har blitt festet gjennom glykosidbindinger ved virkningen av en fukosyltransferase. Når hydrolysen av glykosidbindinger skjer ved virkningen av en fukosidase, og dermed skiller fukosen, sies det at biomolekylet er defukosylert.
Når glukaner fukosyleres, genereres mer komplekse glukaner kalt fukaner, som kanskje eller ikke er en del av glykoproteiner. Sulfaterte fukaner er definert som de polysakkarider som inneholder sulfaterte L-fukoserester. De er typiske for brunalger. Eksempler inkluderer askofylan, sargasan og pelvetan..
En av de best studerte fukanene er fucoidan, hentet fra brune alger Fucus vesiculosus, som har blitt markedsført (Sigma-Aldrich Chemical Company) i flere tiår.
Distribusjon i naturen
D-fukose er til stede i antibiotika som produseres av mikrober, og i plante glykosider, slik som convolvulin, chartreusin, ledienoside og keirotoxin.
L-fukose er en bestanddel av polysakkarider fra alger, plommer, lin-, soya- og rapsfrø, tyggegummi, potetcellevegger, kassava-knoller, kiwifrukt, barken av ceiba og mucigel av maiskaliptra, samt andre planter.
L-fukose er også tilstede i kråkeboller og i gelatinen som beskytter froskeegg.
Hos pattedyr danner fukaner med L-fukose ligandene som virker på selectin-mediert leukocyttendoteladhesjon, og deltar i en rekke ontogenetiske hendelser.
L-fukose er rikelig i fukosfingolipider i gastrointestinalt epitel og benmarg, og vises i små proporsjoner i brusk og keratinstrukturer.
Hos mennesker er L-fukosefukaner en del av glykoproteiner i spytt og magesaft. De er også en del av antigenene som definerer ABO-blodgrupper. De er tilstede i forskjellige oligosakkarider i morsmelk.
Fukosemetabolisme
Fukosyltransferaser bruker BNP-fukose, en nukleotidaktivert form av fukose, som en fukose-donor i konstruksjonen av fukosylerte oligosakkarider.
BNP-fukose er avledet fra BNP-mannose ved den påfølgende virkningen av to enzymer: BNP-mannose 4,6-dehydratase og BNP-4-keto-6-deoximanose 3,5-epimerase-4-reduktase.
Ved hjelp av en NADP + kofaktor katalyserer det første enzymet dehydrering av BNP-mannose. Reduksjon av posisjon 6 og oksidasjon av posisjon 4 produserer BNP-6-deoksy-4-keto-mannose (under reaksjonen overføres hybrid fra posisjon 4 til 6 av sukkeret).
Det andre enzymet, som er NADPH-avhengig, katalyserer epimeriseringen av posisjonene 3 og 5, og reduksjonen av 4-ketogruppen, av BNP-6-deoksy-4-ketomannose..
Bakterier kan vokse ved å bruke fukose som den eneste kilden til karbon og energi ved hjelp av et fukoseinduserbart operon som koder for katabolske enzymer for dette sukkeret..
Ovennevnte prosess involverer: 1) innføring av fri fukose gjennom celleveggen formidlet av en permease; 2) isomerisering av fukose (en aldose) for å danne fukulose (en ketose); 3) fosforylering av fukulose for å danne fukulose-1-fosfat; 4) en aldolasereaksjon for å danne laktaldehyd og dihydroksyacetonfosfat fra fukulose-1-fosfat.
Funksjoner
Roll i kreft
Symptomer på mange typer kreftsvulster inkluderer tilstedeværelsen av glukanbundne proteiner som kjennetegnes ved å ha en endret oligosakkaridsammensetning. Tilstedeværelsen av disse unormale glukanene, blant hvilke fukaner skiller seg ut, er knyttet til maligniteten og det metastatiske potensialet til disse svulstene..
I brystkreft inkorporerer tumorceller fukose i glykoproteiner og glykolipider. Fukose bidrar til progresjonen av denne kreften, og favoriserer aktivering av kreftstamceller, hematogen metastase og invasjonen av svulster gjennom ekstracellulære matriser.
Ved lungekarsinom og hepatokarsinogenese er økt fukoseuttrykk assosiert med et høyt metastatisk potensiale og lav sannsynlighet for overlevelse.
I kontrast er noen sulfaterte fukaner lovende stoffer i behandlingen av kreft, som det er blitt bestemt av mange in vitro-studier med kreftcellelinjer, inkludert de som forårsaker bryst-, lunge-, prostata-, mage-, tykktarm- og endetarmskreft..
Roll i andre sykdommer
Økt ekspresjon av fukaner i serumimmunglobuliner har vært assosiert med juvenil og voksen revmatoid artritt.
Leukocyttadhesjonsmangel II er en sjelden medfødt sykdom på grunn av mutasjoner som endrer aktiviteten til en FDP-fukosetransportør i Golgi-apparatet.
Pasienter lider av mental og psykomotorisk retardasjon, og lider av tilbakevendende bakterieinfeksjoner. Denne sykdommen reagerer gunstig på orale doser av fukose.
Biomedisinsk potensial
Sulfaterte fukaner oppnådd fra brune alger er viktige reservoarer av forbindelser med terapeutisk potensial.
De har antiinflammatoriske og antioksidantegenskaper, som hemmer migrasjonen av lymfocytter på infeksjonssteder og favoriserer frigjøring av cytokiner. Øk immunresponsen ved å aktivere lymfocytter og makrofager.
De har antikoagulerende egenskaper. Oralt vist å hemme blodplateaggregasjon hos humane pasienter.
De har antibiotika og antiparasitt potensial og hemmer veksten av magepatogene bakterier Helicobacter pylori. Drep parasitter Plasmodium spp. (forårsakende middel til malaria) og Leishmania donovani (forårsakende middel for amerikansk viscerotropisk leishmaniasis).
Til slutt har de kraftige antivirale egenskaper, som hemmer inngangen til cellen av flere virus av stor betydning for menneskers helse, inkludert Arenavirus, Cytomegalovirus, Hantavirus, Hepadnavirus, HIV, herpes simplex-virus og influensavirus.
Referanser
- Becker, D. J., Lowe, J. B. 2003. Fucose: biosyntese og biologisk funksjon hos pattedyr. Glykobiologi, 13, 41R-53R.
- Deniaud-Bouët, E., Hardouin, K., Potin, P., Kloareg, B., Hervé, C. 2017. En gjennomgang om brune algecellevegger og fukoseholdige sulfaterte polysakkarider: celleveggkontekst, biomedisinske egenskaper og nøkkel forskning utfordrer karbohydratpolymerer, http://dx.doi.org/10.1016/j.carbpol.2017.07.082.
- Flowers H. M. 1981. Kjemi og biokjemi av D- og L-fukose. Fremskritt innen karbohydratkjemi og biokjemi, 39, 279-345.
- Listinsky, J. J., Siegal, G. P., Listinsky, C. M. 2011. Den voksende viktigheten av α-L-fukose i brystkreft hos mennesker: en gjennomgang. Am. J. Transl. Res., 3, 292-322.
- Murray, R. K., et al. 2003. Harpers illustrerte biokjemi. McGraw-Hill, New York.
- Pereira, L. 2018. Terapeutisk og ernæringsmessig bruk av alger. CRC Press, Boca Raton.
- Staudacher, E., Altmann, F., Wilson, I. B. H., März, L. 1999. Fucose i N-glykaner: fra plante til menneske. Biochimica et Biophysica Acta, 1473, 216-236.
- Tanner, W., Loewus, F. A. 1981. Plantekarbohydrater II. Ekstracellulære karbohydrater. Springer, New York.
- Vanhooren, P. T., Vandamme, E. J. 1999. L-fucose: forekomst, fysiologisk rolle, kjemisk, enzymatisk og mikrobiell syntese. Journal of Chemical Technology and Biotechnology, 74, 479-497.



Ingen har kommentert denne artikkelen ennå.